运动能对全身产生重大影响:MIT/哈佛团队绘制“运动减肥”的基因和细胞通路
时间:2022-10-13 16:08:19 热度:37.1℃ 作者:网络
众所周知,高脂肪饮食容易让人变胖;而有规律的运动是对抗肥胖、糖尿病等多种代谢疾病的有效干预手段。确定这一过程中产生有益影响的分子机制可以为肥胖等代谢疾病提供治疗靶点。然而,这是一项具有挑战性的任务。因为,高脂肪饮食会推动所有细胞和系统向一个方向发展(变胖);而运动又推动了几乎所有细胞和系统向其相反的方向发展(减肥)。这一复杂相互作用的潜在机制仍难以捉摸。
2022年10月4日,美国麻省理工学院 Manolis Kellis 团队和哈佛医学院 Laurie J. Goodyear 团队合作在 Cell 子刊 Cell Metabolism 上发表了题为:Single-cell dissection of the obesity-exercise axis in adipose-muscle tissues implies a critical role for mesenchymal stem cells 的研究论文。
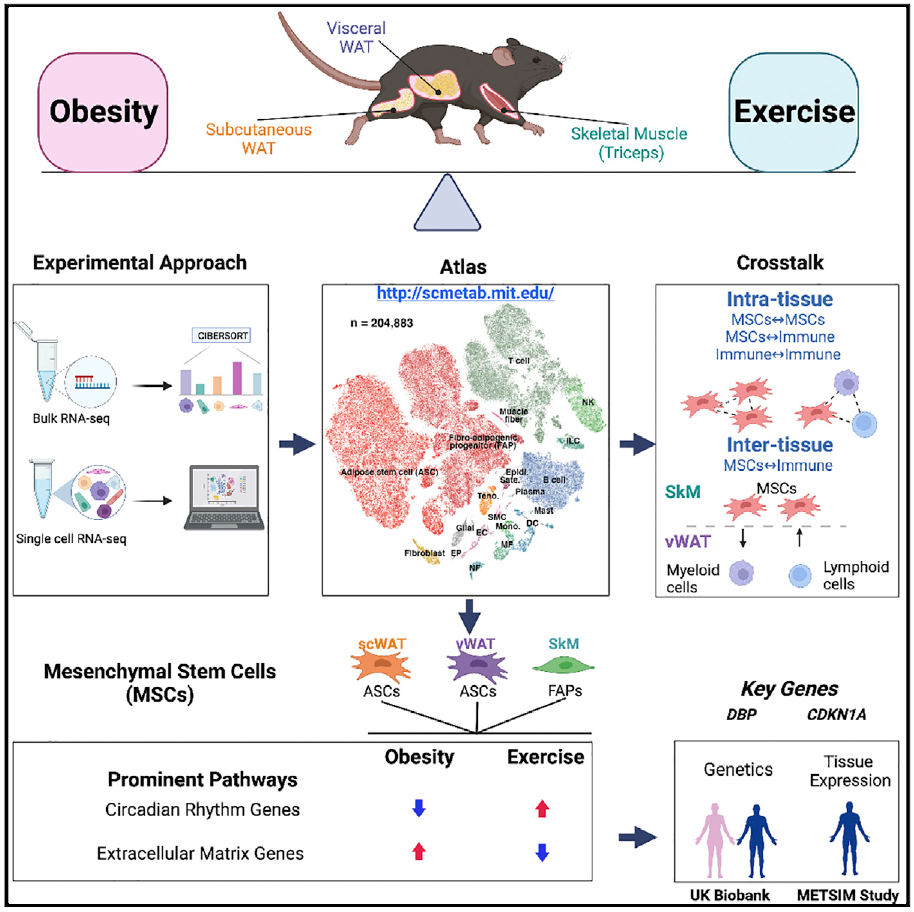
研究团队利用单细胞技术和计算生物学,通过同时研究运动和肥胖在分子、细胞类型特异性和跨组织水平上的反应绘制出许多被运动或高脂肪饮食改变的细胞、基因和细胞通路,从而证实运动真的能对全身产生重大影响。该研究扩展了科学家们对运动和饮食如何影响身体的理解。这些发现可以为开发增强或模拟运动益处的药物提供潜在的靶点。

FTO 基因是一种与肥胖相关的等位基因,也称肥胖基因。在携带 FTO 基因变异的人中,如果两个副本均变异,其肥胖几率会比正常人群高出70%;如果只有一个副本变异,肥胖几率也会比常人高出30%。
2015年,Manolis Kellis 实验室在《新英格兰医学杂志》(NEJM)发表的研究表明,FTO 基因区域与肥胖风险密切相关。该区域的基因控制着一种通路,促使脂肪祖细胞的未成熟脂肪细胞变为脂肪燃烧细胞或脂肪存储细胞。

这一发现证明了肥胖的遗传因素,也促使了 Manolis Kellis 实验室开始研究运动如何在细胞水平上作用于脂肪祖细胞。
白色脂肪组织(WAT)和骨骼肌(SkM)分别是最受肥胖和运动影响的组织(之一)。因此,一直是在组织水平上研究的重点。
为了探索这个复杂的问题,Manolis Kellis 团队决定对小鼠骨骼肌、内脏白色脂肪组织(vWAT)和皮下白色脂肪组织(scWAT)进行单细胞 RNA 测序。vWAT 聚集在内脏器官周围,主要储存脂肪;scWAT 存在于皮肤下,主要负责燃烧脂肪。这些组织来自四个不同实验组的小鼠。两组小鼠被分别喂食正常饮食和高脂肪饮食。三周后,两组动物又被进一步分为久坐组和运动组。
研究人员在所有三种组织中发现了1386个组织水平差异表达基因。基因本体论途径富集和蛋白质-蛋白质相互作用分析揭示了干预措施和组织之间共同和独特的生物学过程。

他们还生成了一个包含204883个细胞的单细胞图谱,用于研究肥胖-运动相互作用。通过分析这些小鼠的组织,研究人员可以全面地对53种不同细胞类型中被运动激活或抑制的基因进行分类。
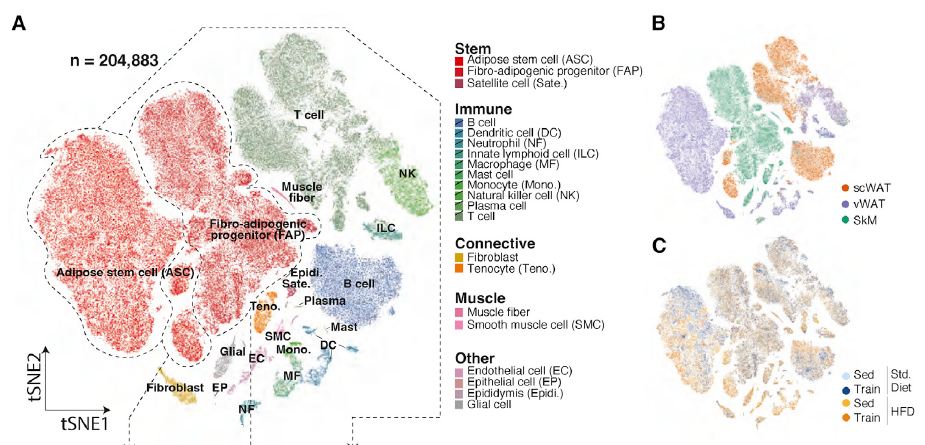
他们观察到在所有三种类型的组织中,间充质干细胞(MSC)似乎控制了他们观察到的许多饮食和运动诱导的影响。间充质干细胞是一种可以分化为其他类型细胞的干细胞,包括脂肪细胞和成纤维细胞。研究团队发现,在脂肪组织中,高脂肪饮食调节了间充质干细胞分化为脂肪储存细胞,而运动则逆转了这种作用。
除了促进脂肪储存,研究人员发现高脂肪饮食还刺激间充质干细胞分泌重塑细胞外基质的因子。细胞外基质(ECM)是一种蛋白质和其他分子组成的网络,包围并支持体内的细胞和组织。ECM的重塑有助于为扩大的脂肪存储细胞提供结构,同时还创造了一个更具炎症性的环境。
Manolis Kellis 表示,随着脂肪细胞的脂质超载,压力会非常大,这会进一步导致低度炎症。这种炎症是全身性的并且可以长期存在。这也是导致肥胖的许多不利影响因素之一。
他们还发现,高脂肪饮食和运动对控制昼夜节律的细胞通路具有相反的影响。昼夜节律即生物钟,是一个以24小时为周期,控制着机体从睡眠到体温、激素释放以及消化等许多生理功能的系统。研究表明,运动可以促进调节昼夜节律基因的表达;而高脂肪饮食则起到了相反的作用。
随后,该团队将他们的研究结果与代谢特征相关的人类基因数据库进行了比较。从而证实,在这项研究中发现的两种昼夜节律基因,即DBP和CDKN1A,具有与人类较高肥胖风险相关的遗传变异。
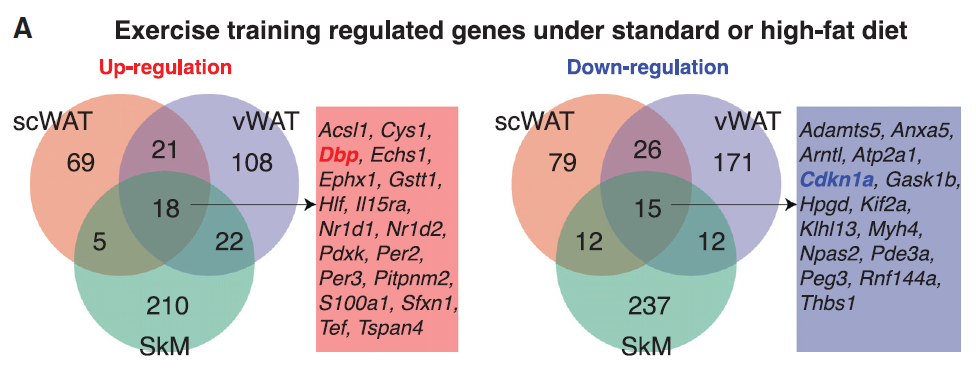
研究团队表示,这些结果帮助他们了解这些靶点的转化价值,以及如何潜在靶向特定细胞类型中的特定生物过程。
目前,该团队正在分析这项研究中使用的小鼠小肠、肝脏和脑组织样本,以探索运动和高脂肪饮食对这些组织的影响。他们还与人类志愿者一起进行血液样本和活组织检查,并研究人类和小鼠生理学之间的异同。他们希望他们的发现将有助于指导药物开发人员设计可以模仿运动某些有益效果的药物。
最后, Manolis Kellis 教授总结道,给每个人的建议应该是,尽可能选择健康的饮食,多锻炼身体;而对于那些无法做到这些的人来说,这项研究表明,我们未来应该可以操纵特定基因、特定分子和细胞过程,以通过治疗实现同样的有益效果。
论文链接:
https://doi.org/10.1016/j.cmet.2022.09.004
https://www.nejm.org/doi/full/10.1056/nejmoa1502214


