《柳叶刀 · 血液》丨中国CAR-T细胞疗法:快速崛起,未来光明
时间:2022-12-15 18:00:08 热度:37.1℃ 作者:网络
近日,国际知名刊物《柳叶刀-血液病学》(The Lancet Haematology,IF=30.153)刊登了一篇评论性综述,本综述回顾与总结CAR-T细胞疗法的开发和临床应用的十年历程。
在创新和临床应用方面,中美处于并跑状态,但中国在原始靶点创新与商业化方面上有待提升。未来,以干细胞、合成生物学和基因编辑等技术为基础的下一代CAR-T细胞治疗,将在中国迅速崛起,且未来光明。文章题目如下:CAR-T-cell therapies in China: rapid evolution and a bright future”(中国CAR-T细胞疗法:快速崛起,未来光明)
 -01-中国CAR-T临床试验概况
-01-中国CAR-T临床试验概况
▉ 中国的临床试验概况
截至2021年11月15日,中国已有714项CAR-T细胞疗法的临床研究注册,其中ClinicalTrials.gov 510项、中国临床试验登记研究204项,到2021年,中美CAR-T临床试验注册总数出现了下滑,而在前几年一直是增加的态势(图1A)。
在地区分布方面,中国CAR-T细胞治疗临床研究主要分布在北京 (n= 84)、广东 (n= 65)、浙江 (n= 65)、江苏 (n= 59) 和上海(n= 54;图1B)等医疗资源集中、科研水平较高和经济较发达地区(图B)
在临床试验阶段方面,320项CAR-T临床研究正在进行中,其中大多数(约70%)仍处于PhaseI、PhaseI/II(图1C、D)。
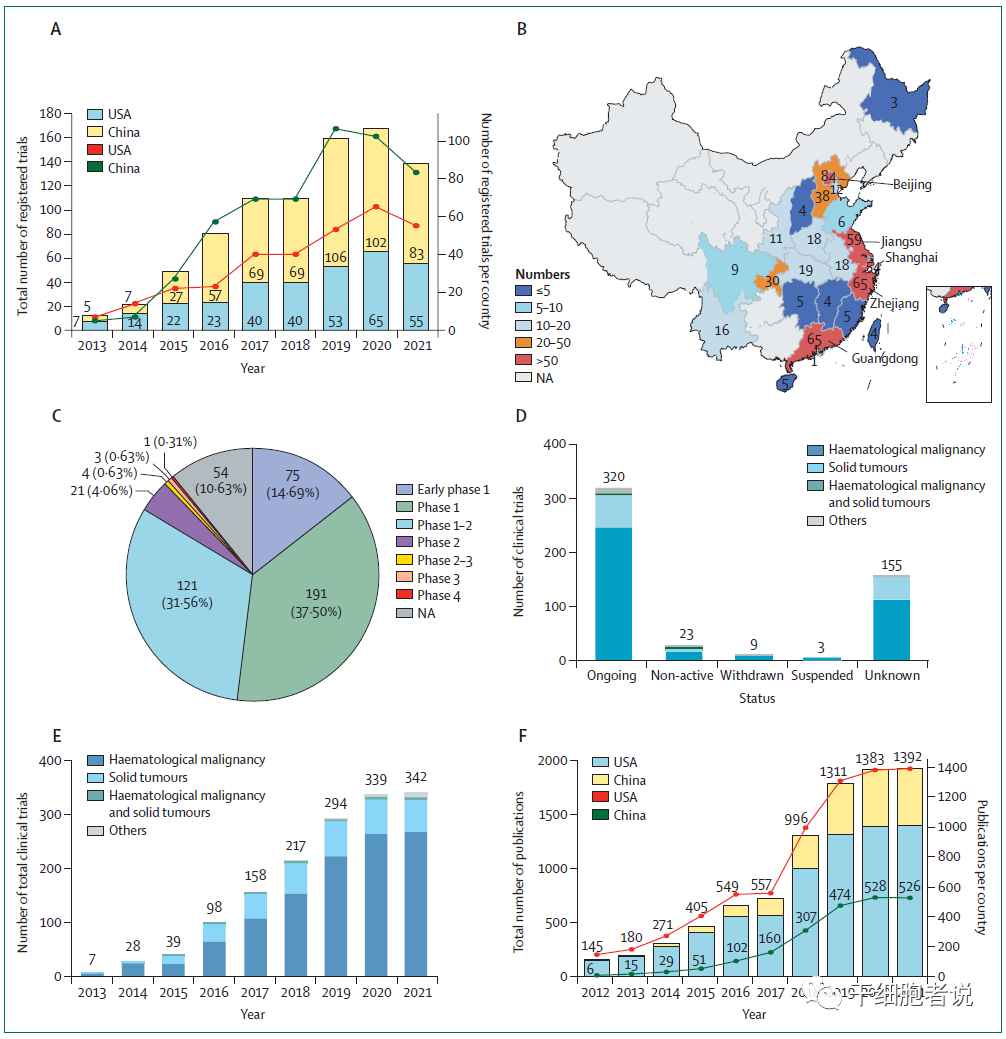
图1.中国CAR-T细胞疗法临床试验情况,以及中美对比
在适应症方面,在2021年正在进行的342项临床试验中,血液肿瘤占绝大多数,尤其是B细胞恶性肿瘤。有119项(23%)用于实体瘤,其中最常见实体瘤试验包括肝癌、胰腺癌和脑癌。
值得注意的是,已经有部分企业在做肿瘤之外的适应症,并且比例有所增加(图D和图E),且疾病涵盖范围广泛,包括自身免疫性疾病、传染病和POEMS综合征。具体来说,针对自身免疫性疾病,适应症包括系统性红斑狼疮、硬皮病、肾炎、干燥综合征、视神经脊髓炎谱系障碍。针对传染病,则包括艾滋病、慢性活动性EB病毒感染和新冠肺炎。
▉ 中国新药临床试验申请(IND)概况
中国CAR-T细胞疗法的IND数量不断增加,已有32家公司的73个CAR-T细胞产品提交IND申请,36个获得默示许可进入临床试验,其中急性淋巴细胞白血病和非霍奇金淋巴瘤是最常见适应症之一(表1.)。
虽然国内开展临床研究很多,但在中国上市并获得商业化的产品只有两款,这也反映出研究与产出的不平衡。

表1.中国CAR-T细胞疗法获批IND情况(靶点和适应症)
-02-中国CAR-T快速崛起的关键驱动因素
积极的政策和法规刺激(国内法律法规促进细胞疗法发展,加快细胞新药开发的步伐)、充足的资金支持(从2018年到2021年,累计融资23.7亿美元,复合年增长率45%)、庞大的患者群体和快速增长的临床试验系统(人口庞大、临床试验认知和参与度提高、临床试验和研究者增长)。
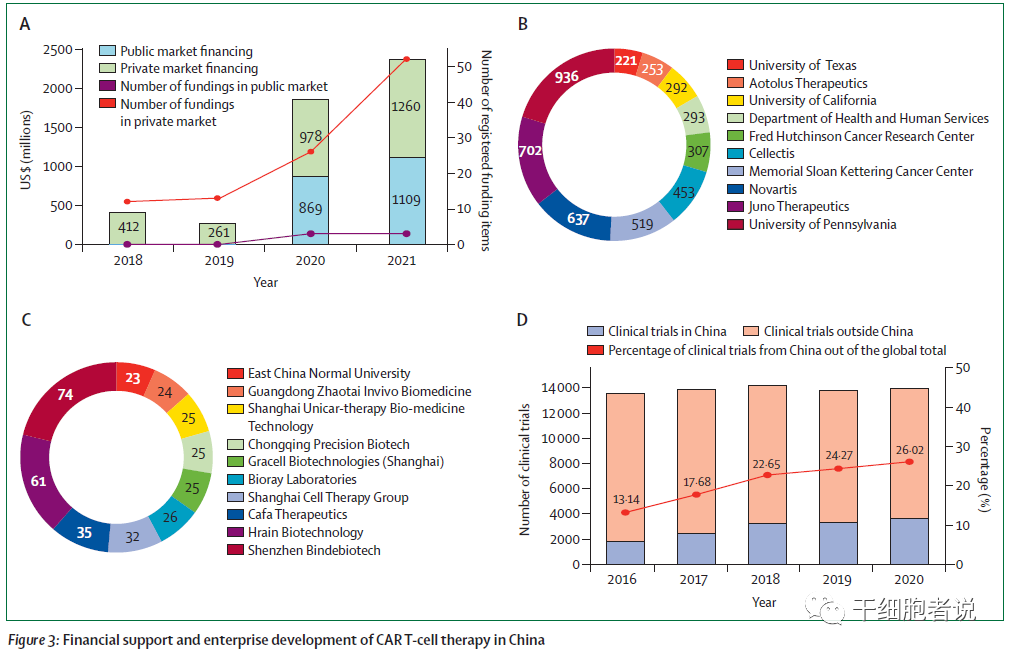
图2.中国CAR-T细胞疗法的资金支持和企业发展
-03-中国CAR-T疗法十年成就
▉ 靶向创新
我国学者不仅首次利用CD5和CD7靶点的CAR-T细胞治疗T细胞恶性肿瘤,更致力于探索多靶点CAR-T细胞治疗从而减少复发率,例如CD19/CD22双靶点CAR-T细胞治疗ALL和B-NHL、BCMA/CD38双靶点CAR-T细胞治疗MM、CLL1/CD33双靶点CAR-T细胞治疗AML等。
在实体肿瘤领域,我国学者首次引入GPC3靶点治疗肝细胞肝癌、Claudin18.2靶点治疗胃癌、B7H3靶点治疗间变性脑膜瘤、EphA2靶点治疗复发性胶质母细胞瘤。
非肿瘤疾病领域,CD19/BCMA双靶点治疗系统性红斑狼疮(SLE)、HIV-1 gp120靶点治疗艾滋病的CAR-T细胞临床试验也正在进行中。
▉ 功能增强
提高CAR-T细胞疗效的方法之一是加强其功能。中国科学家通过化CAR结构、阻断免疫检查点受体(PD-1、Tim-3和 Lag-3)、通过其他生化修饰增加CAR-T 细胞抗肿瘤特性、药物联合CAR-T(地西他滨、索拉非尼、舒尼替尼、桥接半相合造血干细胞移植)、优化离体培养、鸡尾酒CAR-T细胞治疗(CD19联合CD22、BCMA联合CD19)等多种手段,不断增强CAR-T细胞功能,并抵抗CAR-T细胞耗竭使其持续发挥抗肿瘤作用。
▉ 精准调控
我国学者在CAR-T细胞中引入“开/关”概念,精确调节其生物学功能,及时避免细胞因子释放综合征(CRS)、神经毒性综合症(ICANS)、移植物抗宿主病(GVHD)等毒副反应的发生。严重副作用仍是CAR-T细胞疗法临床广泛应用的主要障碍,国内对CAR-T细胞精准调控的研究报道较少,因此精准调控设计是中国下一代 CAR-T细胞设计最重要的方向之一。
▉ 通用型CAR-T细胞研发
通用型CAR-T(UCAR-T)细胞具有健康供者来源、制备成功率高、适用性范围广等特点,我国学者研发的通用型CAR-T细胞在治疗B-ALL和T-ALL中疗效显著,且CRS、ICANS、GVHD等毒副反应低。但是,仍存在一些局限性,其中GVHD是阻碍临床应用的主要挑战之一,因为现有技术仍无法完全敲除T细胞受体,且基因编辑会增加基因突变、克隆扩增和潜在的靶向、非肿瘤效应的风险。
▉ 建立新型制备平台
传统CAR-T细胞,制备主要依赖慢病毒体系,随机整合的CAR插入位点具有一定的生产工艺风险。中国研究团队采用非病毒体系、定点CAR插入技术制备的CAR-T细胞治疗B-NHL,取得目前最好的疗效。
▉ 干细胞定向分化技术
诱导多能干细胞 (iPSC) 或胚胎干细胞(ESC)具有很强的体外扩增能力,且可进行基因编辑。因此,干细胞诱导分化的免疫细胞是未来细胞治疗合理有效的策略。我国学者探索获得不同来源CAR细胞(如NK细胞、巨噬细胞等)的方式,以实现更强的肿瘤细胞免疫治疗。 图3.CAR-T细胞疗法在中国的发展
图3.CAR-T细胞疗法在中国的发展
-04-未来展望
中国正在积极推进细胞治疗研究从实验室走向临床。CAR-T细胞疗法成为一种富有前景的细胞免疫疗法,有可能使广大癌症患者受益,越来越多的CAR-T细胞产品进入治疗开发的试验性新药阶段。
然而,CAR-T细胞疗法成功之路并非坦途,靶点优化、精准调控、功能增强、合成生物学和通用型CAR-T细胞治疗设计方面仍存在挑战。此外,实体瘤会阻碍CAR-T细胞治疗的广泛应用,而不良反应(包括CRS、ICANS和GVHD)的机制和复发风险也需要进一步探索。通过基因编辑和合成生物学等技术的精准调控,中国正在开发高效的通用型CAR-T细胞治疗和iPSC衍生的细胞免疫疗法方面取得进展。中国CAR-T细胞治疗后桥接同种异体HSCT的新策略,有望获得更好的临床疗效和安全性。
总的来说,CAR-T细胞疗法的创新,有望提高我国细胞免疫治疗的临床应用。未来,以干细胞、合成生物学和基因编辑等技术为基础的下一代CAR-T细胞治疗,将在中国迅速崛起,且未来光明。


