最新进展 | 厄达替尼治疗FGFR改变的晚期实体瘤患者2期临床研究
时间:2023-08-17 17:50:42 热度:37.1℃ 作者:网络
【编译者按】RAGNAR试验第一次在具有不同组织学来源、具有FGFR1-3改变的肿瘤中研究厄达替尼的抗肿瘤活性。研究结果表明,在多种肿瘤组织学、具有FGFR改变的晚期实体瘤患者中,厄达替尼具有稳健的客观反应率、有临床意义的反应持续时间和临床获益。此前对FGFR抑制剂的II期或III期研究仅限于尿路上皮癌和胆管癌,RAGNAR的研究结果验证了特定的FGFR改变是多种组织学实体瘤的一个治疗靶点,此结果可能有助于为今后设计FGFR抑制剂的研究提供参考。
本文所报道队列纳入了30例高级别胶质瘤,其对厄达替尼的客观反应率为10%、疾病控制率为57%,mPFS为3.9月,mOS为6.3月;纳入了7例低级别胶质瘤,其对厄达替尼的客观反应率为29%、疾病控制率为71%,目前未取得mPFS和mOS。此研究结果对于带有FGFR改变的胶质瘤有一定的临床意义。

Introduction
成纤维细胞生长因子受体(FGFR)家族蛋白在正常细胞增殖、迁移、分化和存活中发挥着重要作用,FGFR基因改变(包括激活突变或融合),可导致下游细胞信号的构成性激活,从而导致肿瘤发生。厄达替尼是一种口服、选择性的和强效的FGFR 1-4 酪氨酸激酶抑制剂,已被批准用于治疗携带敏感的FGFR2或FGFR3改变的晚期或已转移的尿路上皮癌患者。
在针对尿路上皮癌患者应用厄达替尼的II期BLC2001研究中,40/101(40% [95% CI 31-50])名患者产生客观反应,疾病控制率(即完全应答、部分应答和病情稳定的患者)为81/101(80%)。在针对有FGFR改变的亚洲胆管癌患者进行的多中心、单臂、2a期LUC2001研究中,9/22(41%)名患者对厄达替尼有客观反应,疾病控制率为18/22(82%)。RAGNAR研究单独报告的有FGFR改变的胆管癌患者的探索性队列中,21/35(60%)名患者对厄达替尼有客观反应有客观反应,疾病控制率为35/35(100%)。
针对FGFR基因改变的不同组织来源的肿瘤的靶向疗法研究还很少。在FIGHT-101研究中,128例伴有或不伴有FGFR改变的晚期恶性肿瘤患者中,12例(其中5例为胆管癌)(9%)患者接受FGFR 1-3抑制剂 pemigatinib 治疗后出现部分反应。
晚期、不可切除或已转移的实体瘤患者预后较差,几乎都无法治愈。对于已经用尽标准疗法的晚期实体瘤患者来说,临床试验之外的选择寥寥无几。这些患者往往肿瘤进展迅速,生存期短。RAGNAR试验旨在评估厄达替尼在带有FGFR改变的晚期实体瘤患者中的抗肿瘤活性和安全性。在本文中,我们将报告组织学多来源队列的主要分析结果。
Methods
单臂、2期的RAGNAR 研究在亚洲、欧洲和美国等15个国家的156个研究中心进行。该研究根据肿瘤组织学和患者年龄分为四个队列,本文报告的结果是该研究的主要队列的结果,该队列纳入多组织学来源。符合条件的患者年龄在12岁或以上,组织学表现为不可切除、晚期或已转移的实体瘤恶性肿瘤(尿路上皮癌除外);带有FGFR 1-4基因突变或融合且具有完整的激酶结构域;;在接受至少一种系统治疗后疾病进展,且没有其他标准疗法可供选择;剔除曾接受过FGFR抑制剂治疗的患者。
参试者每天口服一次厄达替尼,周期为21天,直到疾病进展、出现不可耐受的毒性反应等为止。允许在处理毒性反应时中断或减少剂量。主要终点是根据 RECIST v1.1(针对非中枢神经系统肿瘤)或 RANO(针对中枢神经系统肿瘤)评估的客观反应率ORR。次要终点包括客观反应率、反应持续时间、疾病控制率、临床获益率、无进展生存期PFS、总生存期OS、安全性等。
Results
临床截止日期2022年8月15日为止,此队列中有217名患者接受了厄达菲替尼治疗,其中144例(66%)带有FGFR融合,75例(35%)带有FGFR突变,涉及FGFR 1-3,没有FGFR4 基因改变的患者入选。217 名患者中有 97 名(45%)女性,120 名(55%)男性。不同肿瘤组织学的患者人数及其基线特征见表1。
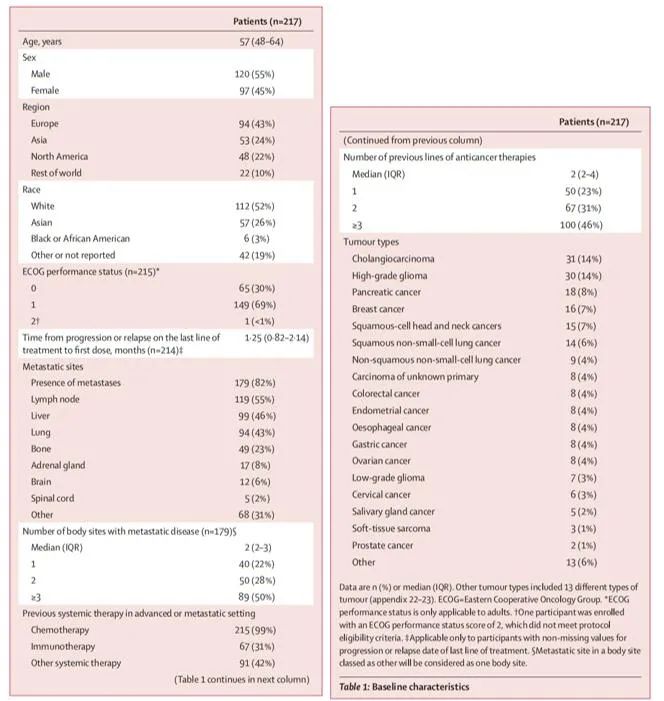
表1. 患者基线特征
中位随访时间为 17.9 个月(IQR 13.6-23.9)。中位治疗时间为 4.3 个月(IQR 2.1-9.2)。最常见的治疗中止原因是疾病进展(159/217 [73%])和不良反应(22/217 [10%])。所有 217 例接受治疗的患者之前至少接受过一种系统治疗,中位数为两种系统治疗(IQR 2-4);100 例(46%)患者之前接受过三种或三种以上的治疗(表1),只有22例(10%)患者在入组前接受的最后一种疗法中出现了应答(部分应答)。
在 217 例患者中,有 159 例(73%)患者的肿瘤负荷较基线有所减轻(图 1),有 64 名(30%,95% CI 24-36)患者出现了客观反应(图 2)。该研究拒绝了客观反应率为 15% 的零假设,达到了主要终点。在 64 例应答患者中,有 6 例(3%)完全应答,58 例(27%)部分应答(图 3)。在16种肿瘤类型中观察到了对厄达替尼的应答(图2)。
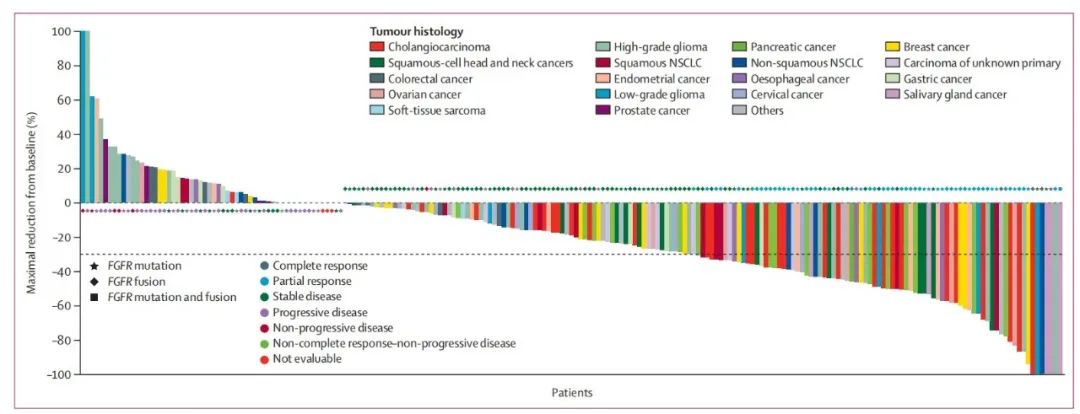
图1. 目标病灶与基线相比的最大减少百分比
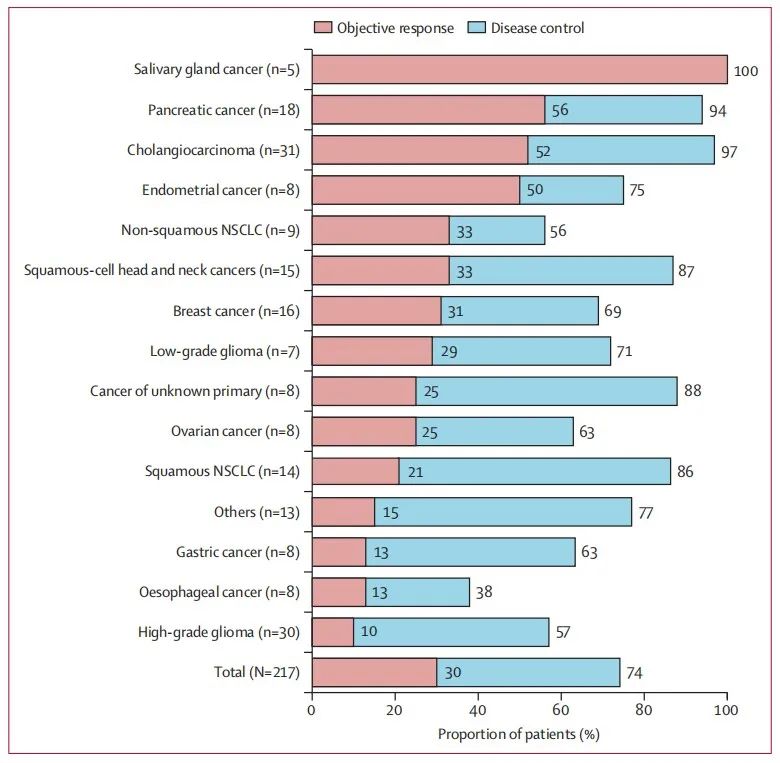
图2. 多种肿瘤类型的应答
(其他类型包括十二指肠癌和甲状腺癌)
中位应答持续时间为6.9个月(95% CI 4.4-7.1)。在有完全或部分应答的患者中,从开始接受厄达替尼治疗到获得应答的中位时间为1.4个月(IQR 1.4-2.7)。57名患者在疾病进展后继续治疗至少4周(中位数41.5天[IQR 18-83])。在217例患者中,疾病控制率为160/217,74%(95% CI 67-80),临床获益率为99/217,46%(95% CI 39-53)。中位PFS为4.2月(95% CI 4.1-5.5),中位OS为10.7月(8.7-12.1)。在不同FGFR 1-3突变和融合的患者中都观察到抗肿瘤活性。
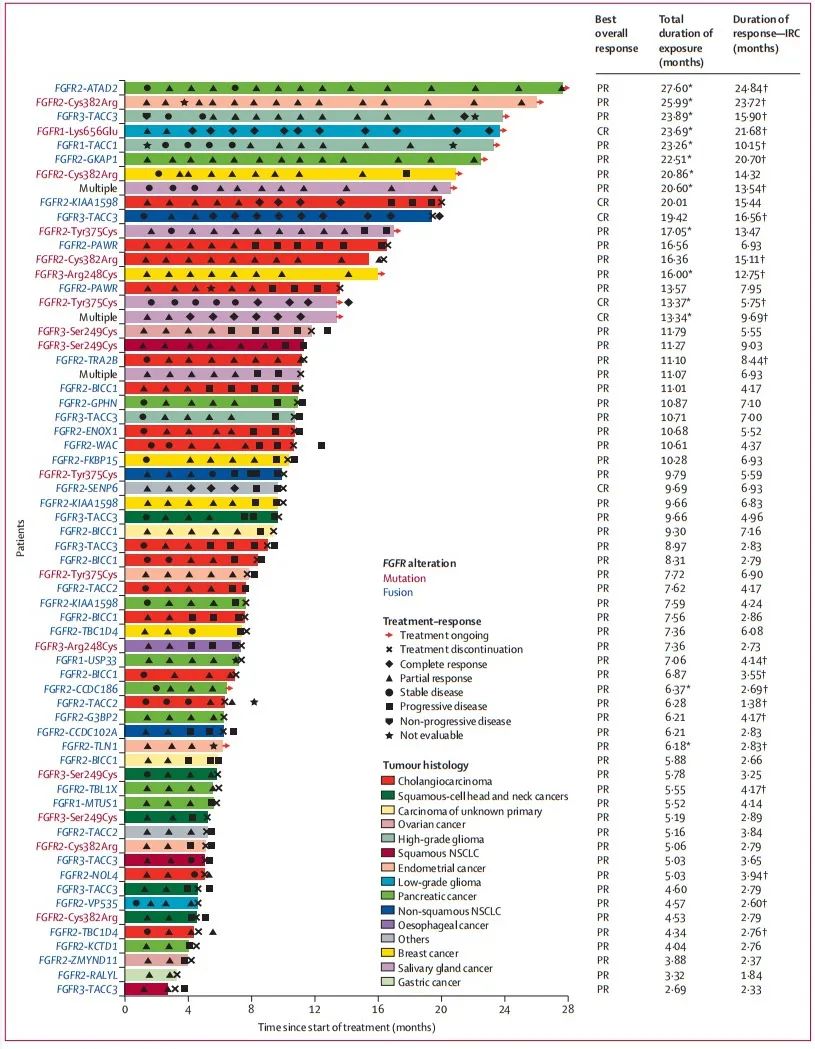
图3. 按FGFR改变划分的对厄达菲替尼的反应和持续时间
217 例患者中有 216 例(100%)至少出现过一次治疗突发不良事件,152例(70%)患者发生了任何原因导致的3-5级治疗突发不良事件(表2)。217 例患者中,分别有 136 例(63%)、162 例(75%)和 22 例(10%)发生了导致减量、中断剂量或中止治疗的治疗突发不良事件,有100例(46%)发生了与厄达菲替尼相关的3级及以上治疗突发不良事件。
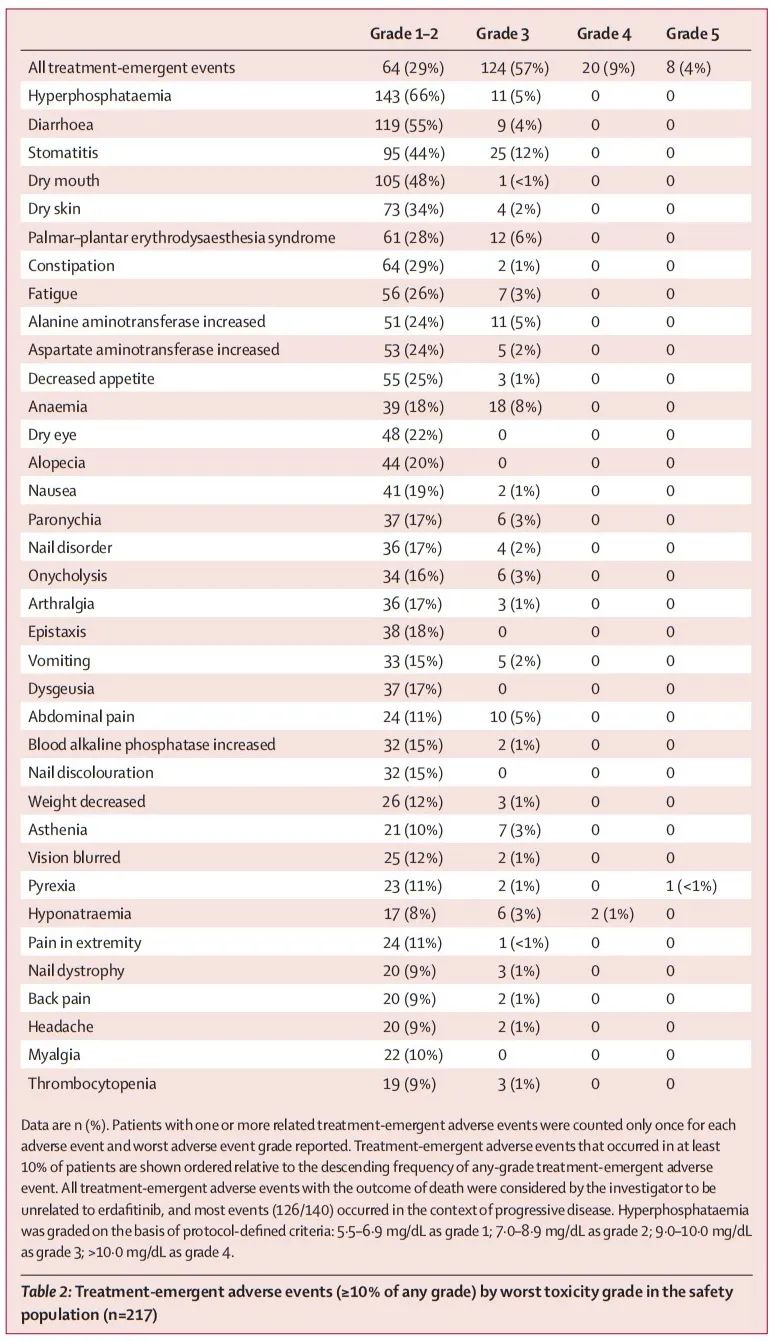
表2. 治疗突发不良事件
Discussion
RAGNAR的初步分析数据证实,厄达替尼对不同组织学来源的FGFR改变的患者具有抗肿瘤活性。在没有其他有效治疗方法的晚期实体瘤患者中,16种不同肿瘤组织学肿瘤的客观反应率为30%,有临床意义的反应持续时间为6.9个月。RAGNAR 的一个主要优势是,这项研究是迄今为止报告的首例多组织学来源肿瘤的FGFR靶向疗法的 2 期试验,共招募了32种不同肿瘤组织学类型的患者。研究设计的一个重要因素是按肿瘤类型限制样本量,以防止某组织学类型占主导,从而提高了罕见肿瘤类型的代表性。
在 RAGNAR 研究中,治疗方案有限的晚期实体瘤患者获得了临床获益,如胰腺癌癌种的客观反应率达到了 56%。虽然有关FGFR抑制剂穿越血脑屏障能力的数据很少,但在中枢神经系统肿瘤中也观察到了不错的活性,低级别胶质瘤的客观反应率为 29%,高级别胶质瘤的客观反应率为 10%。值得注意的是,46%的患者曾接受过三种或三种以上的系统治疗,根据研究者的报告,只有10%的患者在入组前的最后一种治疗中获得了应答。鉴于其他FGFR抑制剂在类似患者群体中的疗效明显较低,厄达替尼在各种组织学和FGFR改变的患者中观察到的活性值得注意。
次要终点结果显示,疾病控制率为74%,中位PFS为4.2个月,中位OS为10.7个月。这些研究结果对于RAGNAR研究中观察到的肿瘤类型的最后一线治疗人群具有重要的临床意义。例如,胶质母细胞瘤采用已获批准的二线疗法的中位生存期为 9月,而头颈部复发性或转移性鳞状细胞癌采用二线抗 PD-L1 疗法的中位生存期为 7-8月。
在某些肿瘤类型(如结直肠癌)中观察到的反应很少或没有反应,但由于样本量较小很难解释这些发现。既往多次治疗失败的转移性实体瘤预计会存在多种基因改变,这可能会限制对FGFR抑制剂治疗的反应性。值得注意的是,RAGNAR 中有 70% 的患者没有获得应答,这突出表明有必要更好地了解存在FGFR改变的实体瘤的生物学特性、FGFR改变的类型、以及并发基因组改变在导致FGFR靶向疗法耐药方面的作用。例如,需要进一步分析了解厄达替尼在FGFR激酶域改变的肿瘤中的活性。
观察到的毒性(包括中心性浆液性视网膜病变)与厄达替尼和其他FGFR抑制剂的已知安全性特征一致。大多数患者都出现了剂量中断和剂量减少的情况,其中10%的患者因不良事件而停药,这可能会影响药物的活性。这些挑战凸显了进一步研究病理机制的必要性,这可能会开发出耐受性更好的新型FGFR靶向疗法。
单臂研究设计限制了解读RAGNAR研究结果的能力。然而,在这一患者群体中,随机试验设计是不可行的,因为FGFR改变的实体瘤非常罕见,而且在没有可用标准疗法的情况下不存在等效性。此外,鉴于预后和自然病史的多变性,在一项随机试验中结合多种肿瘤类型和组织学可能在方法学上并不合适。因此,在这种情况下,真实世界的数据可能会提供更多的信息,通过探索FGFR改变的预后意义和潜在的真实结果,为研究结果提供背景信息。
总之,RAGNAR 主要分析的活性和安全性结果证实,在多组织学来源的肿瘤中,厄达替尼可为有易感 FGFR 改变并已用尽其他治疗方案的晚期实体瘤患者带来有意义的临床获益。


