【衡道丨笔记】甲状腺穿刺细胞病理学检查及分子检测实践分享
时间:2023-09-01 23:14:45 热度:37.1℃ 作者:网络
内容摘要
甲状腺癌流行病学
-
2000-2016年甲状腺癌发病率增长迅速(女性APC 17.7%,在所有癌症类型中增幅最大)。
-
甲状腺癌发病率的高速增长,很大程度上与高分辨率超声的大量应用有关。
-
死亡率相对稳定,并处于较低水平。但在女性中呈现上升趋势(APC 1.6%)。
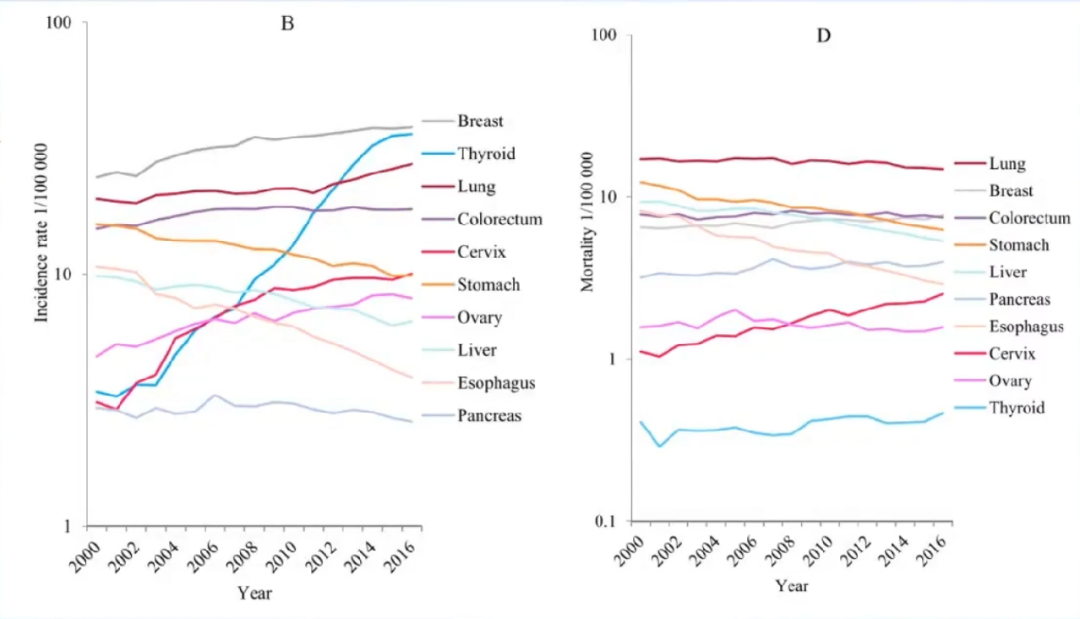
2016年发病率:女性15.81(男5.11,总10.37)死亡率:女性0.45(男0.29,总0.37)
-
我国甲状腺癌患者5年生存率与美国仍有差距(84.3%:98%)。
-
临床工作重点:正确甄别甲状腺癌,为甲状腺疾病的个体化精准治疗提供依据;规范化治疗;平衡好治疗的风险和获益;术后全程管理。
超声引导下甲状腺FNA细胞学(UG-FNA)
术前评估甲状腺结节良恶性时,超声引导下FNA是敏感性和特异性最高的方法,列入《2021版CSCO分化型甲状腺癌诊疗指南》Ⅰ级推荐。
应用范围:首诊可疑恶性的甲状腺结节;考虑复发、转移性甲状腺癌的术前明确诊断。
诊断价值:评估甲状腺结节的性质,提高甲状腺手术恶性肿瘤比例,避免不必要的手术。
-
约有10-30%的FNA显示不确定诊断(Ⅲ、Ⅳ),其中70-80%术后证实为良性病变。
-
由于近年国际国内相关实践指南推荐有恶性征象者行FNA,良性者可不行FNA,细胞学良性诊断比例下降,不确定诊断比例上升。
-
分子检测可降低甲状腺结节诊断不确定性。
-
检测结果阴性的甲状腺结节仍需积极监测(检测方法的局限及假阴性)
BRAF V600E突变与PTC
甲状腺癌中乳头状癌(PTC)最多见(超过90%),BRAF V600E在PTC中突变率欧美30-60%,亚洲70-90%。2022年北京协和医院发表一项多中心研究,395名PTC患者,310例存在BRAF突变(78.5%),均为BRAF V600E。与TCGA数据库的突变率存在显著差异。
-
BRAF V600E不存在于甲状腺良性及低分险肿瘤。因此FNA细胞样本伴BRAF V600E突变可以高度怀疑恶性结节(阳性预测值达99.8%);
-
BRAF V600E提高FNA诊断效能;
-
BRAF基因检测联合细胞学检查,能显著提高术前诊断的敏感性、NPV和准确性。
-
BRAF V600E检测方法及样本获取:

我院开展甲状腺UG-FNA+BRAF情况
制片:拨散法,注射针针体将载玻片上的穿刺物轻柔拨散开,尽可能保持涂片厚度均匀,立刻放入95%酒精固定;
染色:HE染色;
穿刺物洗脱液:打出针腔内标本后,针腔壁上仍有穿刺物残留的细胞液成分。涂片后针均在盛有约300μL PK Solution的EP管中涮洗;
DNA提取:细胞室每天3次将洗脱液送至分子室,保存在4℃,不超过48h;
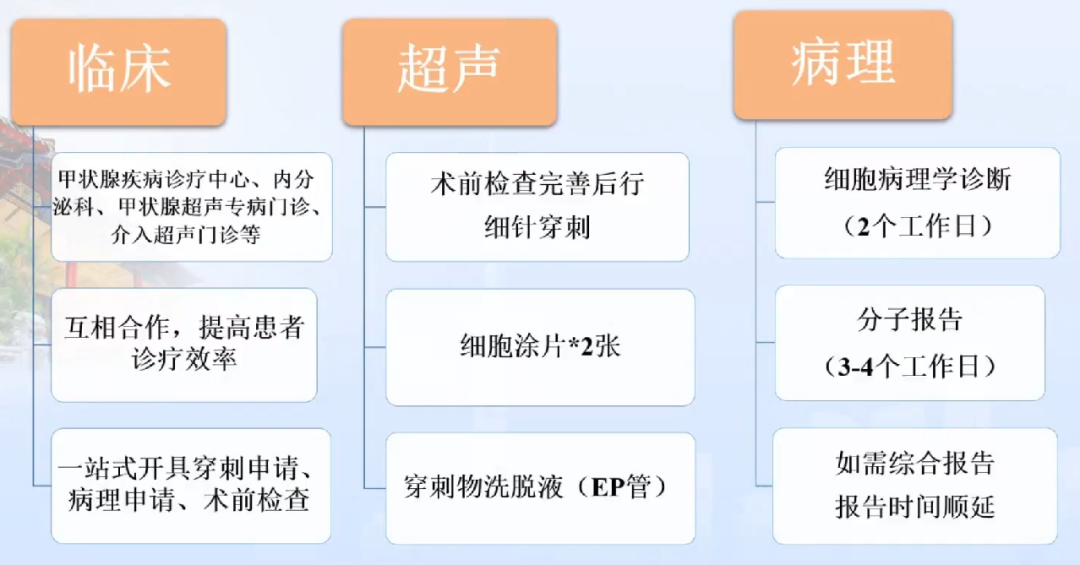
报告模式:细胞学报告与分子报告保持相对独立
1.可明确分类病变,先出具细胞病理学报告(2个工作日)。报告内容包括:病变描述、TBS诊断分类,必要的注释,备注各级TBSRTC恶性风险度;
2.部分Ⅰ、Ⅳ级病变(有一定的细胞异型基础),综合BRAF结果出诊断结论。
病例分享
病例一
-
男,60岁;
-
超声:甲状腺左叶下极见7*6mm低回声不均质团块,形态欠规则,边界欠清,其内见点状强回声,MT可能。
-
细胞学诊断:(甲状腺左叶结节)涂片见少量非典型腺上皮细胞,倾向意义不明确的非典型病变(AUS)。(TBSRTCⅢ)
-
BRAF V600E:存在点突变
-
临床:

-
组织病理学:(甲状腺左叶+峡部)乳头状癌
病例二:
-
男,67岁;
-
超声检查:甲状腺右叶中部背侧见5*4mm低回声团块,纵横比>1,向包膜外突出,其内见点状强回声,MT不除外(TI-RADS 4a)
-
细胞学诊断:(甲状腺右叶结节)涂片见数堆腺上皮细胞,部分细胞胞核稍有异型,倾向肿瘤性病变,请做进一步检测除外恶性。(TBSRTC Ⅳ)
-
BRAFV 600E:存在点突变
-
临床:
-
组织病理学:(甲状腺右叶+峡部)乳头状癌。
启示:
1、当样本中细胞量很少,但具有异型性时,很可能细胞学诊断为TBSRTC Ⅲ(AUS)。
2、当样本中细胞以微滤泡形式为主,部分细胞核出现异型性(核增大、形态不规则、局灶性染色质透明等),可能细胞学诊断为TBSRTC Ⅳ。
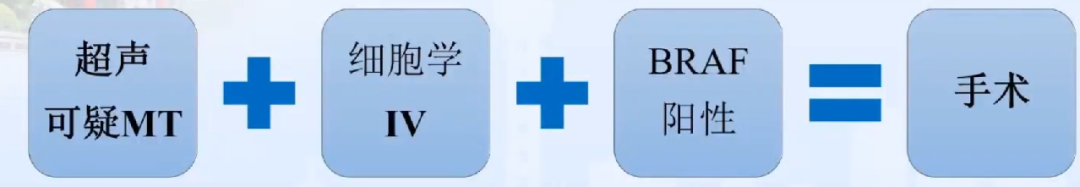
3、病理解读要独立于分子检测,部分细胞有异型+BRAF点突变,支持提级处理(升级为TBSRTCⅤ,可疑恶性)。
4、ARMS法敏感性高,对于细胞量稀少导致的TBSRTC Ⅲ,辅助诊断价值很高。
病例三:
-
女,52岁;
-
超声检查:甲状腺右叶中下部背侧见4.1*7.1mm低回声团块,边界欠清,纵向生长,内见点状强回声,MT可能。
-
细胞学诊断:(甲状腺右叶结节)涂片见数堆腺上皮细胞,部分细胞拥挤,细胞核大、可见核沟,倾向肿瘤性病变,请做进一步检测除外恶性。(TBSRTCⅣ)
-
BRAF V600E:未检测到突变
-
临床:

-
组织病理学:(甲状腺右叶+峡部)乳头状癌。
启示:
当样本中细胞以微滤泡形式为主,部分细胞核出现异型性(核增大、形态不规则、局灶性染色质透明等),细胞学可能诊断为TBSRTCⅣ,即使BRAF阴性,也应该注明细胞核的形态学改变,描述性语言有可能会影响临床处理。
思考:
单一BRAF基因检测,无法提供足够高的阴性预测值,希望开展多基因检测以提高分子检测灵敏度。但成功率、可及性、时效性方面如何平衡?
病例四:
-
男,48岁;
-
超声检查:甲状腺右叶中上部见25*19mm低回声团块,边界不清,非水平位,周边分布数枚斑点状强回声,TI-RADS 4c。右颈根部颈动脉后淋巴结回声异常——考虑受侵不除外。
-
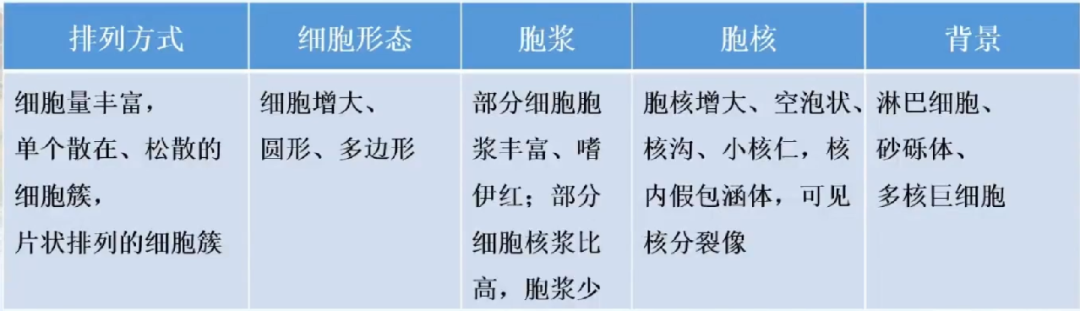
细胞学特征:
-
诊断?
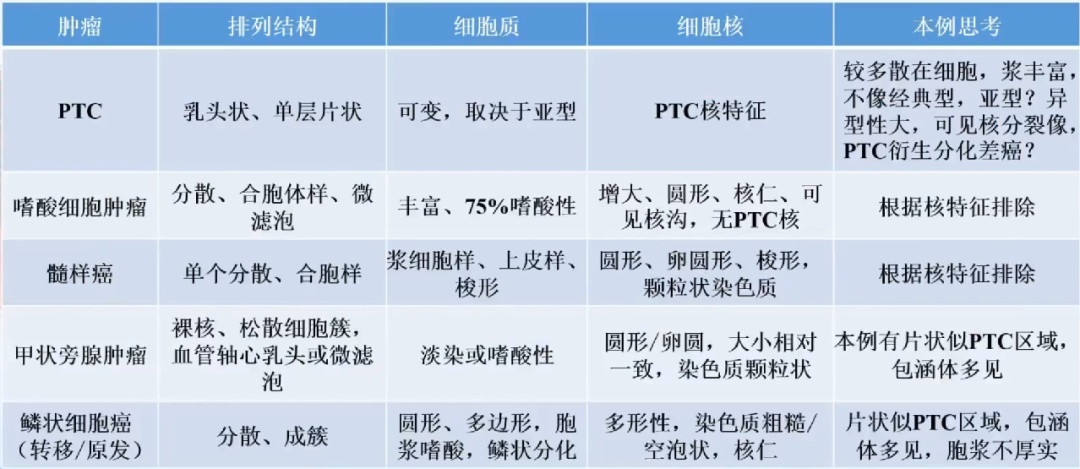
-
细胞学诊断:(甲状腺右叶)见恶性肿瘤细胞,倾向低分化癌,建议术中冰冻(TBSRTC Ⅵ)
-
BRAF V600E:存在点突变
-
病理诊断:肿物全部取材,可见乳头状癌成分,部分肿瘤细胞呈实性巢状生长,细胞胞浆丰富嗜伊红,细胞核空泡状,部分核仁明显,部分区可见鳞化,小灶可见坏死,核分裂像密集区约2个/10HPF,结合免疫组化结果,考虑乳头状癌(约占70%),部分区分化降低,呈高级别分化型甲状腺癌(约占30%)。
-
免疫组化:TG(部分+)、TTF-1(部分+)、CD56(+)、CK19(+)、Galectin-3(少量弱+)、Ki-67(10%+)、P40(少量+)、P63(少量+)
-
高级别分化型甲状腺癌(DHGTC):2022年WHO第5版甲状腺肿瘤分类中新命名的一种甲状腺侵袭性癌,具有高级别形态学特征(高分裂像活性、肿瘤坏死),中等预后风险。分子特征:BRAF、RAS、TERT等
启示:
BRAF V600E可用于鉴别诊断,排除甲状腺低风险肿瘤、髓样癌、嗜酸细胞癌、甲状旁腺肿瘤等诊断。
总结
1、甲状腺UG-FNA用于术前诊断,有助于决定临床处理方案,加BRAF检测,可降低诊断不确定性,并可用于少见细胞形态肿瘤的鉴别诊断。
2、单一BRAF检测,检测成功率高(所需细胞量少)、可及度高(ARMS 1000元)、时效性高(3-4天出结果),尤其在我国BRAF阳性率高的情况下,适于普遍开展。
3、单一BRAF检测,阴性预测值有限,识别高危PTC患者临床意义有限,难以指导预后分层。条件允许的情况下,应与其他基因变异一同评估。

