Carbohydr Polym 山东大学李霞教授团队发现聚古罗糖醛酸具有保护心脏免受阿霉素所致心脏毒性的作用
时间:2023-09-13 20:00:28 热度:37.1℃ 作者:网络
阿霉素也称多柔比星(doxorubicin, DOX),作为临床一线蒽环类化疗药物之一,其使用因易导致心脏毒性而严重受限。与DOX相关的心脏毒性涉及多种病理机制,其中由心肌细胞焦亡而导致心脏毒性受到越来越多的关注,但其机制尚未完全清楚。因此,探索阿霉素心脏毒性机制并提供新的潜在治疗药物具有重要临床意义。
2023年8月25日,山东大学海洋学院李霞教授团队在多糖领域期刊Carbohydrate Polymers上发表了题为“Polyguluronic acid alleviates doxorubicin-induced cardiotoxicity by suppressing Peli1-NLRP3 inflammasome-mediated pyroptosis”的文章,该文初步探讨了聚古罗糖醛酸(PG)在阿霉素所致心脏毒性中的防治作用及分子机制。

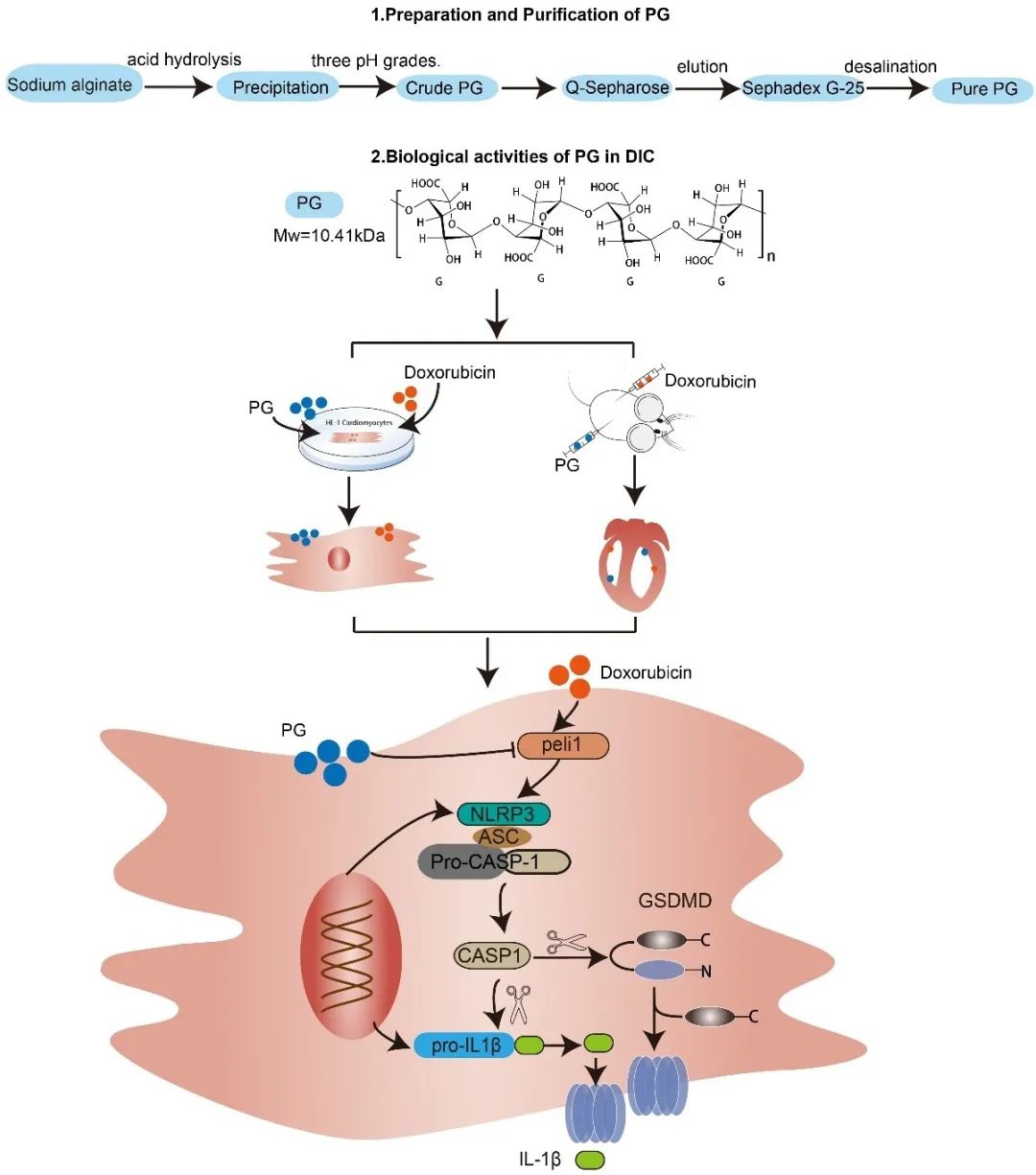
聚古罗糖醛酸(PG)来源于海藻,是由α-1,4- L -古罗糖醛酸组成的海藻酸盐的降解产物,其具有降血脂、抗菌、抗炎、抗氧化、免疫调节等多种优良的生物学活性。该团队通过酸水解的方法制得高纯度聚古罗糖醛酸(PG),并在体外和体内评价了聚古罗糖醛酸对阿霉素诱导的心脏毒性的防治作用。
首先,PG可以减轻DOX诱导的线粒体损伤、提高HL-1心肌细胞的活力并抑制心肌细胞中乳酸脱氢酶(LDH)和IL-1β的释放,改善阿霉素导致的心肌细胞焦亡形态,保护心肌细胞维持正常形态。进一步研究发现,PG可阻断焦亡经典通路NLRP3/ASC/Caspase1/GSDMD轴的激活,抑制DOX诱导的心肌细胞焦亡。
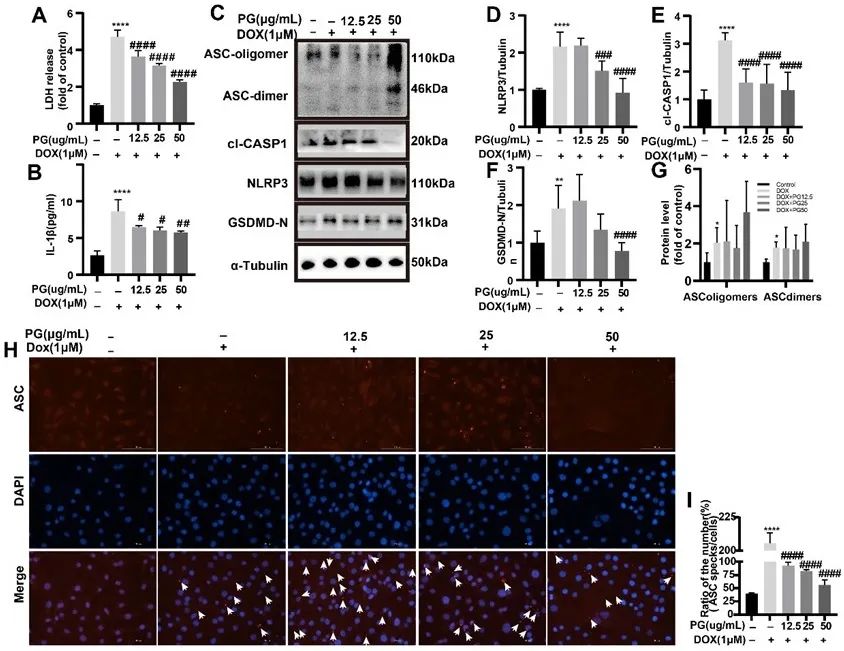
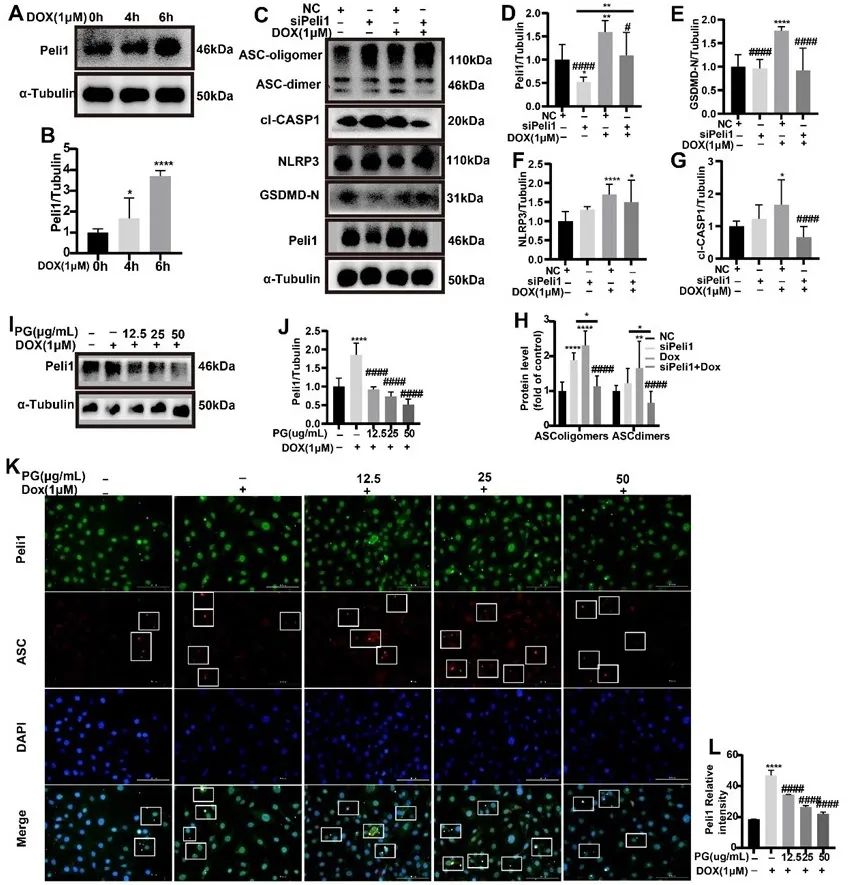
其次,研究发现阿霉素在诱导心肌细胞焦亡的同时引起E3泛素连接酶Peli1的表达上调,而下调Peli1则抑制NLRP3/ASC/Caspase1/GSDMD轴诱导的焦亡。而PG的使用则可抑制DOX诱导的Peli1上调,从而抑制NLRP3炎症小体介导的心肌细胞焦亡。由此推测,PG可能通过抑制E3连接酶Peli1参与的焦亡发挥抗焦亡作用。
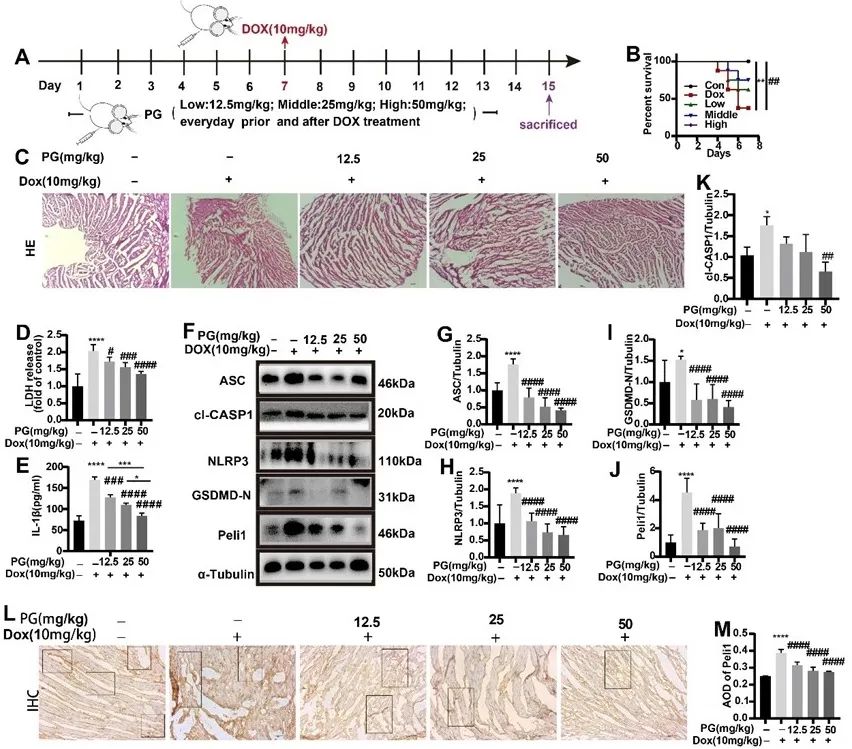
最后,在体内评价了PG对阿霉素诱导心脏毒性的防治作用。研究发现,PG可延长阿霉素作用下小鼠生存期,抑制心肌细胞中乳酸脱氢酶(LDH)和IL-1β的释放,下调E3泛素连接酶Peli1的表达,从而抑制NLRP3、ASC、Caspase1和GSDMD焦亡蛋白的表达,降低心肌组织焦亡水平,保护心肌组织免受阿霉素损伤。
综上所述,在阿霉素所致心脏毒性体内和体外实验中,以酸水解法制备的PG耐受性良好,无明显毒副作用; PG可下调阿霉素诱导的Peli1的表达上调,阻断NLRP3炎性小体介导的心肌细胞焦亡。本研究表明海藻酸多糖聚古罗糖醛酸(PG)具有保护心脏免受阿霉素毒性的作用,是一种潜在的防治阿霉素心脏毒性的海洋多糖药物,具有实际的临床价值和广阔的应用前景。本成果已申报国家发明专利。
山东大学海洋学院生物与医药专业博士生张娥为本论文第一作者,山东大学海洋学院李霞教授和宋淑亮高级研究员为该论文共同通讯作者,山东大学为唯一完成单位。本研究得到国家自然科学基金No. 82073870 和 No.82273992 的支持和资助。
论文链接:
https://doi.org/10.1016/j.carbpol.2023.121334


