Blood Adv:cHL患者ASCT后进展后的生存期与影响因素
时间:2023-10-16 17:30:21 热度:37.1℃ 作者:网络
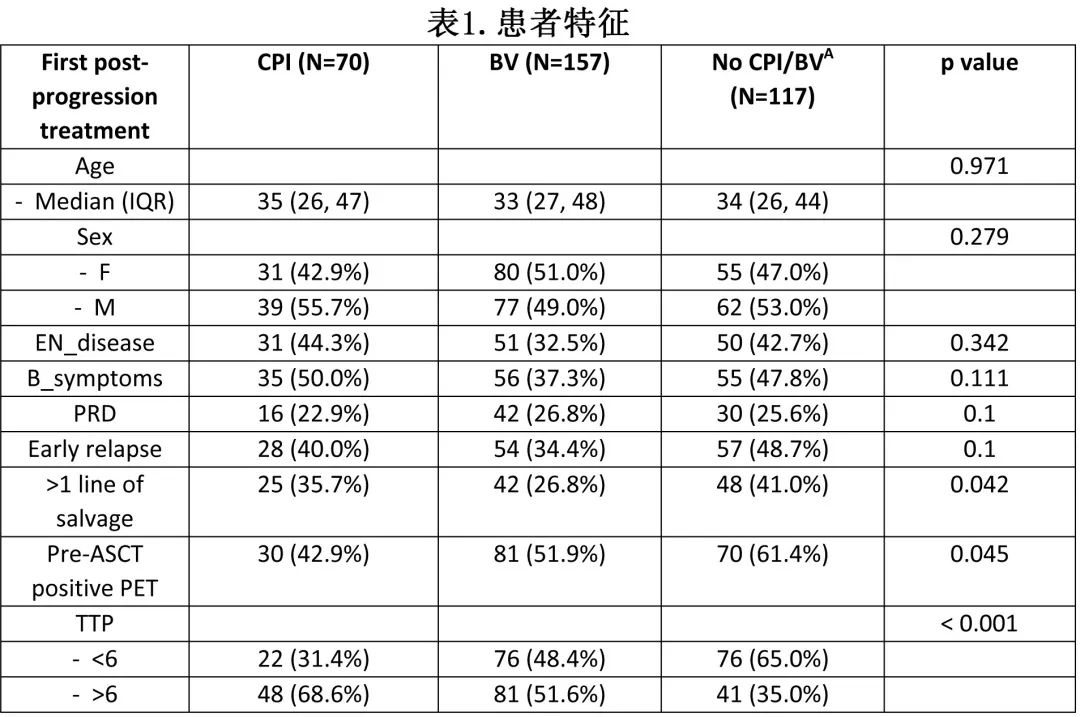
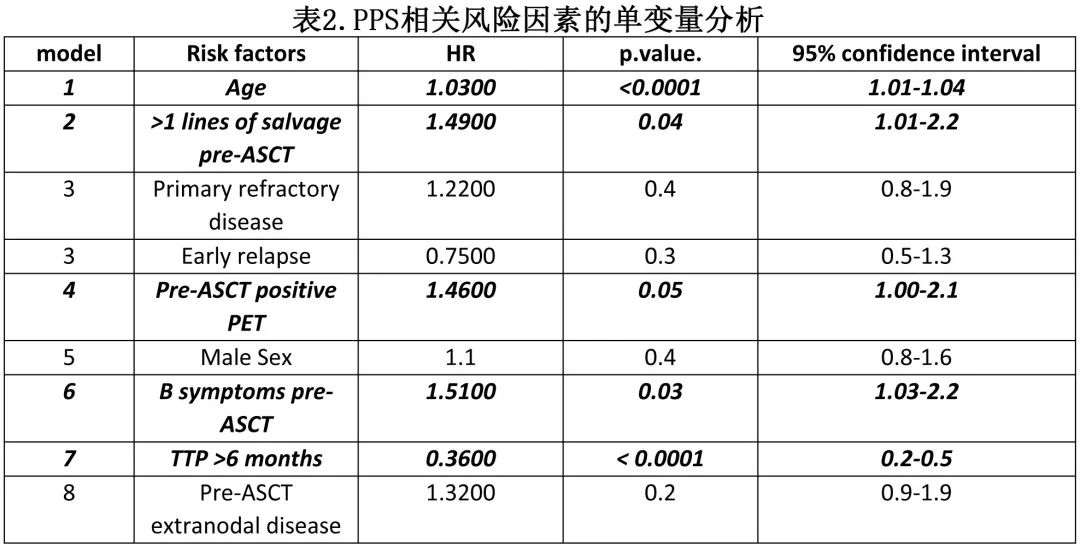
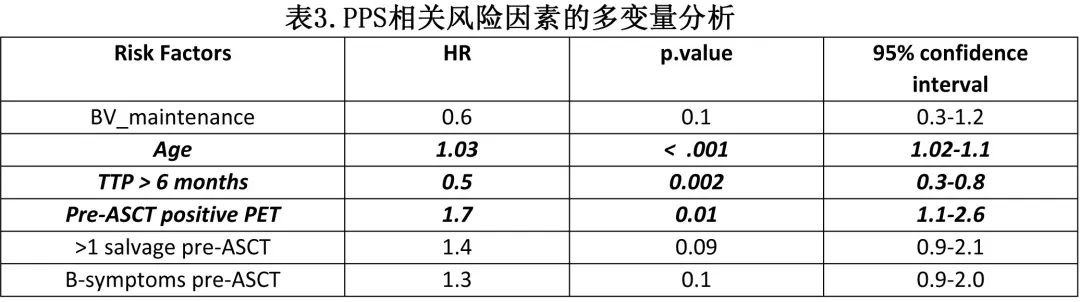
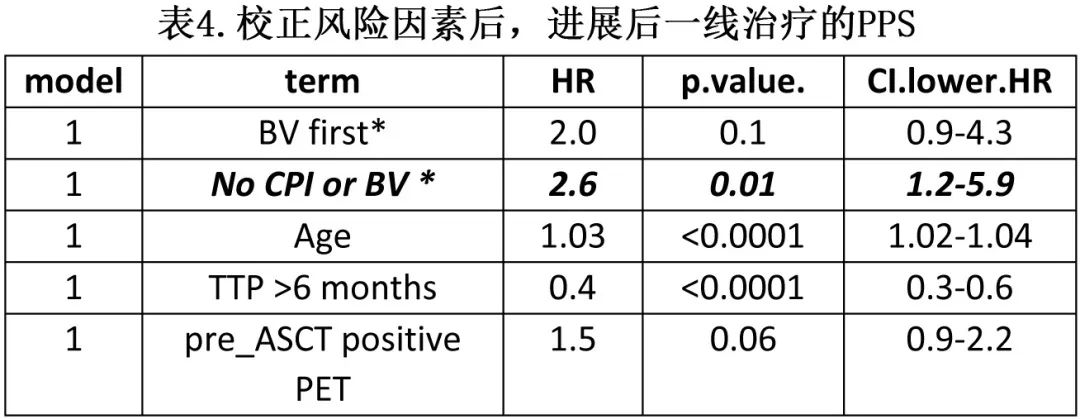
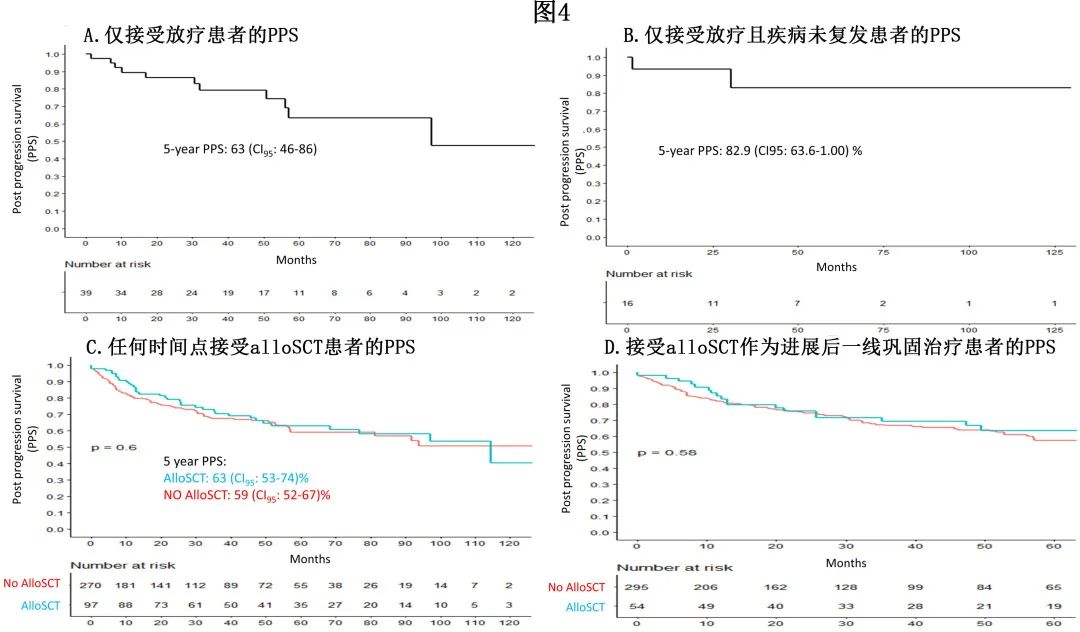
挽救治疗和自体造血干细胞移植(ASCT)是复发难治经典霍奇金淋巴瘤(R/R cHL)患者的标准治疗,ASCT 后复发的患者传统上预后较差,在新药前时代中位生存期仅2-3年。而在一线和复发性难治性患者中添加新药,尤其是维布妥昔单抗 (BV) 和检查点抑制剂 (CPI)显示了令人鼓舞的缓解和生存期。2021年The Lancet Oncology发表的3期KEYNOTE-204研究期中分析显示,在ASCT后复发或不适合ASCT的R/R cHL中,帕博利珠单抗的无进展生存期(PFS)优于BV。也有一下小型回顾性研究评估了ASCT后复发的cHL患者的移植后生存期,但接受新药治疗的患者较少。因此,需要在新药时代进行大型观察性队列研究,以估计 ASCT 后进展性 cHL 的移植后生存期、预后因素和新药排序的影响。《Blood Advances》近日发表文章, 报告了使用多机构观察性队列中ASCT 后复发的367例 cHL患者的结局。 关键点 1、在新药时代,自体干细胞移植后进展的 cHL 患者的总生存期接近9.5年。 2、与未接受新药的患者相比,接受 CPI 作为 ASCT 后进展后首次治疗的患者的死亡率较低。 患者特征 该研究纳入18家中心2011-2020期间所有接受挽救治疗和ASCT且在移植后进展的R/R cHL患者367例(接受挽救治疗和ASCT的R/R cHL患者共1158例)。中位年龄为34岁,192例患者为男性。ASCT 后至疾病进展的中位时间为6个月,336例患者ASCT 前至少有一个改良 ATHERA 风险因素。65例 (19%) 在 ASCT 后 BV 巩固治疗期间或之后复发。90例 (24%) 接受 BV 作为 ASCT 前治疗,其中14例 (4%) 还接受 CPI 作为 ASCT 前治疗。ASCT 后进展的中位治疗线数为2。147例 (40%) 在 ASCT 后进展的任何时间点接受CPI,70例 (20%) 患者接受 CPI 作为 ASCT 后进展的一线治疗;201例 (55%) 在 ASCT 后进展的任何时间点接受 BV 治疗,157例 (43%) 在 ASCT 后进展首次治疗时接受 BV 治疗。117例 (32%) 患者接受单纯放疗(39例)、化疗联合或不联合放疗(59例),其他靶向药物,如依维莫司或panobinostat (10) 或接受alloASCT(9);23例患者无可用的药物名称。表1显示了基于 ASCT 后复发时接受的首次治疗(CPI、BV或无CPI/BV)的三大组患者特征。BV 组在一线治疗后接受移植的患者数量较多,无 CPI/BV 组部分缓解(PET阳性)的患者数量较多,CPI 组至疾病进展时间 (TTP) 超过6个月的患者数量较多。 结局 中位随访48.1个月,中位进展后总生存期(post progression overall survival,PPS)为114.57个月,即9.5年;10年 PPS 为46.2%(图1)。 PPS的相关因素 在单变量分析中,年龄增加与 PPS 恶化相关(图2A);年龄<40岁患者的 PPS 显著高于40-60岁的患者和年龄<60岁的患者(5年PPS 70.1%、49.1%和31.1%,p=0.00017)。ASCT 后至疾病进展时间 (TTP) 为6个月内的患者的生存期显著低于6个月后疾病进展的患者(5年PPS:51.2% vs 68.9%,p<0.0001,图2B)。 接受 ASCT 前 BV 或 CPI 的患者 (N=90) 与 ASCT 后进展时 BV 或 CPI 初治患者的 PPS 无差异(5年PPS 65% vs. 59%,p=0.9)。 除年龄增加 (HR=1.03,p<0.001) 和TTP≤6个月 (HR=1.5,p<0.001) 外,ASCT前高危特征如ASCT前PET阳性 (HR=1.7,p=0.01)、需要>1次挽救治疗 (HR=1.5,p=0.02) 和 B 症状(HR=1.5,p=0.02)和接受移植后 BV 维持 (HR=0.4,p=0.02)也与 PPS 较差相关。而ASCT 前淋巴结外疾病、原发难治性疾病、早期复发 (ER,定义为一线治疗完成后12个月内复发)和性别与 PPS 无关(表2)。 在多变量分析中,年龄增加、TTP≤6个月、ASCT前PET 阳性均与 PPS 较差显著相关(表3) ASCT后进展的治疗 作者评估了移植后进展的 BV 和 CPI 治疗排序如何影响PPS,根据 ASCT 后进展后接受的一线治疗将患者分为三组:CPI组 (N=70)、BV 组 (N=157) 和无 CPI/BV 组 (N=117);23例患者未提供治疗详情,从本分析中排除。在进展后一线接受 CPI 治疗的70例患者中,16例 (23%) 因疾病复发接受了更多线治疗;在进展后一线接受BV 治疗的157例患者中,76例 (48%) 因疾病复发接受进一步治疗;在无 CPI/BV 组的117例患者中,77例 (66%) 因疾病复发接受了进一步治疗。与 BV 组患者 (OR=3.3,p<0.001) 或无 CPI/BV 组患者 (OR=5.1,p<0.001) 相比,CPI组患者因疾病复发接受进一步治疗的可能性显著降低。 在进展后接受BV的157例患者中,54例 (34%) 在疾病复发后的任何时间点接受CPI。在无 CPI/BV 组的117例患者中,24例 (20%) 接受CPI,34例 (29%) 接受 BV 作为后续治疗线。在进展后接受 CPI 的70例患者中,13例 (19%) 接受 BV 作为后续治疗线。 在单变量分析中,接受 CPI 作为 ASCT 后进展后一线治疗的患者的 PPS 显著高于无 CPI/无 BV 组 (HR=3.4,p=0.002) 和 BV 组(HR=2.4,p=0.03,图3A);而接受 BV 的患者和未接受 CPI /BV 作为进展后一线治疗的患者的 PPS 无差异 (HR=1.7,p=0.07)。此外该结果在 ASCT 后6个月内复发的患者亚组中一致(图3B)。 校正年龄、TTP和 ASCT 前 PET 反应后,CPI组患者的 PPS 始终优于无CPI/ BV组 (HR=2.6,p=0.01);而CPI与 BV 组无差异(表4)。 ASCT后进展后的放疗 39例患者在进展时仅接受放疗作为一线治疗,该人群的5年 PPS 为63.3%(图4A)。16例 (41%) 存活且无需任何后续治疗,该人群的5年 PPS 为82.9%(图4B) 异基因造血干细胞移植(AlloSCT) 97例患者在 ASCT 后任何时间点接受 alloSCT 治疗疾病进展,54例接受 alloSCT 作为进展后一线治疗的巩固治疗。在任何时间点接受和未接受 alloSCT 的患者特征无差异。 在任何时间点接受 alloSCT 的97例患者中,19例 (20%) 在中位随访25个月内需要后续治疗线;显著低于未接受 alloSCT 的患者(270例中的102例 (37%),p=0.001)。在 ASCT 后进展的任何时间点接受 alloSCT 的患者与未接受 alloSCT 的患者的 PPS 无差异(图4C)。alloSCT组25例 (39%) 患者死亡,无任何进一步复发。在1线进展后治疗后接受 alloSCT 的54例患者中,49例不需要任何进一步治疗进展。该人群中的2年非复发死亡率(NRM)为30%。 为消除先导时间偏倚,作者比较了接受 alloSCT 作为进展后一线治疗的巩固治疗的患者与未接受 alloSCT作为进展后一线治疗的巩固治疗的患者。接受 alloSCT作为进展后一线治疗的巩固治疗的患者与接受 alloSCT 作为后续治疗或根本未接受 alloSCT 的患者组之间无显著差异(图4D)。 总结 在这项多中心队列研究中,观察到 cHL 患者在现代治疗时代 ASCT 后复发患者仍有接近10年的中位PPS。年龄>40、ASCT后6个月内进展、ASCT前PET 阳性与 PPS 较差相关。与未首先接受 BV 或 CPI 的患者相比,进展后一线接受 CPI治疗的患者的 PPS 更高。接受 alloSCT 与较高的 PPS 无关。 总的来说,在新药时代,ASCT后进展性 cHL 的生存期较长,与既往报告相比更佳。接受 CPI 作为疾病进展首次治疗的患者的 PPS 较高;在该人群中,接受 AlloSCT 与 PPS 无关。 参考文献 Desai SH,et al. Overall survival of cHL patients who progress after autologous stem cell transplant: results in novel agent era.Blood Adv . 2023 Sep 20;bloodadvances.2023011205. doi: 10.1182/bloodadvances.2023011205