【衡道丨文献】肝脏穿刺活检面面观
时间:2023-11-24 11:27:53 热度:37.1℃ 作者:网络
2023年9月,病理学期刊《Surgical pathology Clinics》专门刊出一期介绍肝脏穿刺活检病理的内容,共12篇综述性文献,详尽介绍了肝脏穿刺的适应症,以及肝脏各种疾病的临床、穿刺活检病理改变,包括非肿瘤性疾病和肿瘤性疾病。

甘肃省人民医院病理科陈旭医生将分数期内容,详尽介绍各种疾病的肝脏穿刺病理表现,供相关医师参考。
肝脏疾病的检查思路和肝脏穿刺活检的适用范围
肝病评估常用的实验室及临床检查
临床检查
①病史(药物、病毒接触、酒精摄入、代谢情况、家族遗传、自身免疫性疾病);
②物理检查(肝脾叩诊、皮肤巩膜黄染、蜘蛛痣、男性乳房发育、腹水);
实验室检查
①丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)、碱性磷酸酶(ALP)和胆红素是评价肝损伤的标志物,血清白蛋白水平和凝血酶原时间(PT)是评价肝功能的标志物。目前,肝病医师用R值定义肝细胞性肝损伤、胆汁淤积性肝损伤及两者混合性;
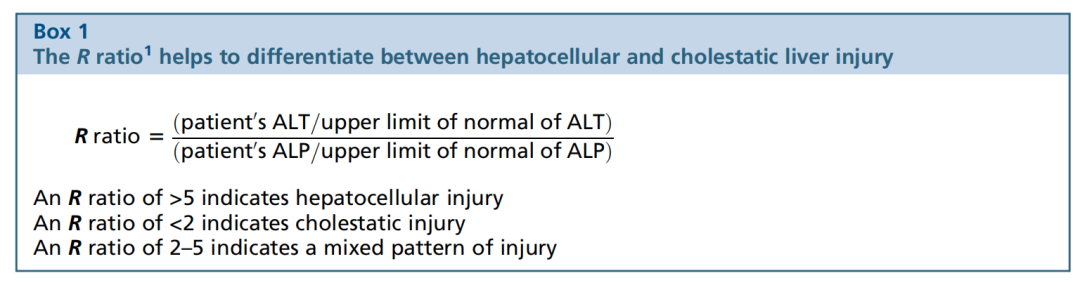
图. R值计算公式及对应肝损伤类型
②病毒学检查、自身免疫抗体检查;
③代谢疾病筛查(铁离子、铜蓝蛋白、ɑ-1抗胰蛋白酶);
④影像学检查。
肝脏穿刺活检的适应症
①没有明确的病因导致的肝脏检查异常;
②导致肝脏检查异常的病因复杂;
③影像提示异常(考虑肿瘤性病变时)。
肝脏穿刺活检方式
①经皮穿刺(需要CT或超声引导);
②经颈静脉穿刺(适用于凝血功能障碍或具有腹水的患者)。
需要肝脏穿刺活检的疾病
①自身免疫性肝炎(AIH)、原发性胆道胆管炎(PBC)和硬化性胆管炎;
②非肝硬化性门静脉高压症、早期Wilson病;
③肿瘤。
不需要肝脏穿刺活检的疾病
①酒精相关肝病(ALD)、非酒精性脂肪性肝病(NAFLD)、遗传性血色素沉着病(HH);
②晚期Wilson病和ɑ-1抗胰蛋白酶(A1AT)缺乏性肝病;
③慢性病毒性肝炎。

图. 肝脏疾病检查及处理思路流程
肝脏非肿瘤性疾病
自身免疫性肝炎(AIH)
定义:
一种免疫介导的肝脏疾病,对肝脏自身抗原的自我耐受性丧失,导致肝脏炎症、坏死和纤维化。
临床表现:
①好发于成人和儿童,主要为女性,最常见的症状是疲劳、肌痛和关节痛。约25%-35%的AIH患者无症状;
②可表现为慢性肝炎、肝硬化、急性肝炎或急性肝功能衰竭,在半数患者中存在肝外自身免疫性疾病(自身免疫性甲状腺炎、类风湿性关节炎、系统性红斑狼疮、乳糜泻、炎症性肠病、白癜风和1型糖尿病)。
实验室检查:
血清转氨酶水平升高、血清免疫球蛋白G(IgG)水平升高、循环自身抗体阳性(抗核抗体(ANA)、抗平滑肌抗体(ASMA)、抗肝肾微粒体1型抗体)。
肝活检组织病理典型改变:
界板性肝炎、浆细胞浸润、小叶性肝炎和小叶中心坏死。
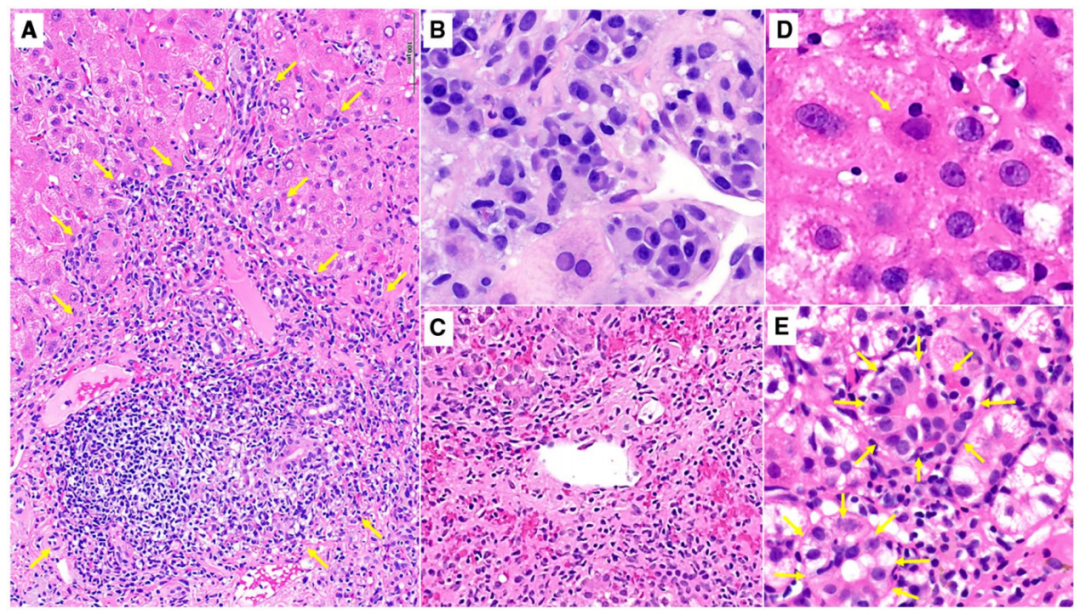
图. AIH的组织学特征。(A)汇管区淋巴、浆细胞和界板性肝炎,涉及门静脉周长的50%。(B)汇管区炎症浸润以浆细胞为主。(C)中央静脉小静脉周围炎。(D)再生肝细胞排列成花环状。
图片源自于doi: 10.1002/hep.31065.
原发性胆汁性胆管炎(PBC)
定义:
一种因免疫介导的小叶内小胆管损伤、破坏而产生的慢性胆汁淤积性肝病,最终导致肝硬化。
临床表现:
①好发于30-60岁女性;
②最常见的症状是疲劳和瘙痒,一部分患者没有症状;
③一些患者中可触及肝肿大,常伴有肝外自身免疫性疾病(干燥综合征和硬皮病)。
实验室检查及诊断标准:
①胆汁淤积性肝病的检查首先进行影像学检查,以排除胆管狭窄或梗阻,包括大的胆管硬化性胆管炎;
②胆汁淤积伴ALP活性升高;
③抗线粒体抗体(AMA)阳性;
④ 肝活检中非化脓性胆管炎和中小胆管破坏的组织病理学改变。
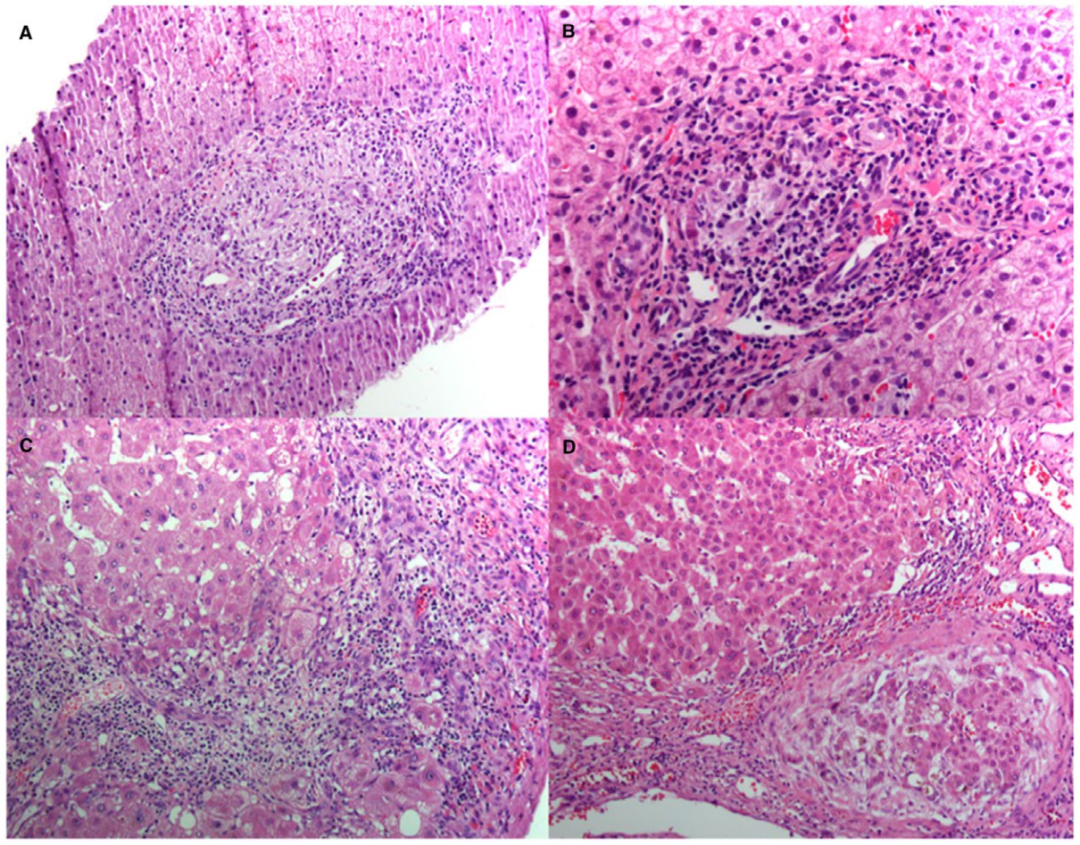
图. PBC组织病理学改变(A)1期PBC伴汇管区炎症和扩张增生的的胆管;(B)2期PBC伴汇管区炎症、局灶性界面性肝炎和胆管增生;(C)3期PBC伴肝脏桥接性炎症;(D)4期PBC显示肝硬化伴胆管减少。
图片源自于DOI: 10.1002/hep.30145
原发性硬化性胆管炎(PSC)
定义:
原发性进行性胆管纤维炎性疾病,以胆管的炎症和瘢痕形成为特征。
临床表现:
①可能无症状,但最常见的症状是疲劳和瘙痒;
②PSC可导致胆管梗阻、胆管炎、胆管癌和失代偿性肝硬化等并发症。
影像学改变:
PSC多灶性狭窄,交替伴有正常或轻微扩张的胆管节段,在胆管造影上形成“串珠状”改变。
实验室检查:
60%的PSC患者有IgG升高,高达50%的PSC患者有循环自身抗体,最常见的是非典型蛋白酶-3抗中性粒细胞细胞质抗体(p-ANCA),但也有ANA和ASMA。
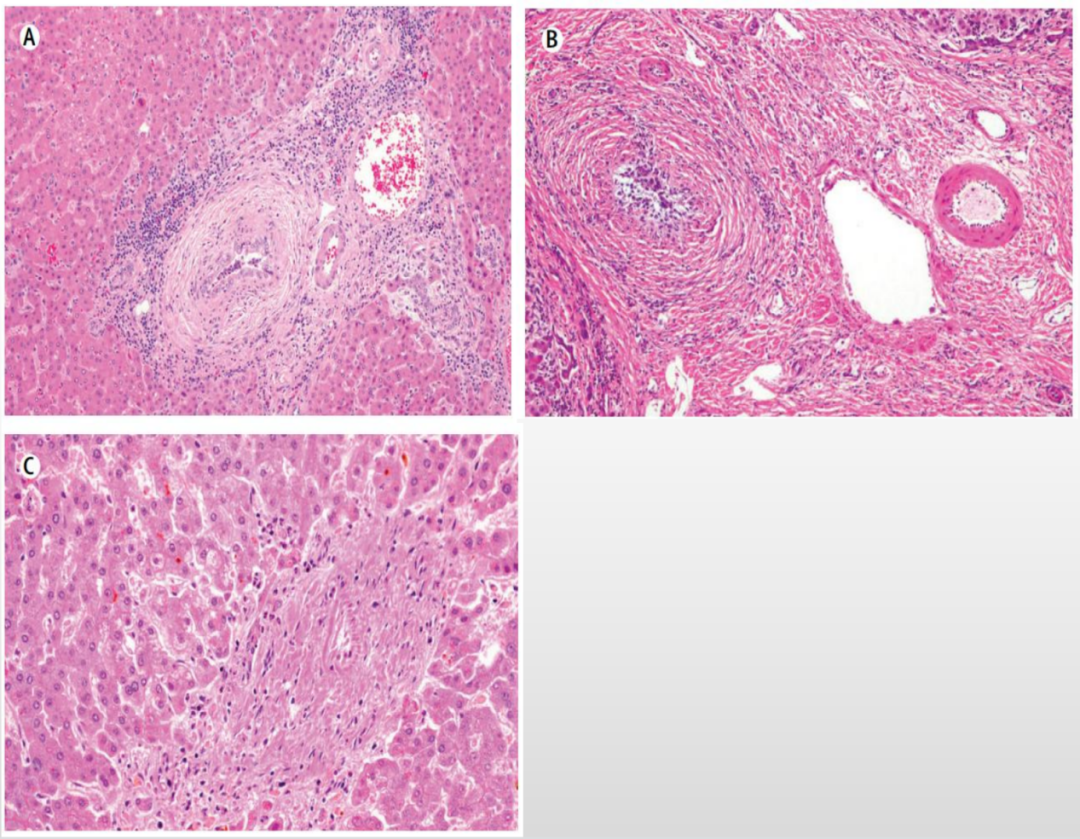
图. PSC组织病理改变。(A)胆管周围有“洋葱样同心圆”样纤维化改变,肝细胞水肿,伴轻度汇管区炎症细胞浸润。(B)胆管上皮呈退行性和萎缩性变化,胆管轮廓不规则。(C)胆管消失,通常见于PSC晚期。
图片源自于https://doi.org/10.1016/S0140-6736(18)30300-3
非肝硬化性门脉高压(NCPH)
定义:
在无肝硬化的情况下,肝-静脉或门-腔静脉压力梯度超过5 mm Hg。
病因:
通常是肝外或全身性疾病有关。
分类:
肝前、肝(窦前、窦后或窦后)或肝后。

图. NCPH常见病因
酒精相关性肝病(ALD)
诊断标准:
①病史(男性饮酒>3次/每天,或女性饮酒>2次/每天);
②影像学显示肝脂肪变性或肝硬化;
③AST和ALT升高(通常<400 IU/L,AST/ALT比值>1);
④ 不需要肝脏穿刺活检。
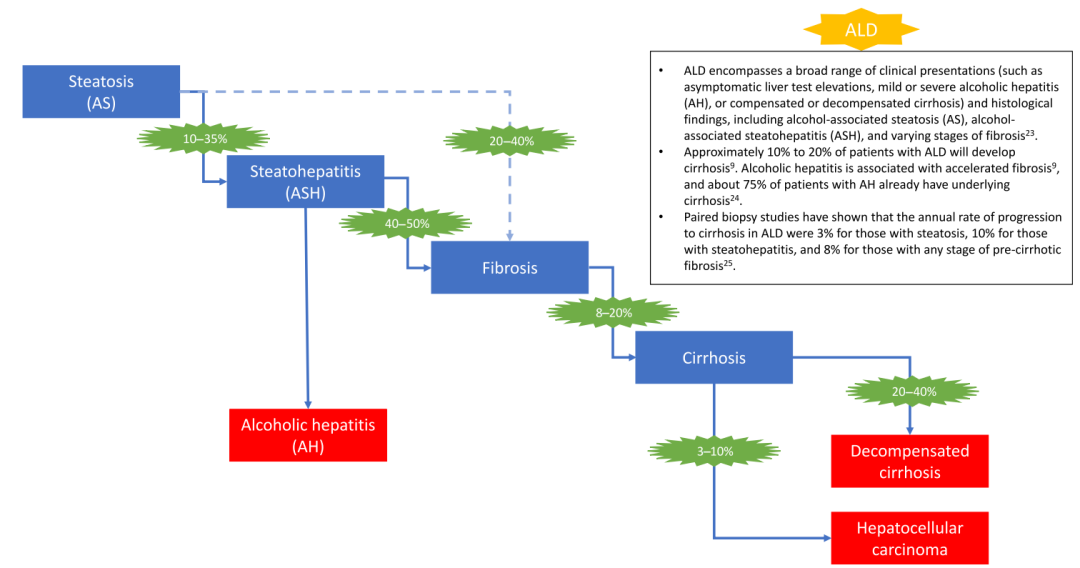
图. ALD相关发展历程
非酒精性脂肪性肝病(NAFLD)
定义:
肝脏脂肪变性(在影像学上或活检中超过5%的肝细胞)与代谢危险因素相关,没有过度饮酒或其他慢性肝病。
病因:
2型糖尿病、肥胖、脂肪代谢异常。
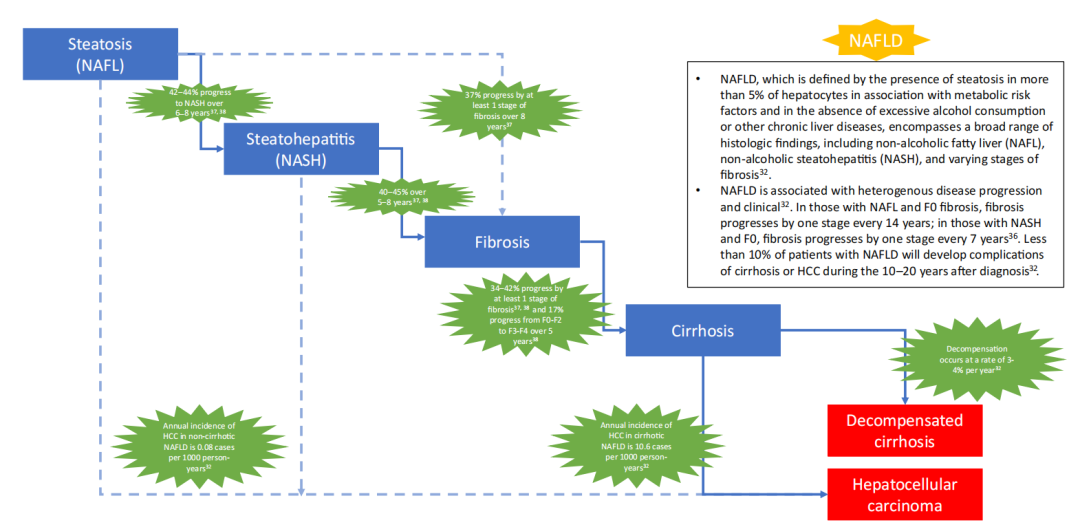
图. NAFLD发展历程
肝脏脂肪变性
大泡性脂肪变性常见疾病:
非酒精性脂肪肝、酒精相关性肝病、丙型肝炎、乳糜泻病、Wilson病、肠外营养、饥饿、低β-脂蛋白血症、脂肪代谢障碍、甲状腺功能减退、药物(如甲氨蝶呤、他莫昔芬、胺碘酮、糖皮质激素)。
微泡性脂肪变性常见疾病:
Reye综合征、妊娠急性脂肪肝、HELLP综合征、先天代谢障碍(如卵磷脂-胆固醇酰基转移酶缺乏、胆固醇酯储存病、Wilson病)、药物(如丙戊酸盐、抗逆转录病毒药物)。
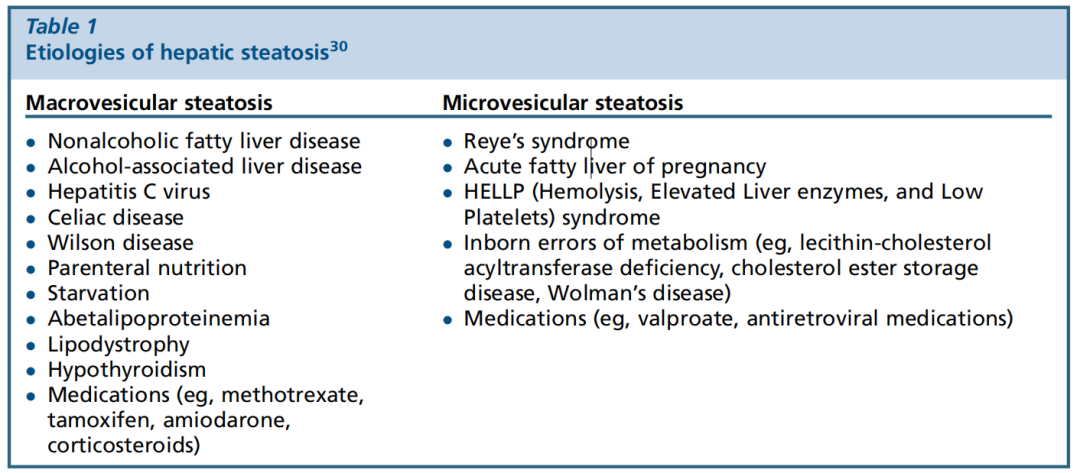
图. 肝脏脂肪变性常见病因
遗传性血色病(HH)
HH一种遗传性疾病,可导致组织(包括肝脏、胰腺、心脏、关节、皮肤)中的过度铁沉积和随后的功能障碍(如肝硬化、糖尿病、充血性心力衰竭、关节痛、皮肤色素沉着和迟发性皮肤卟啉症)。目前不建议通过肝活检来量化铁超载和评估纤维化。
肝豆状核变性(Wilson病)
Wilson病是一种罕见的常染色体隐性遗传病,由缺陷的ATP7B铜转运蛋白引起,导致肝脏和全身铜沉积。可表现为肝硬化(伴或不伴门脉高压和失代偿)、急性肝炎或急性肝功能衰竭。在早期Wilson病,肝脏穿刺活检是评估纤维化的阶段和测量肝铜浓度的重要方法。
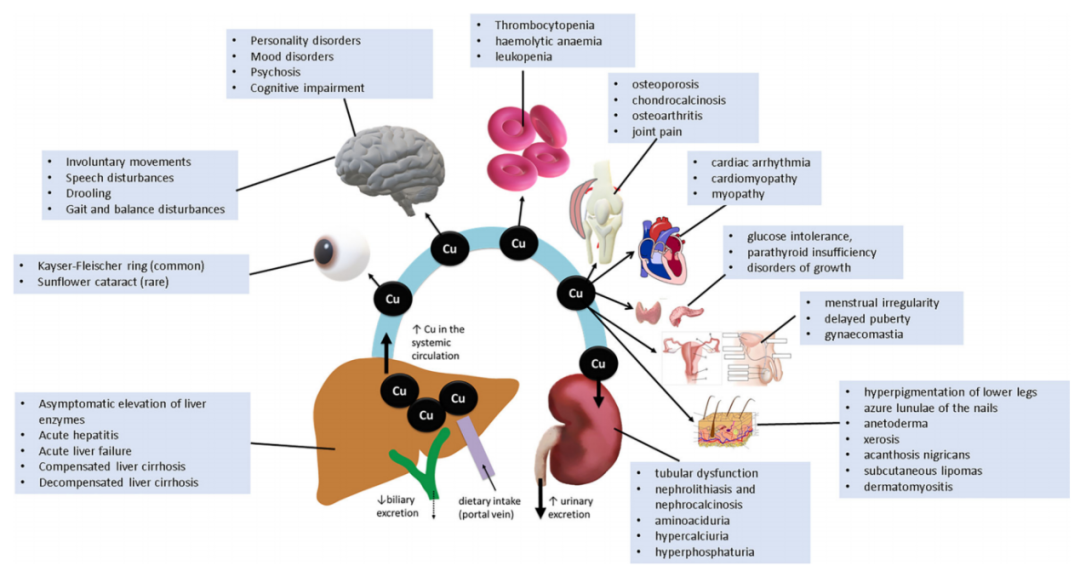
图. Wilson病中的铜毒性
膳食铜(Cu)通过门静脉运输,并在肝脏中积累,肝脏是全身铜平衡的中心器官。ATP7B功能障碍可以引起胆道铜排泄障碍,并导致铜在肝脏中逐渐积累。当肝脏储存铜的能力耗尽时,过量的非铜蓝蛋白结合的铜进入体循环,并沉积在各种器官中,产生肝外铜毒性。铜在角膜、大脑、红细胞、骨骼肌和心肌细胞、大关节的滑膜和肾实质中积累。非铜蓝蛋白结合的血浆铜被肾小管上皮过滤,并通过尿液排出。
图片源自于doi:10.1038/s41572-018-0018-3.
ɑ -1抗胰蛋白酶缺陷症(A1ATD)
①儿童常见,成人罕见;
②A1AT是一种由肝脏合成并分泌的丝氨酸蛋白酶抑制剂(Pi),它可以保护肺组织中的弹性蛋白免受中性粒细胞弹性蛋白酶的过度破坏;
③SERPINA1的不同突变导致肝细胞中错误折叠的A1AT蛋白的积累(导致慢性肝病)和A1AT的体循环减少(导致肺气肿);
④ 在儿童时期表现为急性胆汁淤积性肝病或暴发性肝炎。
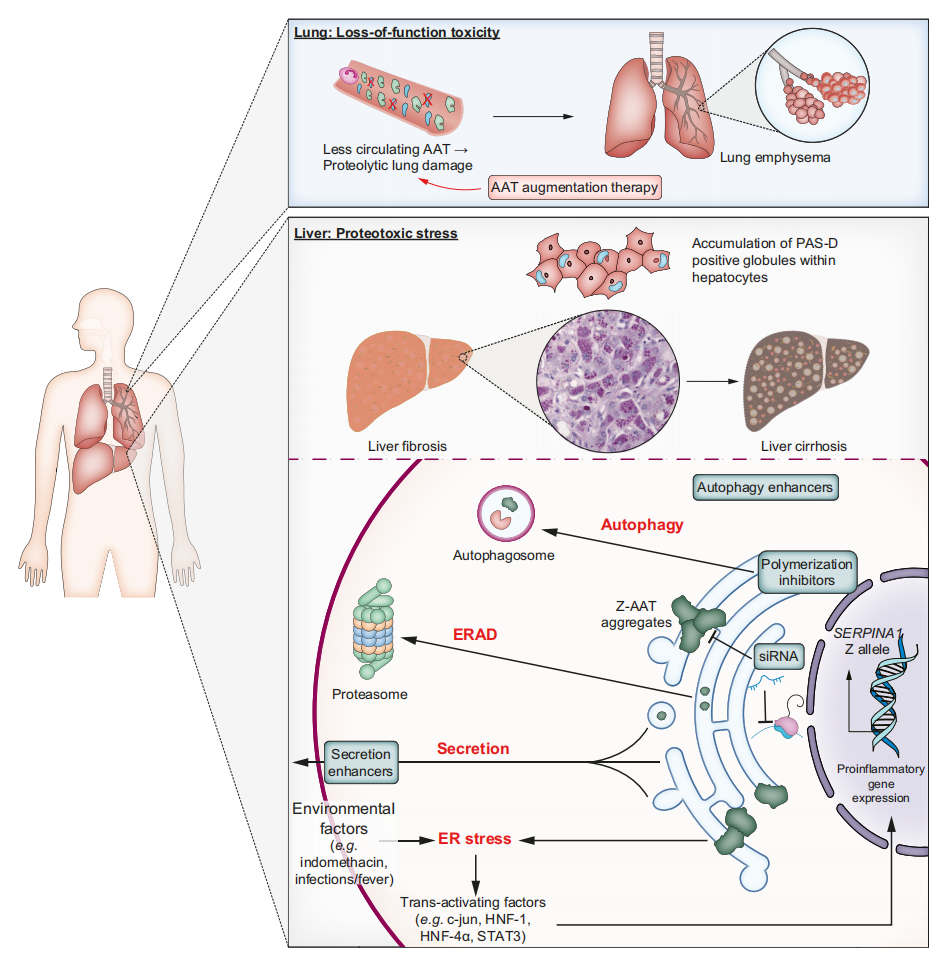
图. A1AT缺乏症的病理生理学、临床表现和治疗方法
A1AT缺失是由于编码A1AT(名为SERPINA1)的基因突变,导致A1AT在肝脏中的降解或保留增加。A1AT的错误折叠和聚合,促进了蛋白质毒性应激、肝硬化和肝肿瘤的发展。体循环中A1AT的缺失导致蛋白酶抑制不足(功能丧失表型),从而导致蛋白水解性肺损伤和泛小叶性肺气肿。
组织学上,在PAS-D染色中,A1AT的保留可以显示为包涵体。特征的纯合子Pi*Z突变,导致AAT分泌减少,单体/聚合Z-AAT被ERAD和自噬小体降解。由此产生的内质网应激刺激A1AT的产生,从而导致疾病恶性循环。AATD相关肝病的治疗策略包括siRNA,减少AAT的产生和分泌,以及自噬增强子减少蛋白质积累。A1AT,ɑ-1抗胰蛋白酶;ER,内质网;ERAD,内质网相关的降解。
图片源自于https://doi.org/10.1016/j.jhep.2021.11.022.
参考文献及书籍:
Mitten EK, Rutherford A. How Hepatologists Use Liver Biopsy in the Evaluation of Liver Disease? Surg Pathol Clin. 2023 Sep;16(3):443-456.


