Front Immunol:脐带血来源的NK细胞治疗子宫内膜癌效果显著
时间:2024-01-12 20:45:26 热度:37.1℃ 作者:网络
自然杀伤(NK)细胞的过继转移是治疗晚期恶性肿瘤的一种可行方法。先前研究已经开发了一种简单、安全且具有成本效益的方法,可以从脐带血(CB)中获得高产率的纯功能性NK细胞,而无需细胞分选、饲养细胞或多种细胞因子。
子宫内膜癌(EC)在全球范围内的发病率和疾病相关死亡率不断上升。尽管有针对晚期或复发性子宫内膜癌的标准治疗,但疗效和预后仍然较差,这突出了创新疗法的必要性。
在子宫内膜癌患者中观察到NK细胞的功能障碍,如细胞数量减少和细胞毒性受损,那么基于NK细胞的过继免疫疗法方案是否能够增强NK细胞的抗肿瘤反应呢?
2023年6月,Frontiers in Immunology期刊上发表了题为“Case Report: Cord blood-derived natural killer cells as new potential immunotherapy drug for solid tumor: a case study for endometrial cancer”的研究论文,研究表明:脐带血来源的NK细胞疗法有望成为癌症的一种有效治疗方法。

图源 | pubmed.ncbi.nlm.nih.gov
该研究报告了一例52岁的女性患者,诊断为低分化IVB期(T3N2M1)子宫内膜癌,患者有副肿瘤综合征,表现为白血病样反应和治疗前血小板增多症。由于她的NK细胞活性极低,该患者在2022年3月至9月期间接受了两个疗程的脐带血来源NK(CB-NK)细胞免疫治疗。
研究人员选择了两个在8/10 HLA匹配的具有KIR错配的可用脐带血单元,并能够从脐带血中生成高产率(>1.0×1010NK细胞)、高纯度(>90%)和功能优越(>80%)的NK细胞,而无需细胞分选、饲养细胞或多种细胞因子。
注:HLA(人类白细胞抗原)
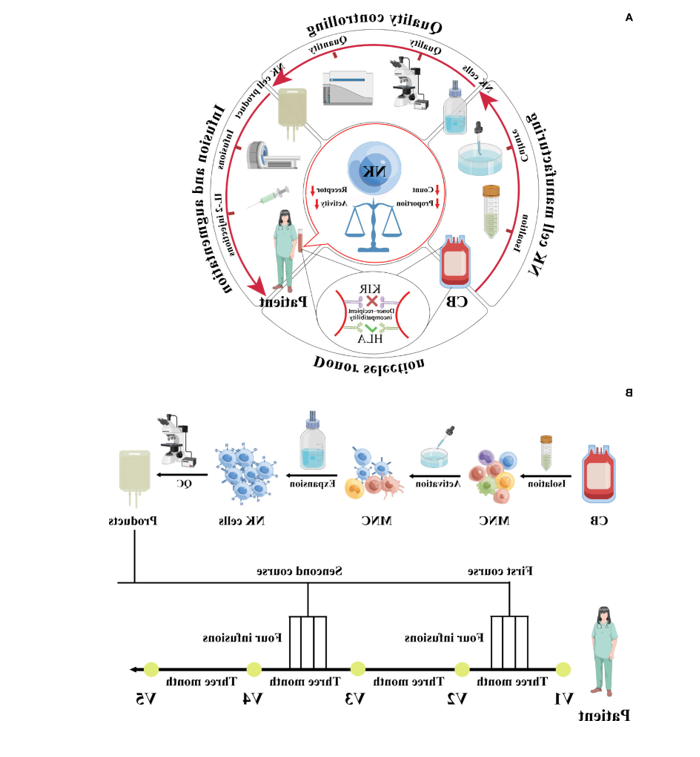
脐带血来源NK细胞产品的临床级制造过程
以及脐带血来源NK细胞治疗和免疫表型监测的时间表
输注CB-NK细胞后未观察到不良反应或移植物抗宿主病。临床上观察到CB-NK细胞可以调节全身抗肿瘤免疫,增加NK细胞活性,降低肿瘤活性,提高生活质量,并随着多个淋巴结转移的消失而减小了腹部和骨盆肿块。而且,CB-NK细胞免疫治疗后,白细胞和血小板计数降至正常水平。
在CB-NK细胞免疫疗法的第一个周期之后,患者获得了部分反应,体力、食欲和睡眠质量都有所改善。通过CT扫描评估了CB-NK细胞免疫疗法的疗效,结果显示腹部和骨盆肿块以及不同区域的多个肿大淋巴结显著减少。然而,右髂血管周围的一些淋巴结和双侧腋窝淋巴结的大小略有增加,两肺仍存在多个结节,表明可能有转移(下图A)。
为了进一步评估CB-NK细胞疗法对进行性肿瘤的治疗效果,在第二治疗周期后进行了PET-CT扫描。扫描结果显示,与治疗前的PET-CT成像相比,子宫右侧高代谢物质的尺寸减小,子宫的代谢和体积显著减少。尽管右股骨头的肿块和右第10和第11肋骨的骨转移没有变化,但骨转移的代谢恢复正常。颈部、纵隔、腹膜后和骨盆的多发淋巴结转移也消失(下图B)。
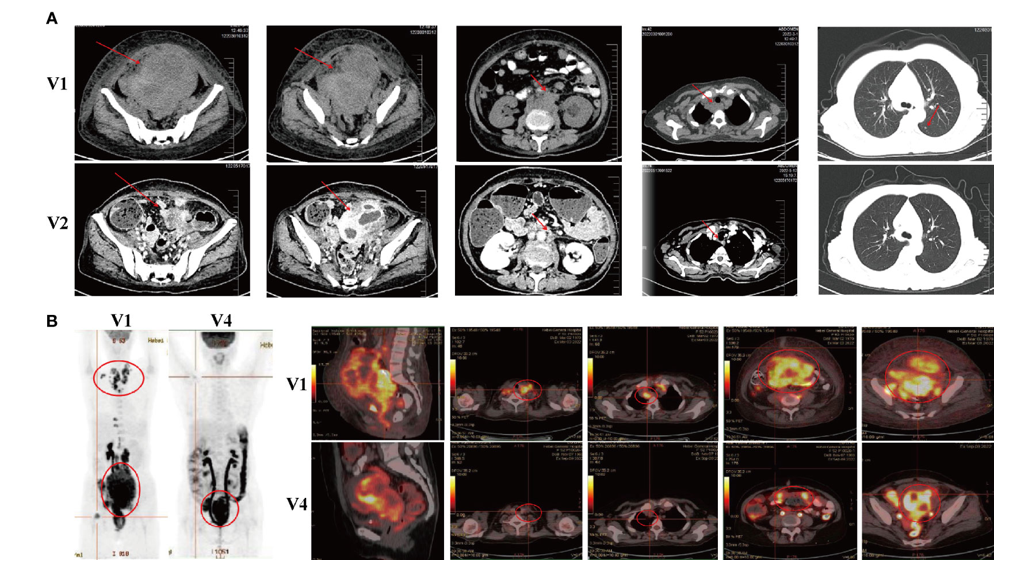
在不同时间点对患者进行放射学评估。
患者的生活质量得到了显著改善,两个疗程的CB-NK细胞治疗后,表现状态评分从3分降至1分(下图A)。肿瘤标志物HE4和CA125(下图B、C)以及血液参数白细胞计数(WBC)和血小板(PLT)(下图D、E)迅速下降,而血红蛋白(Hb)增加到正常水平(下图F)。而且,NK细胞活性在两个疗程的治疗中逐渐增加(下图G)。注射CB-NK细胞期间或之后未观察到副作用,没有出现发烧、呕吐或抽搐等。此外,在整个随访期间,没有报告移植物抗宿主病(GVHD)的迹象。
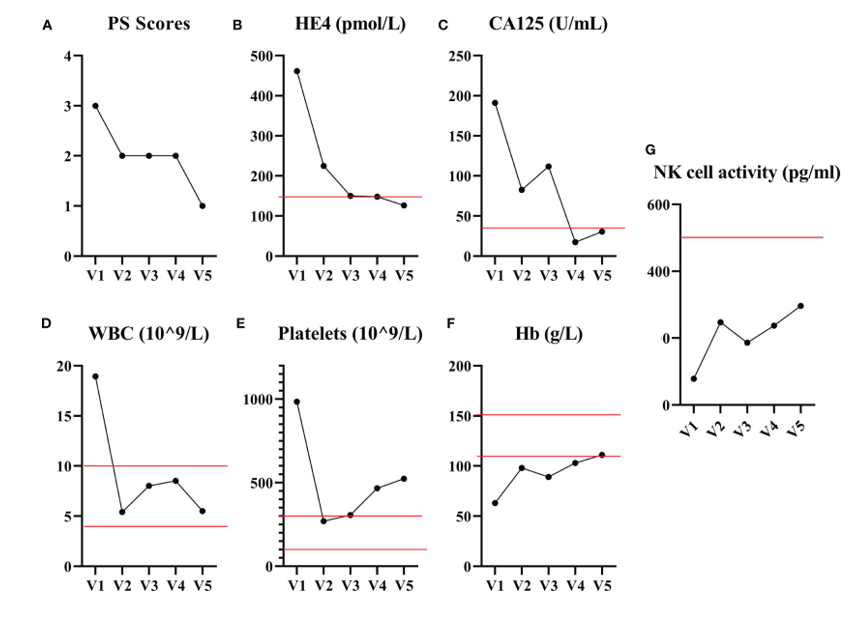
CB-NK细胞治疗前后的表现状态评分和血液生化检查结果。
为了阐明CB-NK细胞介导的免疫反应的机制,研究人员使用流式细胞术对免疫表型变化进行了分析。结果显示,CB-NK细胞治疗通过减少与疾病相关的异常表型显著增强了免疫系统。
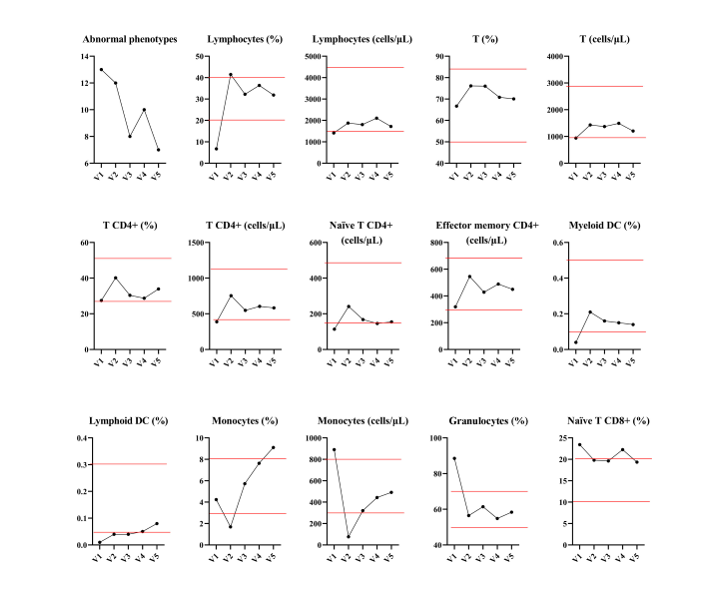
分析CB-NK细胞治疗前后免疫表型的变化。
结语
该病例报告描述了CB-NK细胞免疫疗法在子宫内膜癌治疗中的首次应用。临床结果表明,CB-NK细胞治疗子宫内膜癌是安全有效的。这项试验为癌症免疫疗法开辟了一条新的途径,并启发了使用CB-NK细胞进行进一步的临床研究。CB-NK细胞有潜力成为治疗恶性肿瘤的新型“免疫药物”。
总之,CB-NK细胞对子宫内膜癌的良好活性在临床上得到了证明,未来有望在临床上帮助越来越多的子宫内膜癌患者,并且拓展到其他癌症的治疗中。
参考文献:
Mu, Yongxu et al. “Case Report: Cord blood-derived natural killer cells as new potential immunotherapy drug for solid tumor: a case study for endometrial cancer.” Frontiers in immunology vol. 14 1213161. 30 Jun. 2023, doi:10.3389/fimmu.2023.1213161


