2024ASCO肝癌免疫治疗的最新进展(系统联合局部治疗&新疗法篇)
时间:2024-06-10 21:00:20 热度:37.1℃ 作者:网络
2024年ASCO肝癌免疫治疗新进展聚焦于晚期/转移性肝癌和不可切除的肝癌患者,治疗方案涉及全身治疗,全身和局部治疗的结以及新治疗方案的探索。
本次分享系统治疗与局部治疗的结合和新疗法。
系统治疗联合局部治疗
01 EMERALD-1研究治疗期的安全性分析
EMERALD-1研究(注册号NCT03778957)是一项3期、随机、安慰剂对照的研究,研究对符合栓塞条件的不可切除肝癌患者使用度伐利尤单抗联合/不联合贝伐珠单抗进行经动脉化疗栓塞治疗,研究共入组了来自全球18个国家和地区的616例适于TACE不可切除的HCC患者,按照1:1:1随机分为三组:A组,治疗方案为TACE+度伐利尤单抗,最后一次TACE后给予度伐利尤单抗+安慰剂(两联方案组);B组,治疗方案为TACE+度伐利尤单抗,最后一次TACE后给予度伐利尤单抗+贝伐珠单抗(三联方案组);C组,治疗方案为TACE+安慰剂,最后一次TACE后给予安慰剂+安慰剂(单纯TACE组)。2024年ASCO GI也报告了该研究。该研究主要终点达到:与安慰剂+TACE相比,度伐利尤单抗(D)+贝伐珠单抗(B)+经动脉化疗栓塞(TACE)显著改善了无进展生存期(中位15.0 vs 8.2个月),且在符合栓塞条件的不可切除肝细胞癌患者中安全性可控。
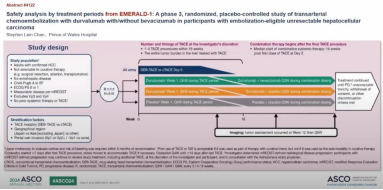

本次会议介绍了这项研究的事后探索性分析,评估了该研究的2个治疗期的安全性:D-TACE(D-T)和D-B。这个研究的设计非常独特的,不同于常规的治疗设计,因为TACE跟系统治疗以前经常同时使用,而这里是先系统性治疗,再序贯或同步治疗。看一下实施后的具体数据,首先第一阶段是度伐利尤单抗联合TACE,第二阶段是贝伐利珠单抗和度伐利尤单抗以及TACE,有一些患者会同步接受TACE的治疗,在两个时间里AE都是相对比较轻的,意味着安全性非常好。

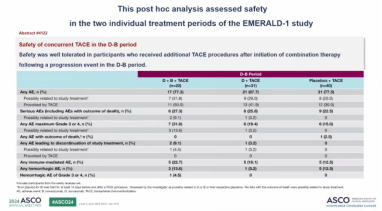
D+B+TACE在D-T和D-B阶段中均具有可控的安全性,这与个体因素和潜在疾病一致。
02 SHATA-001研究

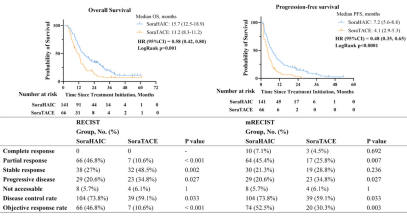
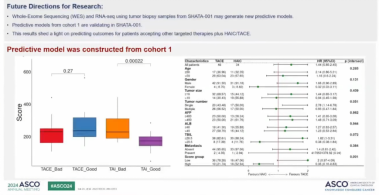
索拉非尼联合HAIC或TACE对比索拉非尼单药用于晚期肝癌一线治疗的随机对照研究。研究当中头对头地比较了HAIC以及TACE,来观察不可切除的大的肝癌的患者应该到底是优选TACE还是HAIC。根据初步数据,可以看到HAIC联合索拉非尼组是优于TACE联合索拉非尼的。研究一共入组了207例患者。主要终点方面,索拉非尼联合HAIC具有更好的OS获益,中位OS分别为:15.6和11.2月(HR=0.53,P<0.001)。其他终点方面,PFS也更优(中位PFS:6.9 vs 4.2月,HR=0.51,P<0.001)。ORR的差别也很大,RECIST v1.1评估的ORR分别为46.8%和10.6%,mRECIST评估的ORR分别为45.4%和25.8%。另外,HAIC的安全性也更好,两组的G3/4 TRAE分别为39.3%和56.7%。
03 TACE、TKI联合或不联合SBRT用于门静脉癌栓患者一线治疗的随机对照研究
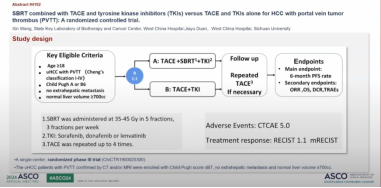
该项三期研究也同时在做。我们可以看到加上了立体定向放疗SBRT之后,患者会有更多的获益,PFS、OS均有改善。
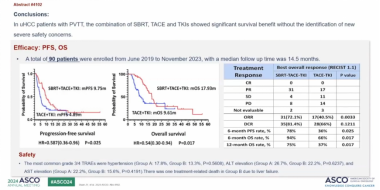
04 阿帕替尼、卡瑞利珠单抗联合肝动脉输注奥沙利铂和5-氟尿嘧啶、阿帕替尼、卡瑞利珠单抗作为肝细胞癌伴门静脉肿瘤血栓的一线治疗:一项随机多中心临床试验
该研究中一组是系统联合局部治疗,一组是系统治疗,目前尚在设计阶段,研究方向包括使用肿瘤活检样本进行全外显子组测序(WES)和RNA测序以寻找额外HAIC治疗的预测性生物标志物,还将探索能预测接受阿帕替尼和卡瑞利珠单抗治疗的患者的反应和生存的生物标志物。

05 PLATIC研究
PLATIC研究是一项单中心II期单臂临床试验,研究PD-1抑制剂(信迪利单抗)和仑伐替尼联合TACE-HAIC作为初始不可切除HCC的转化治疗。77.2%的患者在接受了这种方案的治疗之后完成了转化,由于大部分的患者都是晚期肝癌患者,治疗后都有了非常不错的生存曲线。
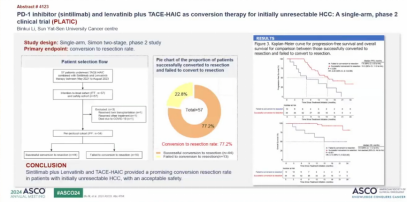
06 REPLACE研究
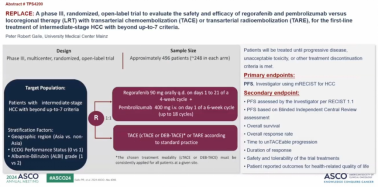
REPLACE研究是一项Ⅲ期、随机、开放标签试验,旨在评估瑞戈非尼和帕博利珠单抗与局部区域治疗(LRT)联合经动脉化疗栓塞(TACE)或经动脉放射栓塞(TARE)的安全性和有效性,用于up-to-7标准之外的中期肝细胞癌(HCC)患者的一线治疗。(正在招募中)
07 替雷利珠单抗加调强放疗治疗可切除大血管浸润性肝细胞癌:一项前瞻性、单臂、II期试验

结论是替雷利珠单抗联合放疗作为可切除HCC伴MVI的围手术期治疗的有效性和耐受性值得进一步探索。
08 NeoLEAP-HCC研究
NeoLEAP-HCC研究围手术期帕博利珠单抗和仑伐替尼治疗可切除肝细胞癌,是一项单臂、多中心、II期试验,旨在评估帕博利珠单抗联合仑伐替尼作为可切除HCC患者围手术期治疗的疗效和安全性。主要终点是主要病理反应(MPR),定义为≤50%的肿瘤床中的活肿瘤细胞。次要终点为完全病理反应(pCR)、客观缓解率(ORR,RECIST v1.1和mRECIST)、无病生存期(DFS)、总生存期(OS)和安全性。当前已完成患者招募,显示出帕博利珠单抗联合仑伐替尼在可切除肝细胞癌的新辅助治疗中显示出良好的抗肿瘤疗效和可控的毒性。还需要再等一年得到最终生存数据。在这个研究也用了ctDNA组织样本去进行生物标记物分析,希望能揭示帕博利珠单抗和仑伐替尼在肝癌治疗中的分子学上新的一些协同机制。

新疗法
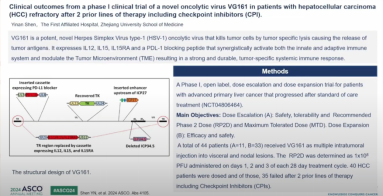
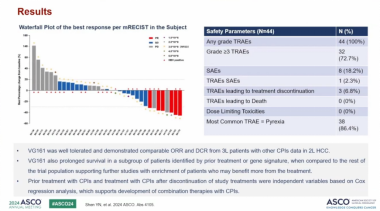
01 新型溶瘤病毒VG161在既往2线治疗后难治性肝细胞癌患者中的I期临床试验的临床结果
这项研究使用了mRNA来增加肿瘤细胞中的新抗原,即表达IL12、IL15/IL15受体α单元和PD-L1阻断肽的VG161,这对于肝癌而言是非常新的一个治疗方式。研究结果显示VG161耐受性良好,在2L HCC中与其他CPI数据具有相当的ORR和DCR,可见该疗法相当有前景,因为大部分接受治疗的患者既往接受过二到三线以上的治疗,对这个mRNA治疗都有应答的。现在中国也有多项研究在启动去评估MRNA疫苗的应用。
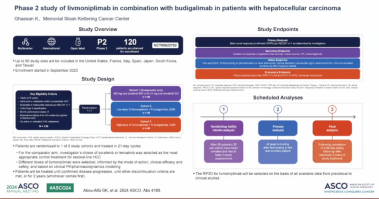
02 livmoniplimab联合budigalimab治疗肝细胞癌患者的2期研究
单克隆抗体livmoniplimab靶向GARP-TGF-β1复合物,阻止活性TGF-β1的释放。Budigalimab布格利单抗是一种抗PD-1免疫检查点抑制剂单克隆抗体。
主要目标包括确定livmo与budi联合使用的最佳剂量和确定推荐的3期剂量(RP3D),以及评估livmo+budi的疗效(最佳总体缓解率)。次要和探索性目标是评估疗效(反应持续时间、无进展生存期、总生存期)、安全性、耐受性、免疫原性、药代动力学/药效学(PK/PD)、预测性生物标志物以及患者报告的症状和耐受性。
在今年的ASCO大会上,我们见证了非常多重要研究数据的更新,总结而言系统疗法取得了一定的进展,系统联合局部的治疗的话还是非常重要,我们可以利用现有的药物和方案进行不同的联合来提高肝癌治疗的疗效。与此同时我们也在等待创新疗法的数据蓬勃涌现,新的技术,比如细胞疗法,MRA疫苗,这些领域都是非常有前景的。
参考文献:
[1]Yunfei Yuan,et al.PD-1 inhibitor(sintilimab)and lenvatinib plus TACE-HAIC as conversion therapy for initially unresectable HCC:A single-arm,phase 2 clinical trial(PLATIC).ASCO2024,Abstract 4123
[2]Binkui Li,et al.Conversion to Resectability Using Transarterial Chemoembolization Combined With Hepatic Arterial Infusion Chemotherapy for Initially Unresectable Hepatocellular Carcinoma.Ann Surg Open.2021 Apr 8;2(2):e057..doi:10.1097/AS9.0000000000000057
[3]https://www.clinicaltrials.gov/study/NCT04777851
[4]https://ascopubs.org/doi/pdfdirect/10.1200/JCO.2024.42.16_suppl.TPS4200
[5]https://ascopubs.org/doi/pdfdirect/10.1200/JCO.2024.42.16_suppl.4118
[6]https://www.clinicaltrials.gov/study/NCT05389527
[7]https://www.clinicaltrials.gov/study/NCT04806464


