2024 EHA | 米托蒽醌脂质体多项血液领域研究成果精彩亮相!
时间:2024-07-13 11:01:16 热度:37.1℃ 作者:网络
前言
第29届欧洲血液学会(EHA)年会于2024年6月13日-16日在西班牙马德里隆重举行,作为欧洲血液学领域最具规模的国际会议之一,EHA年会吸引了来自全世界各地的专家学者进行分享交流、公布并传递血液学的创新进展和突破性临床研究成果。
米托蒽醌脂质体(Lipo-MIT)是我国自主研发、具有独立知识产权的2类新药,于2022年1月7日获得NMPA批准上市,适应症为既往至少经过一线标准治疗的复发或难治的外周T细胞淋巴瘤(PTCL)。此次EHA盛会上展示了多项米托蒽醌脂质体最新研究成果,包括2篇壁报(Poster)、2篇电子壁报(e-Poster)及多篇在线摘要(Publication Only),研究领域涉及白血病、移植预处理和淋巴瘤,有望丰富此类疾病的临床用药选择。
急性髓系白血病
摘要号:P602(Poster)
含盐酸米托蒽醌脂质体方案治疗急性髓系白血病的真实世界研究:短期疗效及安全性分析
英文题目:Real-world outcomes of mitoxantrone hydrochloride liposome regimen for acute myeloid leukemia: a short-term analysis of efficacy and safety1
研究团队:哈尔滨血液病肿瘤研究所 马军教授团队
研究内容:
该研究是一项多中心、非干预性、双向队列研究,旨在观察真实世界中含米托蒽醌脂质体(Lipo-MIT)方案治疗急性髓系白血病(AML)的疗效和安全性。截至2024年2月21日,共纳入239例至少接受一周期含Lipo-MIT方案治疗的AML患者,初治117例、复发/难治122例。初治患者整体复合完全缓解(CRc)率为84.6%(99/117)、客观缓解率(ORR)为91.5%(107/117),45例接受诱导治疗患者CRc率为75.6%、ORR为88.9%;复发/难治患者整体CRc率为45.1%(55/122)、ORR为55.7% (68/122),101例接受诱导治疗患者CRc率为41.6%、ORR为54.5%。Lipo-MIT+阿糖胞苷(MA)为初治患者使用最多的方案,CRc率为86.7%;MA和Lipo-MIT+阿糖胞苷+依托泊苷(MAE)为复发/难治患者使用较多的方案,CRc率分别为54.5%和34.6%。常见3/4级治疗相关不良事件(TRAE)为血小板计数降低(64.5%)、白细胞计数降低(63.6%)、中性粒细胞计数降低(60.7%)、贫血(48.6%)和肺部感染(5.9%)。研究结果证实含Lipo-MIT方案在AML治疗中具有良好的疗效和安全性。
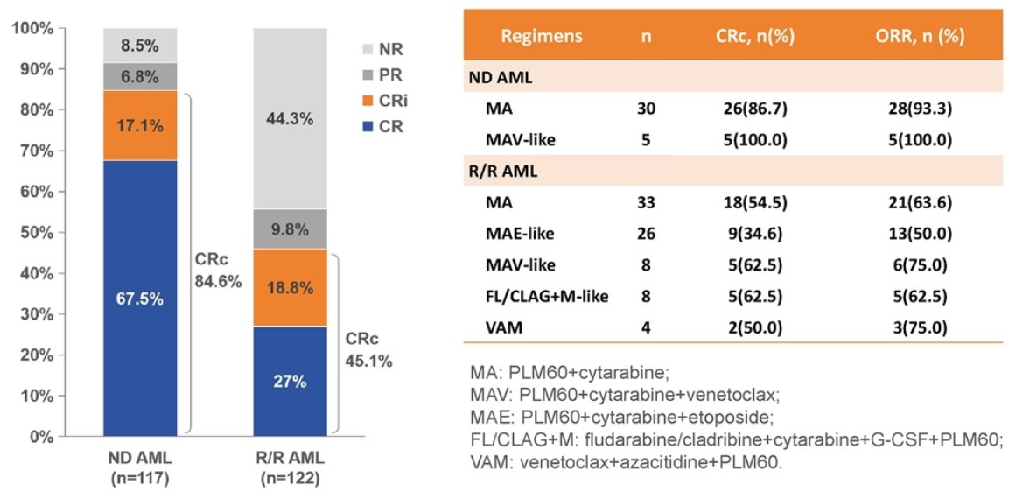
图1. 患者整体疗效结果及不同方案疗效结果
摘要号:P1749(e-Poster)
盐酸米托蒽醌脂质体联合CLAG方案治疗复发/难治AML(非M3)的疗效和安全性
英文题目:Efficacy and safety of mitoxantrone hydrochloride liposome combined with CLAG regimen in refractory and relapsed acute myeloid leukemia (non-M3)2
研究团队:陆军军医大学第二附属医院 张曦教授团队
研究内容:
该研究回顾性分析了2022年6月至2024年1月期间在该中心接受Lipo-MIT联合CLAG(克拉屈滨+阿糖胞苷+粒细胞集落刺激因子)方案治疗复发/难治AML患者的数据。共纳入16例患者,CRc率为68.8%(11/16),CRc患者中9例(81.8%)达到流式MRD阴性。中位随访4.42(0.89-20.1)个月,7例患者接受单倍体造血干细胞移植(haplo-HSCT)治疗,目前仍处于缓解期,3例患者复发。中位无复发生存期(RFS)为17.1(0.59-17.1)个月,中位总生存期(OS)尚未达到。常见的≥3级TRAE为血液学毒性(100.0%)、败血症(18.8%)和肺部感染(12.5%),中性粒细胞计数<0.5 x 109/L的中位持续时间为24(14-41)天,血小板计数<20 x 109/L的中位持续时间为18(3-59)天。Lipo-MIT联合CLAG方案治疗复发/难治AML具有令人鼓舞的疗效和可控的安全性。
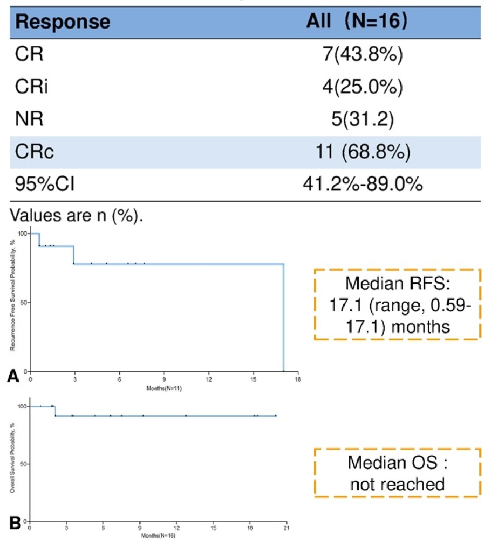
图2. 患者疗效结果
摘要号:P1823(e-Poster)
盐酸米托蒽醌脂质体联合阿糖胞苷治疗新诊断的AML患儿:药代动力学、安全性和有效性
英文题目:Combination of mitoxantrone hydrochloride liposome with cytarabine in pediatric patients with newly diagnosed AML: pharmacokinetics, safety and efficacy3
研究团队:中国医学科学院血液病医院 竺晓凡教授团队
研究内容:
该研究是一项前瞻性、单中心、药代动力学研究,旨在观察Lipo-MIT联合阿糖胞苷用于AML患儿的药代动力学(PK)特性,并初步评估其安全性和疗效。截至2024年2月20日,共分析7例患儿数据。单次静脉注射Lipo-MIT 30 mg/m2后,游离与总米托蒽醌的AUC0-t比值为1.83%±0.554%,表明Lipo-MIT输注后循环中释放的游离米托蒽醌较少,比值固定在1%-2%。总米托蒽醌的平均t1/2为60.2±9.35小时。总体而言,与单独使用Lipo-MIT相比,Lipo-MIT与阿糖胞苷联合使用时的PK特性在AML患儿中未发生改变。最常见的3/4级TRAE包括:血液学毒性(100.0%)、软组织感染(28.6%)。接受1周期和2周期治疗后的CRc率均为85.7%(6/7),在达到CRc的患儿中,流式MRD阴性率为100%(6/6),2例有髓外浸润的患儿病灶消失。Lipo-MIT具有良好的PK特性,与阿糖胞苷联合使用后未受影响,同时显示一定的疗效且安全可耐受。
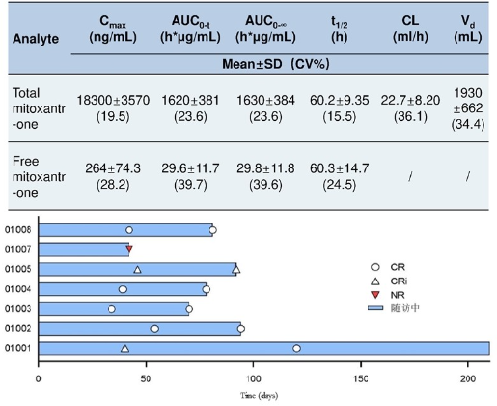
图3. 总米托蒽醌和游离米托蒽醌的PK参数结果以及患者疗效结果
摘要号:PB2460(Publication Only)
盐酸米托蒽醌脂质体联合方案治疗复发/难治急性髓系白血病的疗效和耐受性
英文题目:Efficacy and tolerability of combined regimens with mitoxantrone hydrochloride liposome for refractory and relapsed acute myeloid leukemia4
研究团队:中国医学科学院血液病医院 姜尔烈教授团队
研究内容:
该研究是一项前瞻性、单中心、探索性临床研究,纳入了20例复发/难治成人AML患者,根据患者个体化疾病特征,给予Lipo-MIT联合方案进行诱导治疗,Lipo-MIT中位给药剂量为20.00(11.17-33.75)mg/m2。既往接受过异基因造血干细胞移植(allo-HSCT)复发的患者,诱导治疗后序贯供者淋巴细胞输注(DLI)。12例(60%)患者经过一周期治疗达到CRc,13例allo-HSCT后复发的患者中,9例(69.23%)达到CRc。疗效较优方案包括MAC(Lipo-MIT+阿糖胞苷+环磷酰胺)样方案,CRc率为66.67%。中位随访6.64(1.64-19.61)个月,中位OS为9.99(95% CI,2.05-17.92)个月,中位EFS为2.18(95% CI,1.67-2.53)个月。常见3/4级TRAE包括贫血(50%)、血小板计数降低(35%)、白细胞计数降低(35%)、中性粒细胞计数降低(25%)和肺部感染(40%),无致死性感染。对于化疗后复发/难治、以及allo-HSCT后复发的AML患者,Lipo-MIT联合方案是一种安全有效的选择。
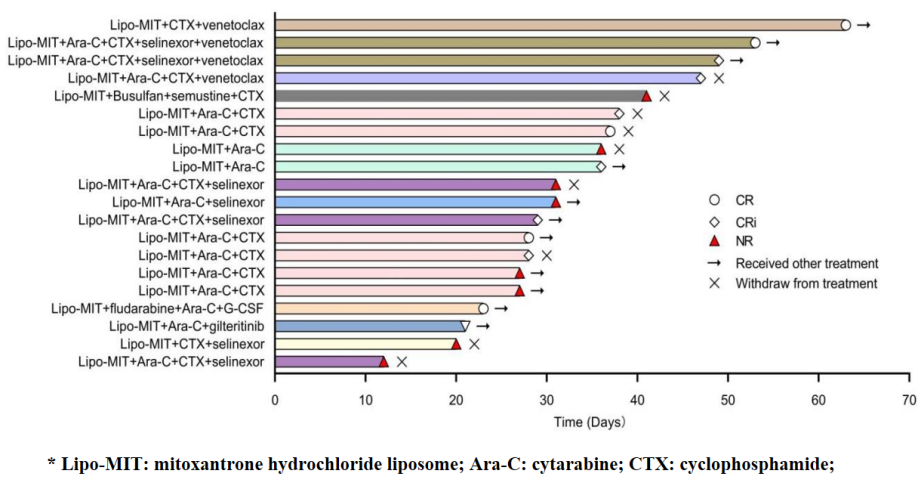
图4. 患者用药方案及疗效结果
白血病移植预处理
摘要号:P1370(Poster)
接受盐酸米托蒽醌脂质体联合白消安和氟达拉滨预处理方案行单倍体造血干细胞移植后以环磷酰胺预防GVHD的前瞻性临床研究
英文题目:A prospective study of PTCY as GVHD prophylaxis after haploidentical hematopoietic cell transplantation using liposome mitoxantrone in combination with busulfan and fludarabine conditioning5
研究团队:苏州大学附属第一医院 吴德沛教授团队
研究内容:
该研究是一项开放性、随机对照研究,纳入14至60岁拟行单倍体造血干细胞移植(haplo-HSCT)的急性白血病患者,随机1:1分配至试验组(米托蒽醌脂质体、白消安、氟达拉滨预处理联合移植后环磷酰胺[Lipo-MIT + BuFlu + PTCy])和对照组(白消安、环磷酰胺[BuCy]预处理联合预防移植物抗宿主病[GVHD]标准方案),旨在评估试验组是否能降低haplo-HSCT后GVHD发生率并改善预后。共计纳入56例患者(对照组、试验组各28例),移植后中位随访7个月,试验组和对照组累计急性GVHD发生率分别为21.42%和42.86%(p=0.086),慢性GVHD发生率分别为25%和39.29%(p=0.252)。中度和重度慢性GVHD整体发生率在试验组和对照组间有显著性差异,分别为0%和17.86%(p=0.019)。两组移植相关死亡率(7.14% vs. 14.3%,p=0.763)和不良事件发生率均没有显著性差异,但对照组EB病毒感染发生率稍高于试验组(17.86% vs. 3.57%,p=0.086)。此外,移植后累计复发率、PFS及OS均无显著性差异。Lipo-MIT + BuFlu + PTCy方案与BuCy方案具有相似的疗效,但在预防GVHD方面更优。
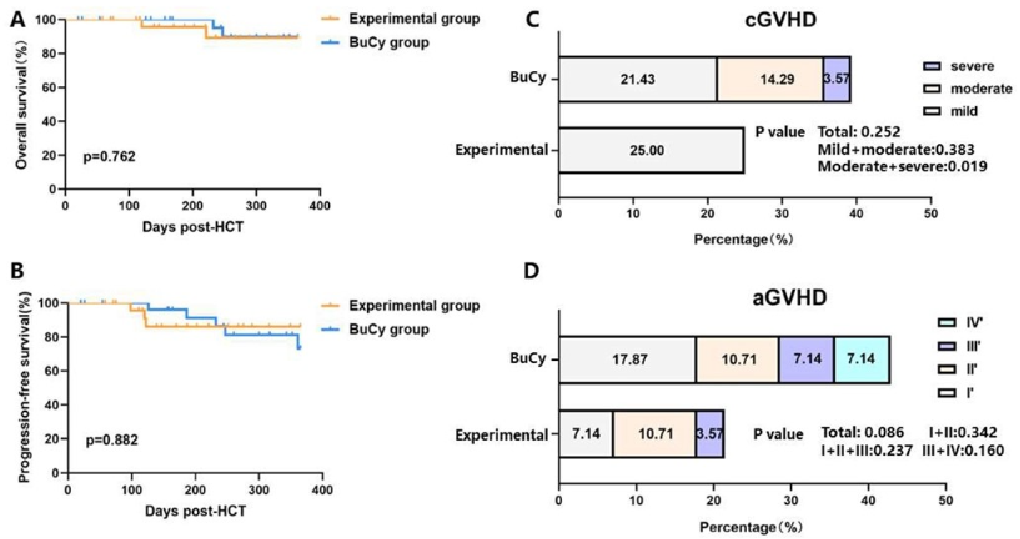
图5. 试验组和对照组的总生存期(A)、无进展生存期(B)、慢性GVHD(C)和急性GVHD(D)发生率结果
摘要号:PB3158(Publication Only)
盐酸米托蒽醌脂质体联合BUCY或氟达拉滨+BUCY用于AML和ALL患者异基因造血干细胞移植预处理的有效性和安全性
英文题目:Efficacy and safety of mitoxantrone hydrochloride liposome combined with BUCY and fludarabine+BUCY conditioning regimens for allogenetic hematopoietic stem cell transplantation in AML and ALL patients6
研究团队:深圳市第二人民医院 杜新教授团队
研究内容:
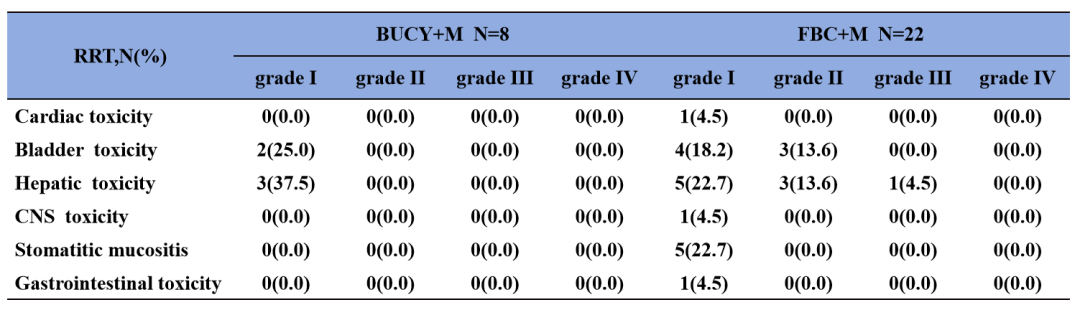
该研究回顾性分析了2023年4月至2023年12月,在该中心进行allo-HSCT并接受含Lipo-MIT预处理方案的30例急性白血病患者数据,其中AML 15例,急性淋巴细胞白血病(ALL)15例。8例行全相合移植患者接受BUCY联合Lipo-MIT(BUCY + M)预处理方案,22例行单倍体移植患者接受氟达拉滨联合BUCY + M(FBC + M)预处理方案。所有患者移植后均达到血液学完全缓解和造血重建,中性粒细胞中位植入时间为19天,血小板中位植入时间为24天。移植后28天内治疗相关毒性主要为肝脏毒性和出血性膀胱炎,大多为轻度。急性移植物抗宿主病(GVHD)发生率为26.7%(8/30),其中5例为1-2级,3例为3-4级。中位随访6.34(2.50-10.25)个月,慢性GVHD发生率为20%,均为1-2级。移植后100天内3-4级感染不良事件发生率为26.7%,其中肺部感染发生率最高(10%)。在BUCY样预处理方案中加入Lipo-MIT具有可接受的安全性,更多长期随访数据有待进一步更新。
表1. 治疗相关毒性结果
淋巴瘤
摘要号:PB3004(Publication Only)
盐酸米托蒽醌脂质体、吉西他滨、长春瑞滨联合或不联合利妥昔单抗(GVM ± R)治疗复发/难治侵袭性非霍奇金淋巴瘤
英文题目:Mitoxantrone hydrochloride liposome, gemcitabine, vinorelbine with or without rituximab (GVM±R) in patients with relapsed or refractory aggressive non-hodgkin’s lymphoma7
研究团队:中国医学科学院血液病医院 邱录贵教授团队
研究内容:
该研究是一项单臂、开放、3+3剂量递增Ⅰ期临床研究,旨在探索Lipo-MIT最大耐受剂量(MTD)和Ⅱ期推荐剂量(RP2D),并进一步评估GVM ± R方案的安全性和有效性。自2022年4月2日至2023年11月28日,共纳入18例复发/难治侵袭性非霍奇金淋巴瘤(R/R aNHL)患者。Lipo-MIT 16、18、20 mg/m2剂量组各发生1例剂量限制性毒性(DLT),均为4级中性粒细胞计数降低超过7天。截至数据统计,18例患者ORR为66.7%,完全缓解(CR)率为44.4%;其中弥漫大B细胞淋巴瘤ORR为71.4%(5/7),CR率为57.1%(4/7),NK/T细胞淋巴瘤ORR为63.6%(7/11),CR率为36.4%(4/11)。常见的3/4级TRAE主要为白细胞计数降低(94.4%)、中性粒细胞计数降低(88.9%)、血小板计数降低(72.2%)、贫血(38.9%)、淋巴细胞计数降低(38.9%)、发热性中性粒细胞减少症(16.7%)、肺炎(16.7%)和低钾血症(11.1%)。GVM ± R方案在R/R aNHL患者中显示初步疗效和可控的安全性,并确定Lipo-MIT以18 mg/m2作为RP2D开展单臂、多中心Ⅱ期临床研究。
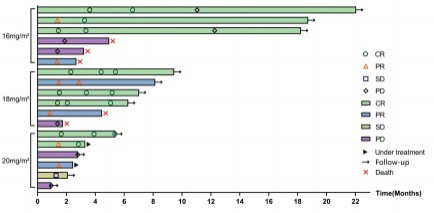
图6. 患者疗效结果
摘要号:PB3009(Publication Only)
盐酸米托蒽醌脂质体联合环磷酰胺、长春新碱、依托泊苷和泼尼松(CMOEP)治疗初治外周T细胞淋巴瘤的Ⅰ期临床研究
英文题目:Combination of mitoxantrone hydrochloride liposome with cyclophosphamide, vincristine, etoposide and prednisone (CMOEP) in treatment-naive patients with peripheral T-cell lymphoma: a phase one study8
研究团队:天津医科大学肿瘤医院 张会来教授团队
研究内容:
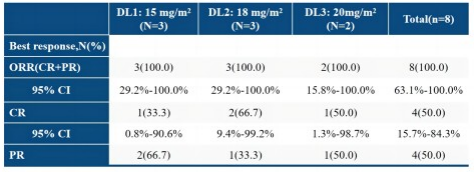
该研究为前瞻性、单臂、多中心、Ⅰ期临床研究,旨在探索CMOEP治疗初治外周T细胞淋巴瘤(PTCL)中米托蒽醌脂质体的剂量限制性毒性(DLT)以及联合方案的最大耐受剂量(MTD),并初步评估CMOEP方案的安全性和有效性。截至2024年2月7日,共纳入11例不同亚型PTCL患者,其中Lipo-MIT 15 mg/m2组3例、18 mg/m2组5例、20 mg/m2组3例,均未发生DLT。截至数据统计,8例患者具有至少一次疗效评估结果,整体ORR为100%,CR率为50%。常见的3/4级TRAE主要为白细胞计数降低(63.6%)、中性粒细胞计数降低(54.5%)、淋巴细胞计数降低(36.4%)和贫血(18.2%)。CMOEP方案在初治PTCL患者中显示初步疗效和可控安全性。
表2. 患者疗效结果
摘要号:PB3011(Publication Only)
含盐酸米托蒽醌脂质体联合方案用于复发/难治NK/T细胞淋巴瘤的有效性及安全性
英文题目:Efficacy and safety analysis of combination therapy based on mitoxantrone hydrochloride liposome injection in relapsed/refractory NK/T-cell lymphoma9
研究团队:北京同仁医院 王亮教授团队
研究内容:
该回顾性研究纳入12例既往接受过含培门冬酶方案治疗的复发/难治NK/T细胞淋巴瘤(NK/TCL)患者,其中11例疾病分期为Ⅳ期,5例末线难治。经含Lipo-MIT联合方案治疗后:5例(41.7%)患者达CR,5例(41.7%)患者达部分缓解(PR),1例(8.3%)患者疾病稳定(SD),1例(8.3%)患者疾病进展(PD)。中位随访4(2-14)个月,中位PFS为5个月,中位OS为7个月。9例患者发生≥3级骨髓抑制,中位恢复时间为14(2-35)天。另外,5例患者发生皮肤蓝染,但未显示皮肤蓝染与治疗疗效间具有相关性。基于Lipo-MIT联合方案治疗复发/难治NK/TCL显示较高缓解率,同时Lipo-MIT具有一定骨髓抑制毒性,在联合细胞毒性药物治疗时应给予积极的支持治疗。
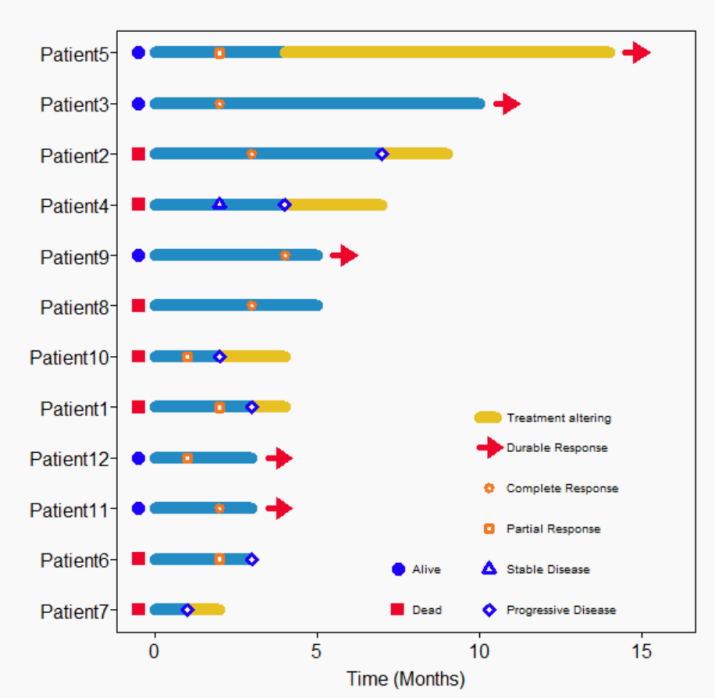
图7. 患者疗效结果
摘要号:PB3027(Publication Only)
环磷酰胺、盐酸米托蒽醌脂质体、长春新碱和泼尼松联合或不联合利妥昔单抗(CMOP ± R)一线治疗非霍奇金淋巴瘤
英文题目:Cyclophosphamide, mitoxantrone hydrochloride liposome, vincristine, and prednisone regime with or without rituximab (CMOP±R) shows high efficacy as a first-line treatment for non-hodgkin’s lymphoma10
研究团队:苏州大学附属第一医院弘慈血液病医院 黄海雯教授团队
研究内容:
该研究为单臂、多中心、Ⅱ期临床研究,旨在评估以盐酸米托蒽醌脂质体为基础的CMOP ± R方案治疗初治非霍奇金淋巴瘤(NHL)的有效性和安全性。自2022年11月至2024年1月,共纳入33例初治NHL患者,其中30例疾病分期为Ⅲ-Ⅳ期,18例IPI评分≥3分。截至数据统计,22例符合疗效评估标准,中位随访时间6.6(0.3-13)个月,ORR为90.9%(20/22),CR率为77.3%(17/22)。亚组分析显示,在晚期(IPI评分3-5)患者中显示较高的ORR(90.9%)和CR率(90.9%)。最常见的3/4级TRAE为血液学毒性,包括白细胞计数降低(33.3%)、中性粒细胞计数降低(36.4%)和淋巴细胞计数降低(48.5%),治疗期间无心脏相关不良事件发生。CMOP ± R方案一线治疗NHL显示良好疗效,特别针对晚期患者不良反应可控。
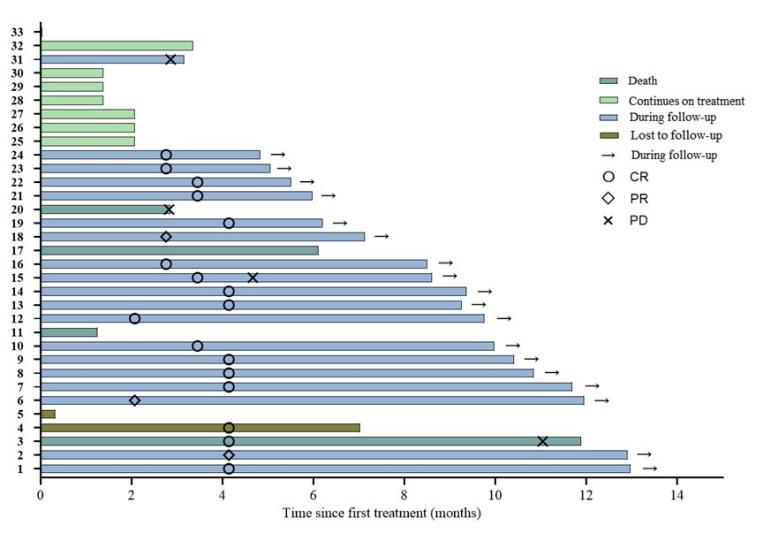
图8. 患者疗效结果
小结
米托蒽醌脂质体作为全球首个米托蒽醌纳米剂型药物,其稳定性增加,血液循环时间延长,活性成分能够有效地在肿瘤组织富集。目前已有多项临床研究成果显示米托蒽醌脂质体在淋巴瘤、白血病以及多发性骨髓瘤等领域具有良好的疗效和安全性,此次会议为其在血液领域的临床应用再添力证。此外,米托蒽醌脂质体的更多临床研究仍在继续开展,期待为广大肿瘤患者带来更多治疗希望。
参考文献
1. Jun Ma, et al. 2024 EHA P602.
2. Xi Zhang, et al. 2024 EHA P1749.
3. Xiaofan Zhu, et al. 2024 EHA P1823.
4. Erlie Jiang, et al. 2024 EHA PB2460.
5. Depei Wu, et al. 2024 EHA P1370.
6. Xin Du, et al. 2024 EHA PB3158.
7. Lugui Qiu, et al. 2024 EHA PB3004.
8. Huilai Zhang, et al. 2024 EHA PB3009.
9. Liang Wang, et al. 2024 EHA PB3011.
10. Haiwen Huang, et al. 2024 EHA PB3027.


