医美闻所未闻:盘点最新出现的肉毒毒素注射并发症
时间:2024-07-15 16:02:06 热度:37.1℃ 作者:网络
Hey guys,A型肉毒毒素(BoNTA)和软组织填充剂是世界上最常见的美容手术。它们执行迅速,并提供可预测和持久的结果。虽然这些注射治疗相对安全,但可能会出现并发症。一项大型回顾性队列研究的数据显示,肉毒毒素治疗的总体并发症发生率为0.065%,透明质酸(HA)填充剂注射为0.106%,羟基磷灰石钙治疗为0.205%,这与早期的填充剂并发症发生率报告一致(<1.25%)。
已被发现肉毒毒素注射在上面部的并发症包括眉毛和眼睑下垂、复视、眼睑外翻、眼睑退缩、口干和不对称(例如“Spock”眉毛)。肉毒毒素在中面部并发症包括嘴唇不对称、下垂和面部表情的不必要变化。下面部和颈部的肉毒毒素并发症包括颞下颌关节功能改变,咬肌肥大治疗后咀嚼力降低,颈纹(横纹)和颈索治疗后声音嘶哑、吞咽困难和颈部无力。

图:Spock眉
填充剂并发症可根据其性质(缺血性、非缺血性)或病因/发病机制分为出血相关、过敏/超敏反应相关、肉芽肿性和免疫介导、感染性/炎症性、血管栓塞性和不适当的技术相关(过度矫正、移行和错位)。虽然这些并发症得到了很好的研究,但其他并发症也可能偶尔发生。本报告总结了一些尚未报告或很少报告的内容,试图阐明潜在的机制和可能的治疗方法。
肉毒并发症
肉毒中毒
2024年4月,美国疾病控制与预防中心(CDC)发布警报警告称,22名女性因未经许可或未经培训的个人在非医疗机构(如家庭或水疗中心)进行的假冒肉毒毒素注射或美容注射而产生不良影响。11名女性住院,6名女性因肉毒毒素病接受肉毒毒素抗毒素治疗。报告的症状包括疲劳、虚弱、模糊和复视、眼睑下垂、吞咽困难、口齿不清和呼吸困难。这不是官方当局第一次警告不要在美国使用未经许可的肉毒毒素制剂。2004年11月,CDC报告了四名与美容肉毒毒素注射有关的疑似肉毒毒素中毒患者。由于美国食品药品监督管理局(FDA)之前的研究没有揭示医美目的使用肉毒毒素后肉毒毒素中毒的病例,因此任何怀疑在处于医美目的使用该产品后肉毒毒素感染的病例都应该引起对所用产品合格性的质疑。
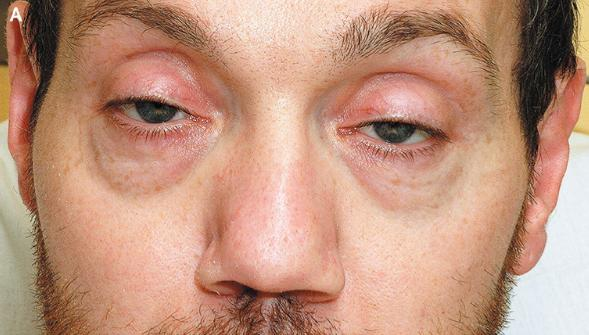
图:肉毒毒素中毒
硬皮病样病变
一份报告详细描述了在额肌注射肉毒毒素后出现的三例硬皮病样病变。15病变为前额萎缩性凹陷(图1)。发生时间为肉毒毒素注射后1-3周。病变最早在发生后两周内自行消退,最晚在发生后三个月内自行消退。肉毒毒素注射治疗偏头痛后,眉间注射部位也出现了类似的病变。肉毒毒素由于短暂缺乏神经刺激(神经源性萎缩),很少会引起表情肌肉的意外局灶性萎缩。作为对这一现象的另一种解释,他们提出了萎缩性斑块可能是由组织对硅油的反应引起的,硅油几乎是每个塑料注射器中的润滑剂。肉毒毒素注射过程中润滑剂的错位可能与导致萎缩的皮肤反应有关,但缺乏支持性研究。
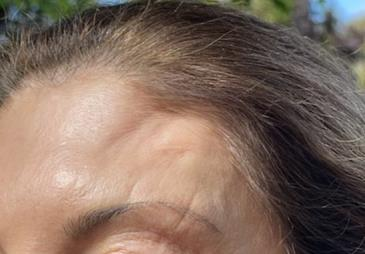
图1
注射后结节
(IMCAS)Alert在线并发症平台最近报道了注射后结节注射后肿块。这些肿块发生在不同的世界范围内批准的肉毒毒素中,这些肉毒毒素用市售生理盐水溶液重建。根据作者之一(FRL)的经验,这些结节主要出现在注射后约24小时的前额,其位置与注射部位相关。它们可能出现在早期顺利注射相同产品的患者身上。大多数情况下,结节会持续几天并自行消退。在某些情况下,局部使用类固醇。当使用相同的肉毒毒素几个月后消退时,一些患者的病程完全恢复。
虽然这种现象的发病机制尚不清楚,但有三份关于肉毒毒素过敏反应的报告,表现为荨麻疹性丘疹,类似于注射部位出现的肉毒毒素后结节,有或没有全身过敏反应。两名患者注射了中国肉毒毒素,皮内试验呈阳性。在这些情况下,产品中的明胶被怀疑是过敏的原因。
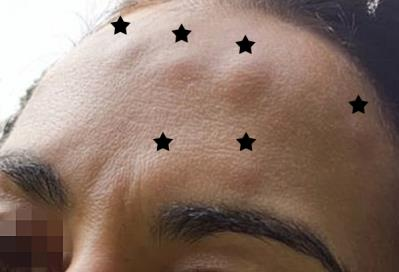
图2:注射后3-4天出现的结节,7-10天后消失
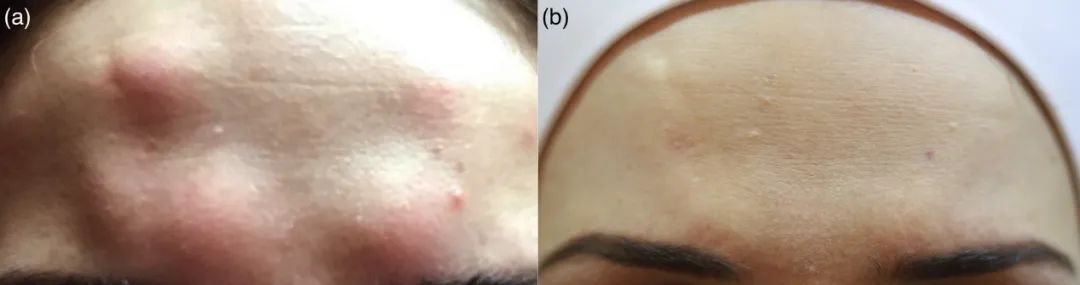
已知有三个病例与注射onabotulinumtoxin(Botox®,Allergan美学)两到三周后出现的发痒的红色结节惊人相似。虽然其中一名患者是第一次注射肉毒毒素,但其他两名患者之前注射过同样的产品,没有出现过问题。其中两名患者接受了局部制剂抗生素和类固醇治疗,一名患者接受全身类固醇和抗生素治疗。在所有病例中,结节在两周后几乎完全消失,局部治疗和全身治疗的患者的临床病程没有差异。所有患者随后都注射了肉毒毒素,没有任何进一步的并发症。
报告了5例肉毒毒素注射后出现的经组织学证实的肉芽肿病例。它们包括化脓性肉芽肿、肌样肉芽肿和异物肉芽肿。在这些病例中,在治疗后两天至六年内,肉毒毒素注射的确切位置出现了病变,但病程更长。一组人在前臂注射Botox®后再现了类肉芽肿病,但无法用盐水注射再现。这使他们认为这是Kveim反应,而不是结节病的再激活。根据这些数据,肉毒毒素注射后的肿块似乎代表了一种异质性实体。虽然有些病例可能是由亚临床肉芽肿性疾病引起的,并且预计会更持久,但大多数病例表现为荨麻疹样现象,临床病程短,不需要任何特定治疗。发病机制尚不清楚,但这些患者可能可以安全地再次注射相同的产品。
非结核分枝杆菌感染
肉毒毒素注射后对7例非结核分枝菌感染患者进行了回顾性研究。临床表现为多发红色丘疹、结节和脓肿的患者。在5例病例中,皮肤组织培养对脓肿分枝杆菌呈阳性。症状持续10天至5个月,直到诊断和治疗。脓肿分枝杆菌是最具耐药性的分枝杆菌菌株;因此,当产生阳性培养物时,必须对其进行药物敏感性测试。建议同时使用两种抗菌药物,因为单一药物会引起耐药性。
血管栓塞
报道了一例肉毒毒素注射液引起的血管栓塞。患者通过30号注射器将肉毒毒素注射到眉间复合体中。注射后,患者回忆起左中央前额突然出现短暂不适。随后,在72小时内,她注意到左侧中央前额的皮肤逐渐变色和压痛。注射后第3天的皮肤检查显示左滑车上远端区域有活体变化。诊断为动脉栓塞引起的前额中央缺血性损伤,患者完成了三次高压氧治疗,反应良好。作者建议通过注射一种非特定物质来阻断动脉,作为一种范式的微观转变。他们认为,栓子是由皮肤组织的微血管形成的,这些微血管被针头捕获,并在下一次注射时形成动脉内栓子。他们成功地在实验系统中复制了这些尺寸为100-300微米的微粒。
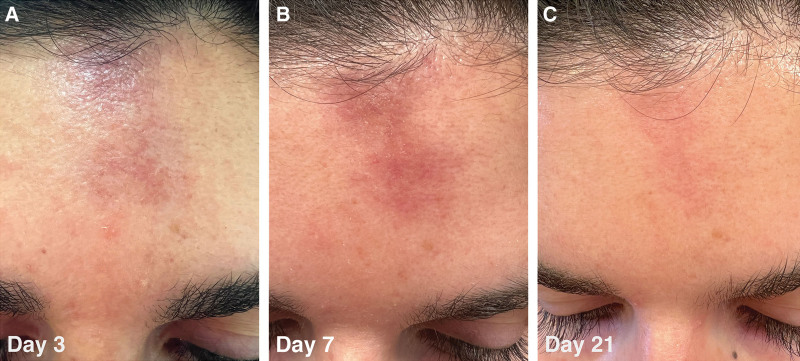
图:肉毒毒素注射后栓塞
2018年发表了一例咬肌注射肉毒毒素后急性视力丧失的病例。在这种情况下,患者在注射后4小时报告右眼视力丧失。右眼的视力下降到20/800。作者提出了两种可能的机制:由神经毒素和内皮细胞之间的相互作用引起的肉毒毒素诱导的促血栓作用和血管壁损伤诱导的血栓形成。他们认为,在针头嵌入动脉腔的情况下,对注射器柱塞施加高压可能会对血管壁造成损伤。损伤引起的栓子可能从咬肌周围的动脉分支逆行至视网膜中央动脉,导致疼痛的视力突然模糊。尽管未经科学证实,但作者认为,在肉毒毒素重建过程中,小瓶塞子中的小橡胶片可能会栓塞并释放到产品溶液中。这一担忧最初是在2008年根据以往麻醉药物的经验提出的。
颞浅动脉假性动脉瘤
已经报道了两例在肉毒毒素注射后2个月和6个月出现的颞浅动脉(STA)假性动脉瘤。病变为肿块,出现在肉毒毒素注射部位。与任何穿透性损伤一样,肉毒毒素注射会损伤血管并产生假动脉瘤。动脉瘤发生在颞上线,因为前动脉分支未被肌肉间隙覆盖,直接位于骨膜上。外膜还将动脉束缚在额肌和颞肌上。所有这些解剖特征都增加了钝性创伤形成假性动脉瘤的风险。
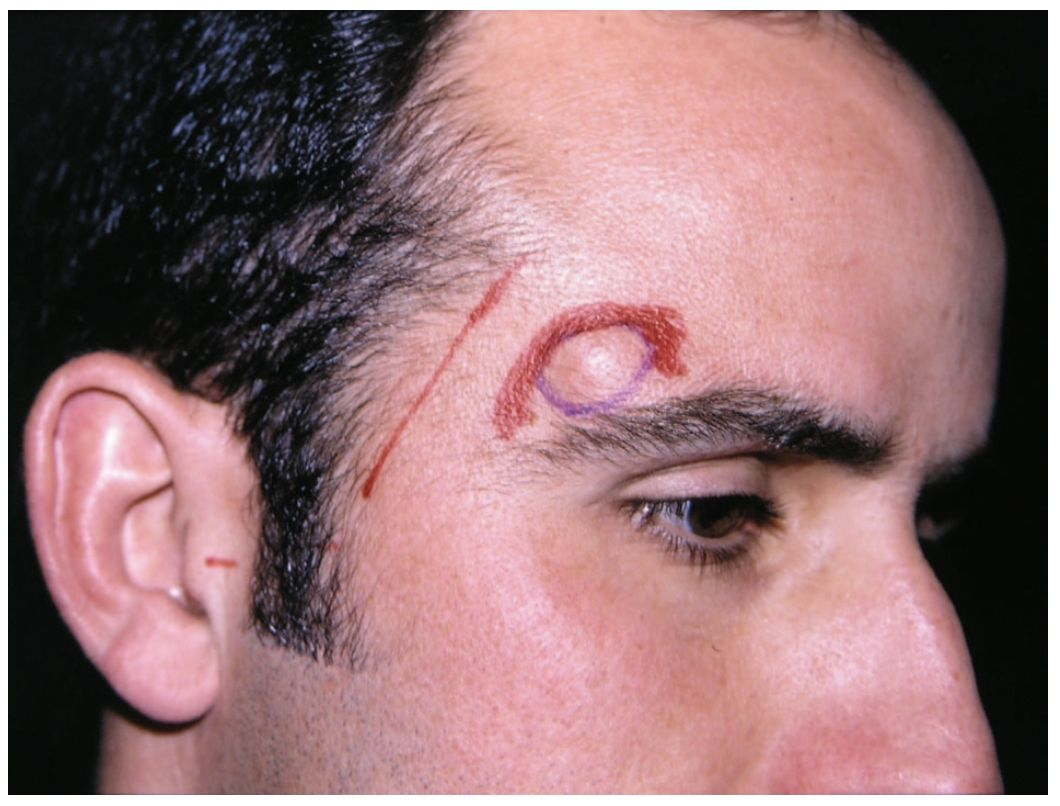
图:肉毒毒素注射后,假性动脉瘤
填充剂并发症
非持续性脱发
填充剂注射后脱发是一种最新报道的后太阳穴提拉术后真皮填充剂并发症(图3)。这项技术的目标是通过使用22G钝针将高G值填充剂注射到后上太阳穴的真皮下平面来进行面中部提升。通过增加这种紧密的浅表隔室中的张力,面部中部和下部的软组织得到提升;然而,位于该隔室中的颞浅动脉中的血流可能会受到损害。2019年前发表了6例继发于填充剂注射的脱发病例。最近还报道了6例非持续性脱发病例,这些病例是在使用临时提拉技术进行填充剂注射后发生的。患者在注射填充剂后数小时内出现头皮疼痛。填充剂注射后9天至3周开始出现明显的脱发,形成持久的非持续性脱发。不幸的是,快速注射高剂量透明质酸并不能预防脱发。血管栓塞,即使是短暂的栓塞,也会突然中断毛囊的重要血液供应,并导致生长期突然终止,从而引发生长期脱发。然后,营养不良的退行性毛囊会随着快速脱落而形成,如毛发镜检查所示。因为这种并发症可以通过最少量的填充剂(0.5毫升)引起,而不能通过及时注射高剂量的透明质酸酶来解决,作者建议避免使用后太阳穴提拉技术。
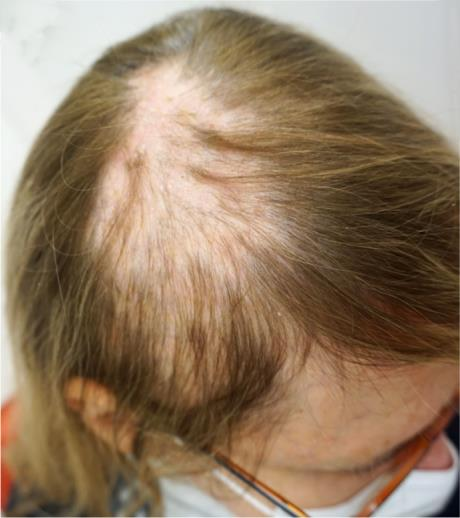
图3
口腔内坏死
组织坏死很少出现在舌头、牙龈和嘴唇上。发表了4例HA增强下巴后血管并发症引起的舌头坏死病例。Thanasarnaksorn等人报道的单侧舌头坏死病例中,使用27号锐针在下颌骨最下部上方的中线注射肉毒毒素。颏下动脉变异已被描述为该并发症的原因。提出的咬合的病理生理学包括血管系统和中线舌孔的变化,这是下颌中线表面的解剖骨骼变化。该孔包含颏下和舌下动脉的一个分支,该分支包括穿通动脉、正中穿通动脉或两者。用锋利的针头在骨头上注射填充剂可能会增加这种血管事件的风险。高剂量的透明质酸酶使患者完全康复。
应采用使用钝钝针、低压注射和负面缺点的预防性注射技术。有一例患者因注射HA填充剂以增强下巴而导致舌动脉栓塞。她几乎立即感到不适,舌头和下巴右侧麻木和剧烈疼痛。填充剂注射后18小时,患者出现发音困难、口腔张开受限和舌头右侧苍白。血管造影显示,舌深动脉远端缺失,舌右侧前部显示延迟。颏下动脉栓塞被认为会导致舌头坏死。舌缺血可能是由于将HA意外注射到颏下动脉或其分支后,栓子通过颏下、舌下和舌深动脉之间的丰富吻合流入舌动脉分支。
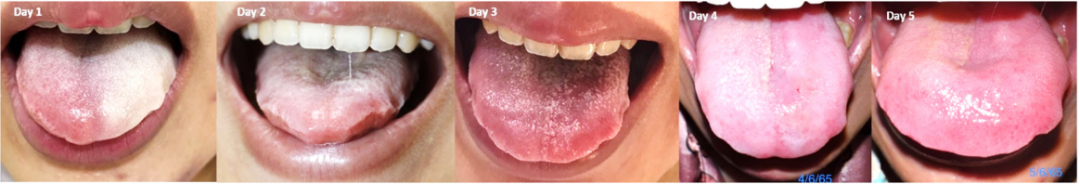
鼻唇折叠处注射填充剂后出现口内坏死。注射过程中,患者在注射部位周围出现剧烈疼痛,从右侧面部到眼睛和口腔内疼痛加剧。第二天,患者出现复视和右眼视力变化。临床检查显示,注射部位周围口腔外皮肤坏死,腭粘膜严重发炎并溃疡,组织坏死从中切牙延伸到右臼齿并接近中线。作者认为,填充材料在眶下动脉中的栓塞可能导致了其栓塞,随后影响了上颌动脉的相邻动脉分支(腭大动脉和蝶腭动脉)。
医疗旅游框架下的非结核分枝杆菌感染
医疗旅游在全球范围内急剧增加,人们从发达国家前往低收入或中等收入国家,以避免在原籍国进行高昂的手术费用。感染性并发症是外科美容游客中最常见的并发症,其中非结核分枝杆菌,如脓肿分枝杆菌,是最常见的病原体之一。手术干预与延长(长达22个月)的抗生素治疗相结合,通常涉及大环内酯类药物,如克拉霉素或阿奇霉素,对于脓肿分枝杆菌相关美容手术感染的康复通常是必要的。
中国有一份关于注射HA后脓肿分枝杆菌感染的报告。患者在未经授权的私人诊所接受了含有“HA和表皮生长因子混合制剂”的产品注射。病变发生在注射后7天,表现为双颊多发红斑、非压痛结节。作者认为,感染源可能是未经批准的美容药物或未经适当消毒的外部环境和医疗设备。这个病人接受了七个多月的治疗。其中一位作者(ML)最近在土耳其的医疗旅游中遇到了一例脓肿分枝杆菌感染病例,该病例发生在一名患者注射HA填充剂后。51与此同时,她的丈夫在同一机构接受了头发移植手术。注射后四天,当她回到家时,病变就出现了。他们在两个脸颊上出现多个牢固的结节(图4)。她接受了两个月的静脉联合抗生素治疗,然后注射重建了剩余的美容缺陷。
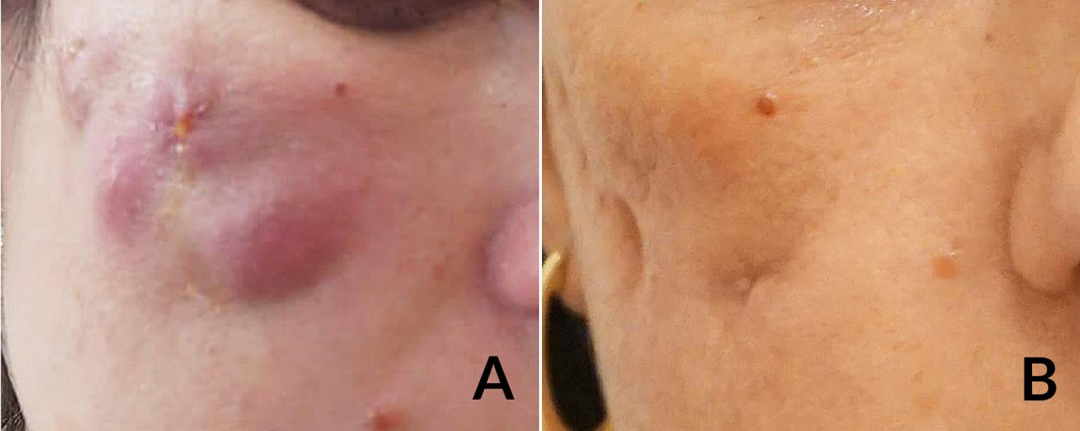
图4
可卡因成瘾者面部骨骼破坏引起的难治性填充剂感染
可卡因引起的中线破坏性病变是可卡因吹入的罕见后果,涉及鼻子、鼻窦,偶尔还涉及腭。所涉及的机制包括可卡因的血管收缩和腐蚀作用,导致鼻骨和腭骨缺血和坏死,从而导致口鼻穿孔,并在这些空间与其他面部空间(如鼻窦)之间持续沟通。其中一位作者(ML)最近治疗了一名患者,该患者右上颧骨区域HA填充剂持续炎症,对任何治疗都有耐药性,包括全身抗生素(图5)。诊断为可卡因引起的腭穿孔,患者接受了大型重建手术,之后面中部炎症消退。据我们所知,这是第一篇关于可卡因诱导的腭穿孔继发的皮肤填充剂持续炎症的报道。
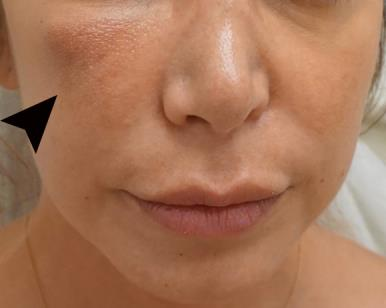
图5
当遇到对治疗有抵抗力的真皮填充剂的延迟炎症反应时,临床医生必须意识到这种可能性。填充剂仓库附近的任何侵入性面部或口腔手术都可能引发填充剂材料的感染性并发症。虽然这种手术(牙科治疗)是间歇性进行的,可以通过预防性抗生素进行控制,但在口腔与其他面部空间持续连接的情况下,存在持续暴露于口腔病原体的情况,抗生素治疗可能无效。
黄瘤样病变(XLR)
在泪沟矫正术中注射填充剂后,下眼睑出现XLR的病例越来越多。XLR是第三种最常见的延迟并发症,当注射泪沟区域时,通常在注射后约十个月出现。一项研究详细介绍了七名女性在注射填充剂后下眼睑出现XLR。无黄原瘤病史。填充剂包括HA(2例患者)、羟基磷灰石钙(4例患者)和聚己内酯微球(1例患者)。填充剂注射和XLR发育之间的平均时间间隔为12个月(6-18个月)。一组报告了一名泪沟注射聚甲基丙烯酸甲酯胶原后XLR患者。经透明质酸、类固醇注射、5-氟尿嘧啶注射、消融或分级CO2激光和直接切除治疗后,结果令人满意。
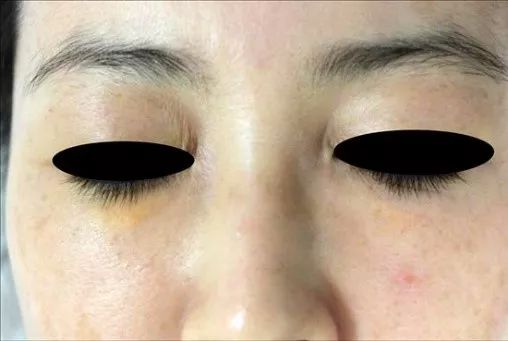
图:黄瘤样反应
这种现象被称为XLR,因为活检通常不能显示典型的病理学。所有报告的病变仅出现在下眼睑,而非填充剂相关的黄瘤最好影响上眼睑。血脂正常的黄瘤的主要机制包括眨眼造成的持续创伤,导致毛细血管受压,从而导致血浆内容物(包括胆固醇)渗出。在XLR的情况下,HA可以结合细胞外基质中外渗的LDL,形成被巨噬细胞吸收的体外复合物,并在黄瘤的形成中发挥作用。另一种解释是,填充剂注射过程中的组织创伤会引起炎症,这可能在黄瘤发病机制中起作用。最后,据报道,一些XLR病例使用羟基磷灰石钙注射,可导致类似黄瘤的组织出现白色染色。由于羟基磷灰石钙填充剂和透明质酸填充剂的混合被广泛应用,特别是在泪沟区域,以降低丁达尔效应的风险,一些据称由HA诱导的XLR病例可能与混合物中的羟基磷灰石钙有关,从而导致拟黄瘤。
颅内穿孔
当使用垂直于骨注射技术(“枪声”技术)的针头辅助注射时,颞区存在颅内穿透的潜在风险。作者建议使用温和的注射方法,使其能够接触骨膜,而不会对骨施加过大压力。在一名患者中发现了窦扩张性。该病变是前额上一种不规则的、坚硬的、非漏斗状的增厚,是在患者在该区域进行非永久性填充剂美容手术四年后形成的。作者认为,可能发生了骨外层皮质的穿透和/或感染,这可能导致这种病变的单向阀阻塞(球阀)机制。结论随着其日益普及和使用,肉毒毒素和填充剂注射很少与严重并发症有关。作者收集了尚未报告或很少报告的并发症。这里讨论的并发症对治疗提供者来说是一个诊断和治疗挑战,因为大多数并发症不包括在常见和众所周知的传统并发症列表中。
参考文献
1. Landau M, Klein J, Leizgold FR, Kroumpouzos G. RARE AND NOVEL COMPLICATIONS OF BOTULINUM NEUROTOXIN TYPE A AND DERMAL FILLER INJECTIONS. Clin Dermatol. 2024 Jun 22:S0738-081X(24)00107-X. doi: 10.1016/j.clindermatol.2024.06.023. Epub ahead of print. PMID: 38914174.


