Front Microbiol:华山医院揭示特定肠道菌群对牙周病的潜在影响
时间:2024-08-28 13:01:16 热度:37.1℃ 作者:网络
牙周病(PD)是一个全球性的健康问题,包括两大类:牙龈炎和牙周炎。牙龈出血是这两种情况的常见临床表现。牙龈炎是PD的初始阶段,是可逆的。然而,当牙龈炎发展为牙周炎时,疾病会导致牙齿周围支撑组织的不可逆破坏,增加骨质流失和牙齿脱落的风险。轻度牙周炎的患病率影响了全世界约20-50%的成年人,而严重牙周炎的患病率约为10%,是成人牙齿脱落的主要原因。鉴于其多因素性质,PD不仅与微生物感染有关,还与糖尿病、心血管疾病、代谢紊乱、肥胖、类风湿关节炎、某些癌症、呼吸系统疾病和认知障碍(包括阿尔茨海默病)有关。为了减轻PD的发病和进展,研究人员已经探索了非手术和抗生素替代方案。最近,新的研究途径涉及通过干扰肠-口轴来抑制PD进展及其危险因素。

肠道菌群控制着宿主的肠道代谢和局部/全身免疫,在健康中起着至关重要的作用。Papageorgiou等人建立了炎症性肠病(IBD)和牙周炎之间的联系,揭示了这些疾病可以相互作用,导致易感个体的慢性炎症和组织损伤。这两种疾病都涉及异常的免疫反应和生态失调。几项关于肠道微生物群在牙周病中的作用的研究显示了四个关键因素。在免疫系统相互作用方面,肠道微生物群调节宿主肠道代谢物和调节局部/全身免疫,从而影响破骨细胞发生和骨骼发育。根据微生物易位的研究,肠道细菌或其代谢物可能通过血液途径转运到口腔,促进PD的发展或恶化。越来越多的证据表明,肠道微生物群紊乱可能导致不同程度的牙周炎。在炎症和全身影响方面,慢性炎症是牙周和肠道疾病的共同特征,可能导致全身健康问题。动物模型已经证实,肠道生态失调会损害肠道屏障功能,破坏口腔微生物群,并通过Th17/Treg失衡加剧牙周炎诱导的骨吸收。动物研究和组学分析表明牙龈炎和牙周炎与肠道微生物群变化有关。
关于益生菌和益生元,研究人员正在探索益生菌和益生元的潜在用途,以调节肠道微生物群,并间接影响牙周健康。然而,这些观察结果主要来自观察性横断面研究和病例对照研究,无法确定因果关系。孟德尔随机化(MR)利用遗传单核苷酸多态性(snp)固有的自然随机化作为工具变量(IVs)来仔细检查观察数据并揭示结果中的因果关系。随着高通量基因组技术和基因组侧关联研究(GWAS)加深了我们对疾病的理解,利用遗传数据进行广泛的表型研究变得越来越可行,这种能力可以用于群体规模的人类微生物组数据。因此,本研究的主要目的是探讨特定肠道菌群与PD之间的因果关系。目的是发现新的生物标志物,确定PD治疗的潜在有效临床途径,并为未来大规模前瞻性队列研究提供证据。
方法:在本研究中,我们采用双样本双向孟德尔随机(MR)方法研究特定肠道微生物群与牙周病(PD)和牙龈出血(BG)发展之间的因果关系,同时探索牙周健康与肠道微环境之间的相互作用。我们对两个队列进行了全基因组关联研究(GWAS),共有346,731名(PD和对照组)和461,113名(BG和对照组)参与者,以及14,306名参与者的肠道菌群GWAS数据,包括148个特征(31个家族和117个属)。使用三种MR方法评估因果关系,以逆方差加权(IVW)测量作为主要结果。采用Cochrane’s Q检验、MR-Egger检验和MR-PRESSO全局检验检测异质性和多效性。采用留一法检验MR结果的稳定性。仪器暴露相关的f统计量大于10被接受。
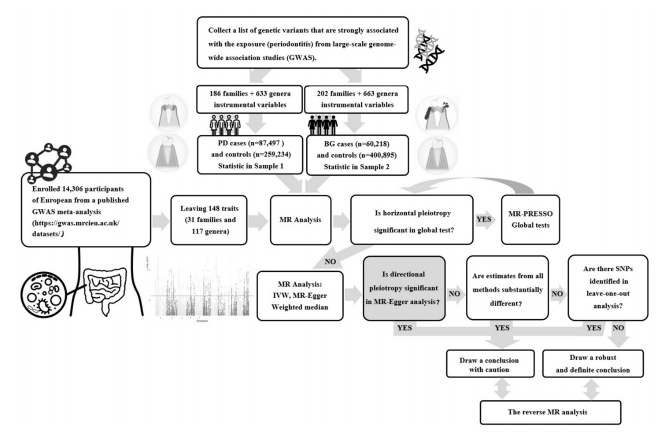
双样本双向孟德尔随机化(MR)研究流程图
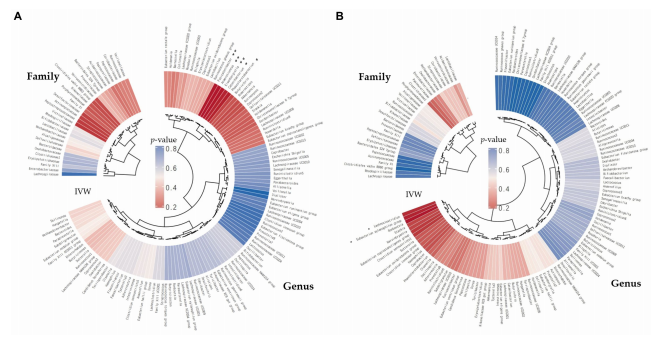
逆方差加权(IVW)分析涉及肠道微生物家族/属与牙周病(PD)风险(A)和牙龈出血(BG)风险(B)之间的关系。同心圆表示IVW分析,最里面的圆圈代表生物学分类。肠道微生物群的分类是在科和属水平上提出的。圆圈内不同深浅的颜色对应于p值的大小,如圆圈内的标签所示(**p < 0.01, *p < 0.05)。
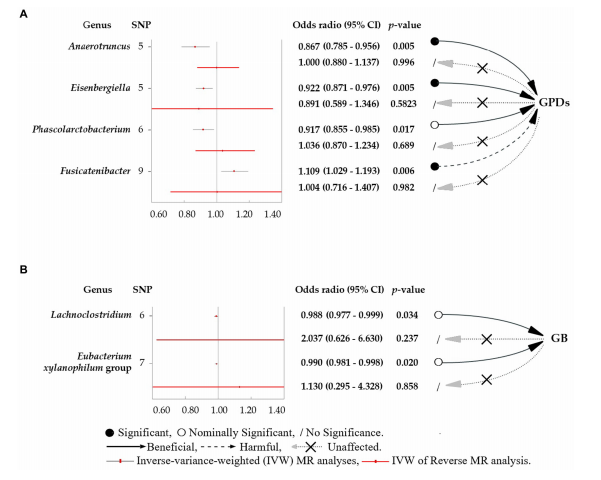
以反方差加权(IVW)分析估算值为特征的森林图。(A)不同肠道微生物属丰度水平snp对牙龈炎和牙周病(PD)的影响。(B)不同肠道微生物属丰度水平对出血牙龈(BG)的snp影响。图中的红点表示IVW估计值,而黑色和红色条表示IVW估计值的相应95%置信区间(ci)。比值比(OR) > 1为危险因素,OR < 1为保护因素。
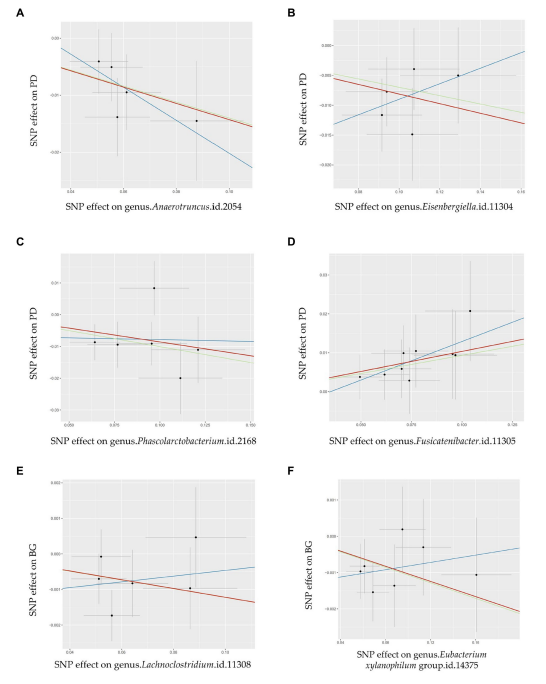
散点图显示6种肠道微生物的显著因果关系及其对牙周病(PD)或牙龈出血(BG)风险的影响的孟德尔随机化(MR)估计。在子图(A-D)中,我们探讨了4种肠道微生物属对PD的因果关系,而子图(E,F)分析了另外2种肠道微生物属对BG的因果关系。在这些图中,向上倾斜的对角线表示正相关,表明肠道微生物属对PD的促进作用。相反,向下倾斜的对角线表示负相关,表明肠道微生物群对PD或BG的抑制作用。每个图中的水平线和垂直线表示每种相关性的95%置信区间(CI)。反方差加权(IVW),加权中位数(WM), MR-Egger。
结果和结论:具体来说,嗜木真杆菌和Lachnoclostridium与降低牙龈出血风险相关,而Anaerotruncus、Eisenbergiella和Phascolarctobacterium与降低PD风险相关。相反,Fusicatenibacter与PD的风险升高有关。没有发现明显的异质性或多效性。总之,我们的MR分析确定了与PD有因果关系的特定肠道菌群,为口腔健康干预提供了潜在的途径。
原始出处:
Meng, Xu; Qiang, Shao; Yinglu, Zhou;Potential effects of specific gut microbiota on periodontal disease: a two-sample bidirectional Mendelian randomization study.Front Microbiol 2024;15(0):1322947


