【论肿道麻】NEJM:MIND饮食预防老年人认知功能衰退的临床试验
时间:2024-11-08 06:03:18 热度:37.1℃ 作者:网络
2024年1月,《美国新闻与世界报道》发布了2024年度最佳饮食榜单,榜单邀请了饮食、营养、肥胖、饮食心理学、糖尿病和心脏病学家等专业从业者组成评审团,对近40种饮食模式进行评比,结果“地中海饮食模式”稳居榜首,第二名为“DASH饮食”,第三名为“MIND饮食”。MIND 饮食是地中海饮食和DASH 饮食(预防高血压的饮食方法)的结合。MIND饮食特别纳入了被认为与降低痴呆风险有关的食物。它包括菠菜、羽衣甘蓝、油麦菜等绿叶蔬菜以及其他蔬菜。它推荐全谷物、橄榄油、家禽肉、鱼、豆类和坚果。它优先选择浆果而不是其他水果,并建议每周吃一份或更多份鱼。有关饮食为目标的生活方式干预的大多数临床试验主要是针对心血管健康进行的,饮食干预对大脑健康的试验数据有限。2024年7月,来自芝加哥拉什大学(Rush University,RUSH)阿尔茨海默病研究中心的Lisa L. Barnes团队在《新英格兰医学杂志》(New England Journal of Medicine)上发表的一篇题为“ MIND 饮食预防老年人认知能力下降的试验”(Trial of the MIND Diet for Prevention of Cognitive Decline in Older Persons),比较了轻度热量限制的MIND饮食与轻度热量限制的对照饮食,以评估3年饮食干预对因家族史而有痴呆风险的老年认知功能未受损成人的认知能力下降、痴呆和阿尔茨海默病脑成像标志物的影响,以评价MIND饮食改善认知和大脑健康,作为预防认知能力下降和阿尔茨海默病的潜在保护措施。研究的结论是与轻度热量限制的对照饮食组相比,MIND 饮食并没有显著的认知改善。

方法
试验设计与监督
在这项为期3年的双中心随机对照试验中,受试者被随机分配至遵循减轻体重轻度热量限制的MIND饮食法(目标摄入量是每天减少250千卡)或同样轻微的热量限制的对照饮食组。执行指导委员会构思了试验设计和统计分析计划。数据协调中心的工作人员定期进行安全检查,并创建数据监测报告和分析,以供独立的国家卫生研究所(NIH)批准的数据和安全监测委员会审查,该委员会由阿尔茨海默病、临床试验和统计方面的专家组成,他们不知道试验组的分组情况。该试验遵循1964年《赫尔辛基宣言》及其后来的修正案的伦理标准,并得到拉什大学医学中心、哈佛大学公共卫生学院和布里格姆妇女医院的机构审查委员会的批准。所有受试者都提供了书面的知情同意书。作者保证数据和不良事件报告的完整性和准确性,以及对方案的忠实性。
入选标准
65岁或65岁以上人群符合纳入条件,在30项蒙特利尔认知评估中得分至少为22分(范围从0到30,得分越低表明损害越大),超重(定义为BMI≥25),报告有阿尔茨海默病家族史(定义为有一级血亲患有痴呆症),饮食不理想(定义为MIND饮食评分≤8分),基于由研究者设计的一份包含14个项目的饮食问卷,该问卷旨在检测饮食不足与大脑健康之间的关系,得分范围从0到14,得分越低表明饮食不足与假定的大脑健康问题之间的关系越紧密。
2017年1月至2018年4月在美国的两个地点(芝加哥和波士顿大都会地区)通过向商业可用名单大量邮寄,向当地医疗机构分发传单以及在报纸,公共汽车,以及地铁车厢、车站和广播募集受试者。经历了两阶段的预选方案,以评估受试者资格。最初的筛选是通过电话进行的,收集年龄、痴呆症家族史、饮食质量、食物过敏、营养补充剂的使用、阿尔茨海默氏或帕金森病药物的使用等信息。符合条件的必须同意不服用维生素(如叶酸、维生素B12或多种维生素),并完成3至4周的磨合期,以评估他们遵守试验干预的可能性。在磨合期,受试者必须接听所有与试验有关的电话,并填写4周中至少3周的饮食记录。完成3周至4周磨合期的参与者由营养师和试验调查员评估其是否适合参加试验。
随机化与干预
受试者按1:1的比例被随机分配到MIND饮食组和对照饮食组。随机化是通过使用R软件3.3版实现(R Project for Statistical Computing)。根据试验地点、性别和年龄类别(65-69岁、70-74岁、75 -80岁、81-84岁)对分配进行分层。在基线时,测量身高、体重和血压,进行认知测试,并完成问卷调查(如24小时饮食回忆和食物频率问卷),然后由数据协调中心的研究人员将受试者分配到各饮食组。受试者被要求遵循他们指定的饮食3年。关键终点指标和协变量的数据在第6个月时收集,然后每年收集一次,直到试验结束。
在注册营养师的带领下,所有受试者的饮食咨询都是通过电话进行的,前6个月每周联系一次,后6个月每隔一周联系一次;在第2年和第3年,受试者每月至少进行两次电话随访。两组受试者都可以得到个性化的指导。在MIND组中,根据过去的饮食回忆,研究人员确定了那些属于该饮食的一部分,以便增加可能缺乏的食物的摄入量。在对照饮食组,建议的目标集中在份量控制上。这些修改旨在改变受试者的短期计划,以实现预期目标,但不改变饮食分配的结构。MIND组的饮食咨询包括将MIND饮食中的食物纳入指导,并将MIND饮食食谱用于减肥的行为策略,保持与基线相同的运动水平,并通过指导和目标设定来监督自己对饮食摄入的责任。对照饮食组的饮食咨询包括相同频率的咨询,但侧重于卡路里跟踪,份量控制和减肥行为策略,而不改变所消耗的食物类型。两组在轻度热量限制方面都得到了同样的支持,目标是在第3年达到体重减轻3%至5%的目标。
受试者被鼓励定期遵循他们指定的饮食。MIND组每月收到由非营利食品种植者组织捐赠的蓝莓(每周2.5杯,或15盎司[425克])、混合坚果(每周5盎司[142克])和特级初榨橄榄油(每周14汤匙,或7盎司[207毫升])。对照饮食组的受试者收到价值30美元的礼品卡的频率与MIND组收到食物的频率相同。在第3个月、第9个月、第18个月和第30个月的小组会议中,所有受试者都至少有5次机会与指定试验组的其他成员联系,以培养社会支持。小组会议包括关于他们指定饮食的教育,促进减肥的技巧,以及其他激励活动,如烹饪课程,益智问答游戏,比赛和节日庆祝活动。
研究人员收集了饮食依从性的几个短期测量指标的信息,如体重评估、受试者报告的MIND问卷(一份包含14个项目的问卷,旨在获得MIND饮食的依从性)和食物频率问卷的饮食评估,以及个性化目标设定。在一个亚组中测量了与关键饮食成分相关的血清生物标志物,包括类胡萝卜素(叶黄素和玉米黄质,反映绿叶蔬菜和其他十字花科蔬菜的摄入量)和α-胡萝卜素和β-胡萝卜素(如胡萝卜、南瓜和辣椒)。
在Covid-19大流行期间,我们被迫暂时停止试验运营约3个月(2020年3月19日至2020年7月15日)。在此期间,两个试验组的受试者继续通过电话接受饮食咨询,但没有进行面对面的测试(例如,认知、体重测量和抽血)。居家命令解除后,44名参与者(24人在MIND组,20人在对照饮食组)拒绝在第3年的评估中回到办公室接受面对面的认知测试。在数据和安全监测委员会的指导下,我们修改了方案,通过电话评估认知(仅情景和语义记忆),并将这些评估纳入初步分析。
终点指标
主要终点是从基线到第3年的整体认知和特定认知领域的变化。认知能力是通过12项公开的认知功能测试来评估的,情景记忆有5项测试(词表记忆、词表回忆、词表识别、东波士顿故事即时回忆和东波士顿故事延迟回忆);2个语义记忆测试(类别流畅性[动物和水果蔬菜]和多语言命名测试);2项执行功能测试(美国国立卫生研究院工具箱中的注意力测试B和Flanker抑制控制和注意力测试);3个知觉速度测试(口语符号数字情态测试、模式比较测试、连线测试A)。使用基线的平均值和标准差值将每个测试的原始分数转换为z分数,然后对所有测试的z分数进行平均,以创建全局复合分数,并对跨组间测试进行平均,以创建四个领域分数。综合得分越高,反映出更好的认知表现认知能力,在基线和第6、12、24和36个月时进行评估。认知测试由具有认知测试认证的研究助理进行,他们不知道试验组的分配情况。
次要终点是磁共振成像(MRI)与基线的变化,即总脑容量、海马体积和白质高强度病变的体积。在试验开始时,所有受试者都接受MRI成像(芝加哥地区使用3-Tesla飞利浦Achieva MRI扫描仪,波士顿地区使用西门子Skyra MRI扫描仪)。在招募了前100名受试者后,我们估计了每个饮食组中参加MRI检查的人数比例,并为一组非随机的参与者提供了MRI检查,以达到300人的目标样本量(约为入组受试者的一半)。仅在基线和第36个月进行MRI扫描。扫描结果由不知道试验组分配的分析师进行评估。
统计分析
该试验旨在测试MIND饮食对3年内全球认知评分年变化率的影响。使用专为混合模型分析而设计的PASS 2008软件(NCSS)中的模拟方法,我们分析了两项观察性队列研究(Rush记忆与衰老项目和芝加哥健康与衰老项目)的数据,并估算了MIND饮食评分对基线时无认知障碍者认知能力下降的影响大小。假设脱漏率为20%,每个试验组300名受试者的样本将为该试验提供90%以上的power,以检测认知能力下降的年速率每年0.02个标准单位的组间差异。次要MRI结果的power测定不是样本量估计的一部分。我们进行了意向治疗分析,纳入了所有接受随机分组的受试者。
由于全球认知评分随时间的变化轨迹是非线性的,我们估计了每次随访时与基线的平均变化,然后比较了试验组之间随时间的变化。我们使用随机截距的线性混合效应模型,正如协议中规定的那样,但我们没有对时间进行线性建模,而是将时间作为每次随访的指标变量。与对照饮食组相比,MIND饮食组在每次随访时对整体认知的影响是通过使用试验组分配和试验访问的指标变量的乘积来估计的。为了分析脑形态特征,我们还调整了临床地区(即波士顿和芝加哥)的模型,以解释扫描仪的差异。多个结果的置信区间宽度,如认知领域(4个结果)和MRI衍生测量(3个结果),没有针对多个测试进行校正,因此这些置信区间不应用于推断这些结果的治疗效果。
为了弥补缺失的数据,我们使用R包中的多重插补算法——链式方程多重插补(MICE)算法进行了多重插补,纳入了广泛的认知相关预测因素,如年龄、性别、教育程度、认知活动、临床地点和基线认知评分。我们认为包含输入数据的分析是对主要分析的补充。为了检验Covid-19大流行后通过电话进行的评估是否影响了初步结果,我们进行了排除这些电话评估的额外分析。
我们将脑MRI衍生的体积标准化为颅内体积,并遵循标准程序对数据进行标准化。然后,我们使用估计的边际均值计算平均值和95%置信区间,以脑成像结果、饮食分配和临床地区为自变量。我们计算了从基线到第3年的差异,然后进行两两比较,以评估MIND饮食组和对照饮食组之间的差异。所有分析均使用R统计计算4.0版(R Foundation for statistical computing)进行。
结果
受试者
于2017年1月至2018年4月纳入受试者;数据收集于2021年6月完成。在1929名接受筛查的人中,1325人(68.7%)被排除在外,其中545人的MIND饮食得分高于拒绝参加试验的8305人,160人因病史或药物使用而未能纳入(图1)。在磨合过程中,109人不符合继续标准。其中有93人退出,5人没有完成饮食日记,11人搬离该地区或因病史或用药不符合继续试验的条件。共有301名受试者被分配到MIND饮食组,303名受试者被分配到对照饮食组。到第3年,MIND饮食组共有26名受试者(8.6%)和对照饮食组14名受试者(4.6%)失访。
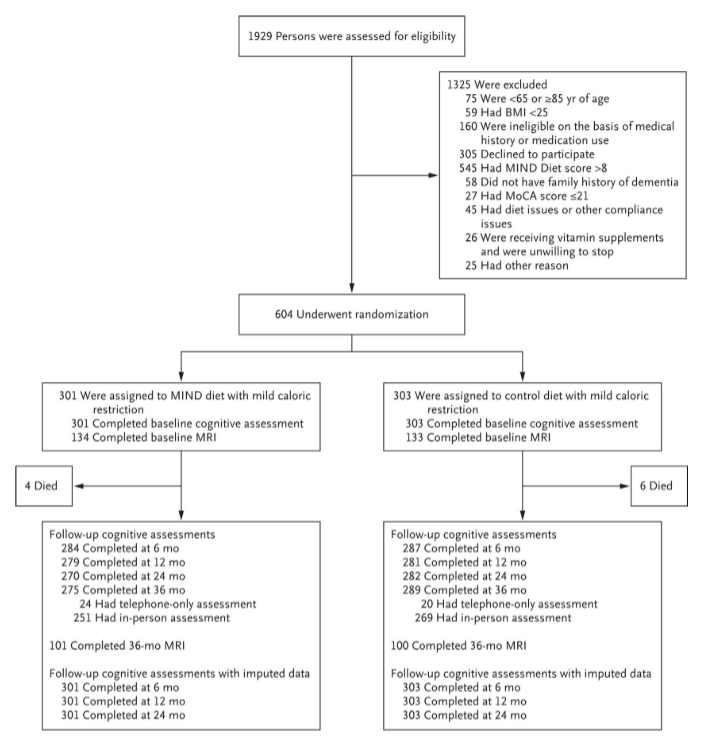
图1 筛选、随机化和随访流程图
受试者在基线时的特征相似,除了对照饮食组携带载脂蛋白E ε4等位基因的受试者比例略高。最常见的共存疾病是高血压和2型糖尿病,其患病率在两组中相似(表1)。在3年的试验中,3020项计划的认知评估中有169项(5.6%)没有进行,需要进行归因,这被认为是一种敏感性分析。
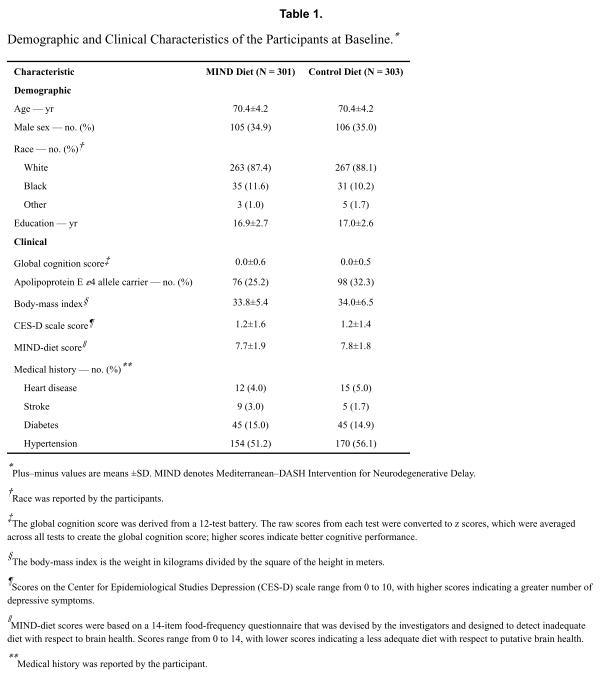
表1 基线时参与者的人口统计学和临床特征
营养生物标记物和体重
基线数据,MIND饮食组的平均分为7.7(95% CI,7.5-7.9),对照组为7.8 (95% CI, 7.6-8.0)。在6个月时,MIND饮食组的受试者MIND饮食得分提高了3.3分,平均得分为11.0分,在整个试验过程中大约保持在这个水平。在对照饮食组,MIND饮食得分也提高了,但只增加了0.7分,平均得分为8.5分。血液中抗氧化营养水平(叶黄素、玉米黄质、α和β胡萝卜素)的生化分析结果支持MIND饮食。两组受试者在随访期间体重均有所减轻;MIND饮食组体重较基线变化为-5.0 kg (95% CI,-5.8- -4.1),对照组体重较基线变化为-4.8 kg (95% CI,-5.7- -4.0)。
主要和次要终点
从基线值到第3年,MIND饮食组总体认知评分(主要终点)的估计平均变化为0.205标准化单位(95% CI, 0.164-0.246),对照组为0.170标准化单位(95% CI, 0.130-0.210)。在意向性分析中,试验组之间的平均评分变化没有显著差异,试验结束时的估计平均差异为0.035个标准化单位(95% CI,-0.022-0.092;P=0.23)(表2和图2)。在两个试验组中,总体认知评分从基线开始的变化遵循类似的非线性模式。当排除Covid-19大流行期间通过电话获得的认知评估(44名受试者[1.5%])时,对缺失数据进行代入的分析结果与主要分析的结果相似。关于其他主要终点的研究结果(即,与基线相比的变化4个认知领域得分)与整体认知得分相似。在第1年,MIND组的平均整体认知评分比基线增加了0.226个标准化单位(95% CI, 0.188-0.264),对照组的平均整体认知评分比基线增加了0.211个标准化单位(95% CI, 0.173-0.248);第2年,与基线相比相应的变化为0.246 (95% CI, 0.205-0.287)和0.200 (95% CI, 0.159-0.240)。
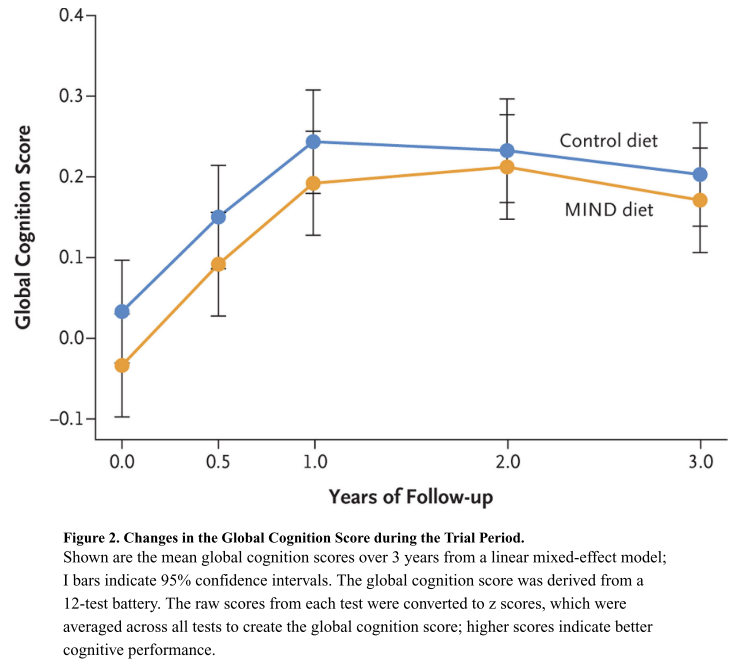
图2 试验期间整体认知评分的变化
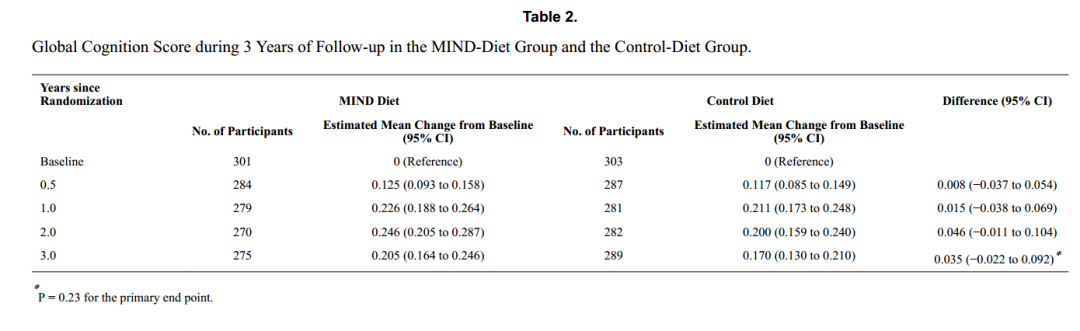
表2MIND饮食组和对照饮食组3年随访期间的整体认知评分
脑成像
604名受试者中,共有267人同意在基线时接受脑成像,其中201人在第3年接受了随访成像。我们从分析中排除了1名受试者,因为基线MRI质量不合格,因此剩下200名受试者用于分析。在试验结束时,MIND组和对照饮食组的白质高强度体积都增加了,而两组的海马和总脑体积都减少了(表3)。与对照饮食相比,MIND饮食在白质高容量的变化方面(平均差异-0.019;95% CI,-0.046-0.008),海马体积(平均差值0.005;95% CI,-0.016-0.026),以及灰质和白质总体积(平均差值0.001;95% CI,−0.003-0.005)没有观察到明显的影响。
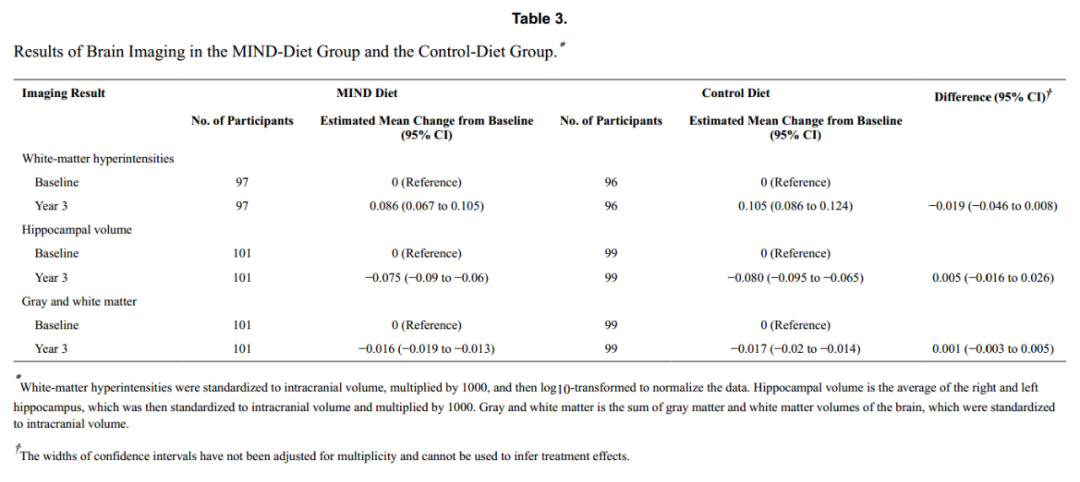
表3MIND饮食组和对照饮食组的脑成像结果
不良事件
3年间,各试验组的不良事件发生率相似,MIND组89名受试者中发生127起不良事件,对照组91名受试者中发生153起不良事件。最常见的是心血管疾病(MIND组17例,对照饮食组32例)和肌肉骨骼疾病(60名受试者发生68例,MIND组39例,对照饮食组29例)。试验期间发生10例死亡(MIND组4例,对照组6例)。数据和安全监测委员会没有将死亡和不良事件归类为与指定饮食有关。
讨论
MIND饮食以地中海心血管饮食和DASH饮食为基础,包括被认为与保持大脑健康有关的食物和营养素。在这项涉及有痴呆家族史的老年人的两中心随机试验中,我们发现遵循MIND饮食的受试者在整体认知能力方面有小幅改善,与那些遵循轻度热量限制的对照饮食的受试者相似。
观察性研究的结果支持了健康饮食对大脑健康的影响,一些证据表明,大量食用绿叶蔬菜、坚果和浆果以及橄榄油与阿尔茨海默病标志性神经病理特征的减少有关。所提出的潜在机制指向抗氧化和某些食物具有抗炎能力,可以保护大脑功能,防止认知能力下降。动物模型也显示了维生素E和二十二碳六烯酸对表面上健康的脑功能的潜在重要性,包括防止脂质过氧化、神经元丧失、β-淀粉样蛋白沉积、记忆和学习能力下降。然而,这些作用在人类身上的机制证据还没有得到很好的证实。我们纳入了总脑容量、海马体积和白质高强度体积的测量来研究生物学机制,但这些MRI扫描的计划参与率未达到50%。然而,尽管这些研究可能不够有力,但试验组的脑成像结果是相似的。
先前对饮食试验的荟萃分析显示了不同的结果,通常不能肯定流行病学研究中观察到的饮食对认知的有益影响。有几个原因可能导致这种差异。观察性研究中存在偏差和混淆是一种可能。也有可能是随访时间的差异和既往存在的共存疾病的影响。在我们的试验中,我们比较了MIND饮食组和对照饮食组,对照饮食组被指出限制卡路里,考虑到两组的体重减轻的证据相似,对照饮食组的受试者可能改善了他们的饮食。重复认知测试的练习效果也可以解释我们两个试验组的改善,正如在以前的随机试验中观察到的结果,有可能这些干预措施并不能改善认知功能,或者需要更长的时间才能观察到效果。
我们的试验存在局限性。该试验的一个特点是要求受试者有痴呆家族史,随机化前饮食不佳,超重,所有这些都被证明是阿尔茨海默病和认知能力下降的重要危险因素。受试者多为受过良好教育的老年人,多为欧洲人后裔,约10%的受试者为黑人。我们的研究结果可能无法推广到来自不同背景和受教育程度低于试验人群的人群。
结论
在一项旨在改善大脑健康的MIND饮食试验中,遵循MIND饮食的受试者与遵循轻度热量限制的对照饮食的受试者在3年后的认知功能和脑成像结果没有显着差异。
论肿道麻 述评
《新英格兰医学杂志》上发表的这项关于MIND饮食的研究,提供了关于饮食模式对老年人认知功能影响的重要见解。MIND饮食,融合了地中海饮食和DASH饮食的精髓,特别强调植物性食品的摄入,限制高饱和脂肪和高糖食品,旨在降低痴呆风险。这项为期三年的随机对照试验,纳入了有痴呆家族史、超重且饮食不佳的老年人,比较了MIND饮食与对照饮食对认知功能和大脑MRI结果的影响。
研究结果显示,尽管两组参与者的全球认知评分均有所提高,但MIND饮食组与对照饮食组间的差异并不显著。此外,MRI测量的大脑结构变化在两组间也未表现出明显差异。这些发现提示,尽管MIND饮食可能对心血管健康有益,但其对预防认知衰退的效果可能并不如预期那样显著。研究的局限性在于参与者的选择偏倚,大多数为受过良好教育的欧洲后裔老年人,这限制了研究结果的普适性。
该研究对公共卫生具有重要意义,因为它挑战了关于特定饮食模式能够显著改善认知功能的传统观点。同时,它也强调了未来研究需要更广泛和多样化的参与者群体,以及可能需要更长时间的干预来观察饮食对认知的长期影响。此外,该研究结果提醒我们,在推荐饮食作为预防认知衰退的策略时,需要谨慎考虑其潜在的局限性和实际效果。尽管MIND饮食未能显示出预期的益处,但其对健康的其他积极影响仍不容忽视,未来的研究可能会揭示更多关于饮食、生活方式和认知健康之间复杂关系的信息。
参考文献:
Barnes LL, Dhana K, Liu X, Carey VJ, Ventrelle J, Johnson K, Hollings CS, Bishop L, Laranjo N, Stubbs BJ, Reilly X, Agarwal P, Zhang S, Grodstein F, Tangney CC, Holland TM, Aggarwal NT, Arfanakis K, Morris MC, Sacks FM. Trial of the MIND Diet for Prevention of Cognitive Decline in Older Persons. N Engl J Med. 2023 Aug 17;389(7):602-611.doi:10.1056/NEJMoa2302368


