发生小细胞转化的TKI耐药EGFR突变肺腺癌具有怎样的分子特征?
时间:2025-03-10 12:08:59 热度:37.1℃ 作者:网络
在表皮生长因子受体(EGFR)突变的肺腺癌中,小细胞转化是较为罕见的酪氨酸受体激酶抑制剂(TKI)耐药机制。本研究旨在评估在接受EGFR-TKI治疗后转化为小细胞癌的EGFR突变的肺腺癌中,分子图谱及Rb1功能状态的动态变化。这是一项双向性研究(2019-2023年),发生小细胞转化的EGFR突变肺腺癌患者的基线和TKI治疗后活检样本进行了Rb1免疫组化和72基因靶向NGS panel检测。Rb1缺陷定义为Rb1蛋白缺失,或Rb1保留/p16高/Cyclin-D1低蛋白表达谱且存在RB1突变。纳入了一组未发生小细胞转化的EGFR突变肺腺癌患者,用于对比Rb1状态。9例患者(10%,9/84)的TKI治疗后活检样本被诊断为小细胞转化。他们所有检测的基线腺癌样本(n = 7)和TKI治疗后小细胞癌样本(n = 9)均存在Rb1缺陷,同时还存在TP53(11/11)和PTEN突变(2/11)。9例未发生小细胞转化患者的18份样本显示,仅1例患者(1/9)存在Rb1缺陷。在EGFR-TKI治疗后转化为小细胞癌的EGFR突变腺癌中,基线时Rb1功能失活几乎普遍存在,提示Rb1缺失是小细胞转化的先决条件。然而,这可能并不充分,因为并非所有基线时Rb1缺失的腺癌都转化为小细胞癌。在基线或疾病进展时,除了TP53和PTEN,未发现其他常见癌基因的重现性突变。在样本量有限的情况下,驱动小细胞转化的特定分子事件仍不明确。
研究背景
表皮生长因子受体(EGFR)突变是肺腺癌中最常见的驱动因素,在亚洲患者中,EGFR突变占所有病例的三分之一到一半。在晚期疾病中,EGFR酪氨酸激酶抑制剂(TKIs)是标准的一线治疗选择 。然而,大多数患者在9-13个月的中位无进展生存期后,不可避免地会产生耐药性。特别是在使用第一代和第二代TKIs时,60-70%的患者会因EGFR外显子20 p.T790M突变克隆的产生和扩大对TKI产生耐药 。不过,这些突变对一些新一代TKIs(如奥希替尼)有反应,并且在肿瘤进展时,通过非侵入性液体活检可以检测这些突变,具有较高的阳性预测价值,无需再次进行组织活检 。
另一种较为罕见的TKI耐药机制是 “组织学转化” 为小细胞癌,在约3-15%的TKI治疗后进展的EGFR突变肺腺癌患者中观察到这种情况 。与典型的原发性小细胞肺癌相似 ,TKI治疗后转化的小细胞癌也经常存在肿瘤蛋白的双等位基因缺失:TP53编码的p53和RB1编码的视网膜母细胞瘤转录共抑制因子1(Rb1);然而,它们保留了最初的EGFR突变 ,提示是由EGFR突变的肺腺癌细胞发生克隆进化和转分化而来,而非新发的第二原发性肿瘤。转化的小细胞癌具有侵袭性,通常采用传统的小细胞肺癌方案进行治疗,总体预后较差 。
少数研究报告,与其他耐药机制的患者相比,在TKI治疗进展、发生小细胞转化的EGFR突变肺腺癌患者中,基线TP53突变和Rb1缺失显著富集。因此,虽然p53和Rb1缺失似乎是小细胞转化的必要条件,但它们本身并不足以导致表型转变。目前,分析小细胞转化患者克隆进化轨迹的研究非常有限,且涉及的患者数量较少 ,人们对这一神秘现象的分子机制也知之甚少。
目前,小细胞转化只能通过组织活检进行组织学检查来诊断。虽然一些研究提出,基线Rb1缺失可作为未来小细胞转化的预测标志物 ,但这一观点需要在独立队列中进行验证。本研究旨在分析TKI治疗后发生小细胞转化的EGFR突变肺腺癌患者的临床病理特征,并评估基线和小细胞转化时分子图谱及Rb1功能状态的动态变化。
研究结果
研究期间,2670例未经治疗的肺癌患者的样本进行了EGFR突变实时聚合酶链反应分析,其中695例患者(695/2670,26%)检测出EGFR突变。同期,收到了84份TKI治疗后的组织样本,其中9例患者(10%)的样本显示小细胞转化(图1中的患者1-9)。患者9有两份TKI治疗后的组织样本,其中第二份为发生转化的小细胞癌样本。因此,本研究共纳入了发生小细胞转化患者的19份样本(9份基线样本和10份TKI治疗后样本)。
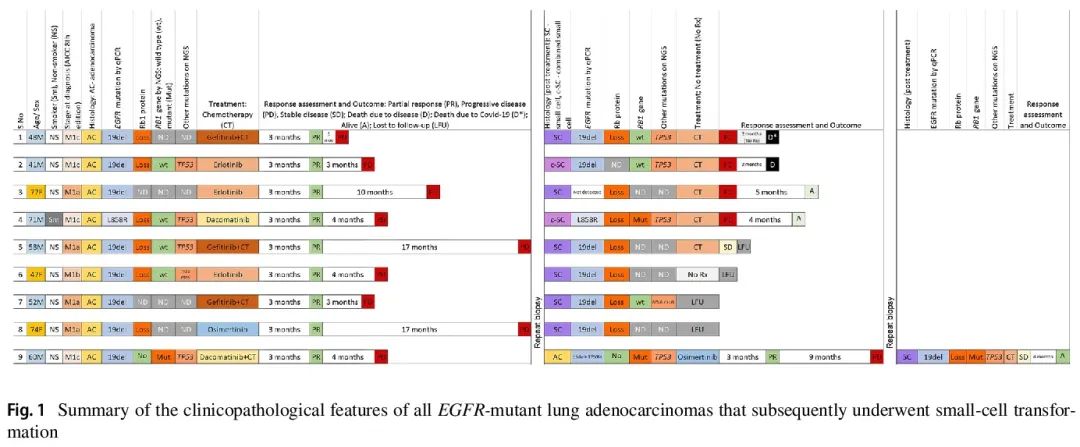
图1
在其余未显示小细胞转化迹象的TKI治疗后样本中,选取了9例患者的样本(18份样本:9份基线样本和9份TKI治疗后样本),用于对比Rb1功能状态。
小细胞转化队列
临床病理特征
所有9例患者均为成年人,诊断时年龄在41-77岁之间(中位52岁),且诊断时存在转移性疾病。其中男性6例,女性3例。除1例患者(患者4)外,大多数为非吸烟者。
基线活检特征
基线时,所有患者均为腺癌,其中8例具有腺样结构,1例为实性结构,且对甲状腺转录因子-1均呈免疫阳性(图2A、G、H)。通过实时聚合酶链反应检测,8例患者检出EGFR外显子19缺失,1例患者检出EGFR外显子21 p.L858R突变。所有患者均接受了第一代或第二代TKI单药治疗或联合化疗。所有患者最初均达到部分缓解,但在中位10个月(4-20个月)的无进展生存期后,最终出现疾病进展(图1)。
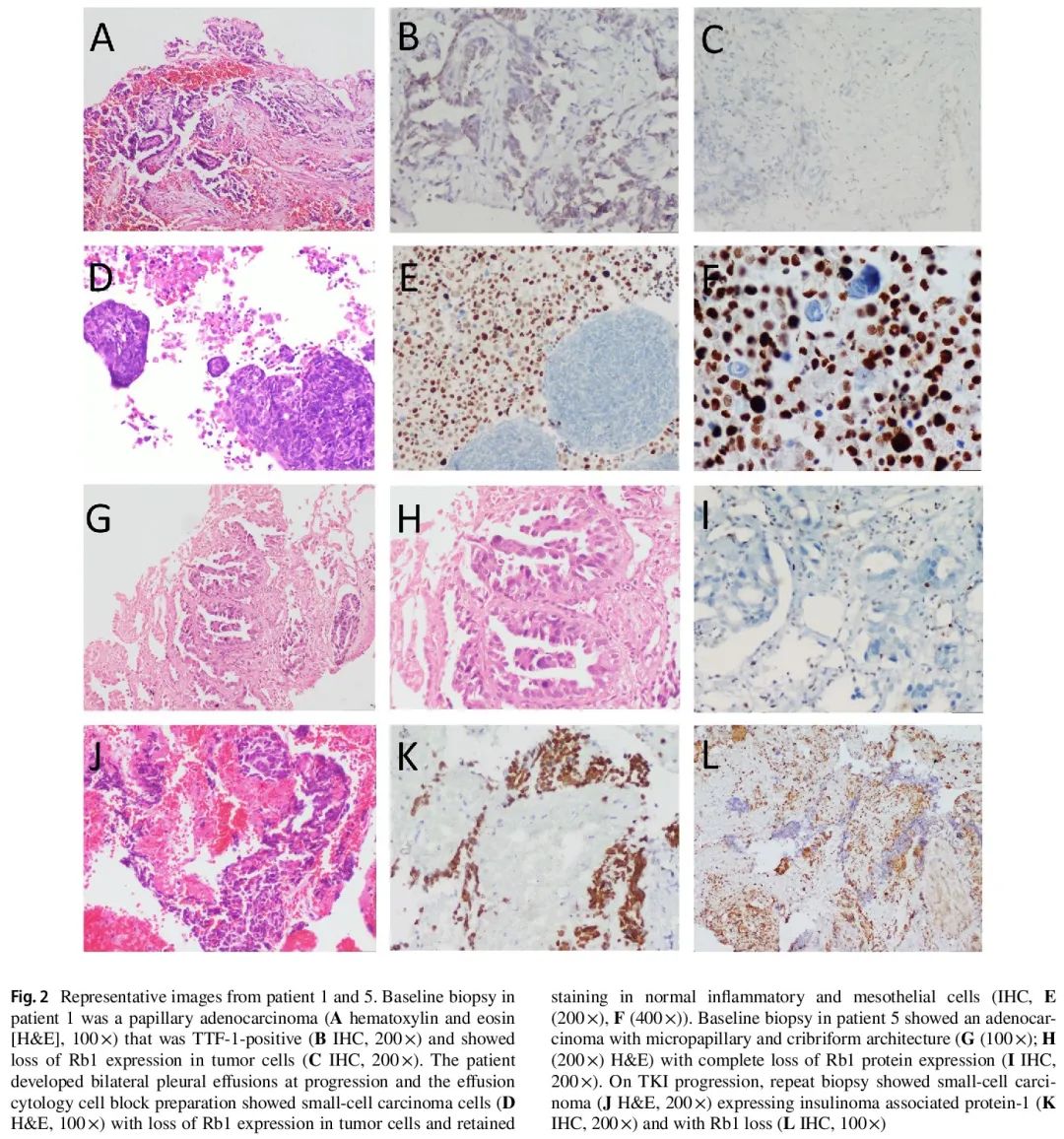
图2
TKI治疗后活检特征
首次疾病进展时的重复活检显示,6例为纯小细胞癌,2例为小细胞癌合并腺癌和鳞状分化,1例患者(患者9)为伴有退行性改变的仅腺癌。聚合酶链反应显示,7份样本仅检测到初始的EGFR突变,1份样本(患者9)检测到额外的EGFR外显子20 p.T790M突变,1份样本(患者3)未检测到EGFR突变。
除了存在EGFR外显子20 p.T790M突变的腺癌患者9接受奥希替尼单药治疗外,其他发生小细胞转化的患者被提供化疗。其中,1例患者拒绝治疗,4例在化疗过程中病情持续进展,其中2例在2个月内死亡,其余2例在第二次活检后的4个月和5个月时疾病进展,仍存活,还有1例在随访期间病情稳定。
患者9使用奥希替尼后最初达到部分缓解,但在第二次活检12个月后最终出现疾病进展。此时的再次活检显示发生了小细胞转化,TTF-1呈阴性,仅存在初始的EGFR突变,EGFR p.T790M突变消失。该患者接受了化疗和全脑放疗,病情已稳定4个月。
Rb1功能状态
免疫组化显示,6/7份基线样本(除患者9外)(图2C、I)、所有TKI治疗后转化的小细胞癌(图2D-F、J-L)和小细胞癌合并其他癌的样本Rb1蛋白表达缺失。在患者9中,基线和首个TKI治疗后腺癌样本中Rb1表达保留,而在转化的小细胞癌中Rb1表达缺失。然而,该患者的所有三份样本均显示p16高/Cyclin-D1低的特征,符合Rb1缺陷,提示Rb1功能失活。因此,所有发生小细胞转化的病例在基线时均存在Rb1缺陷。
NGS显示,在6例接受检测的患者中,仅2例存在RB1突变。患者4仅在TKI治疗后转化的小细胞癌中检测到RB1突变,而患者9的所有三份样本均检测到RB1突变。
其他基因改变
5份样本(患者2、4、5、6和9)的基线靶向NGS检测显示,所有检测样本均存在TP53错义突变和EGFR突变。患者6还检测到PTEN突变。
5份样本(患者1、2、4、7、9)的TKI治疗后靶向NGS检测显示,所有样本均存在TP53突变和初始的EGFR突变。患者9还检测到EGFR p.T790M突变,患者7还检测到PTEN突变。
在进行NGS检测的配对样本(患者2、4、9)中,基线时检测到的TP53、EGFR和RB1变异在TKI治疗后样本中也检测到。除了患者4仅在TKI治疗后样本中检测到RB1突变外,其他配对样本在小细胞转化后未发现任何新获得的突变(表1)。
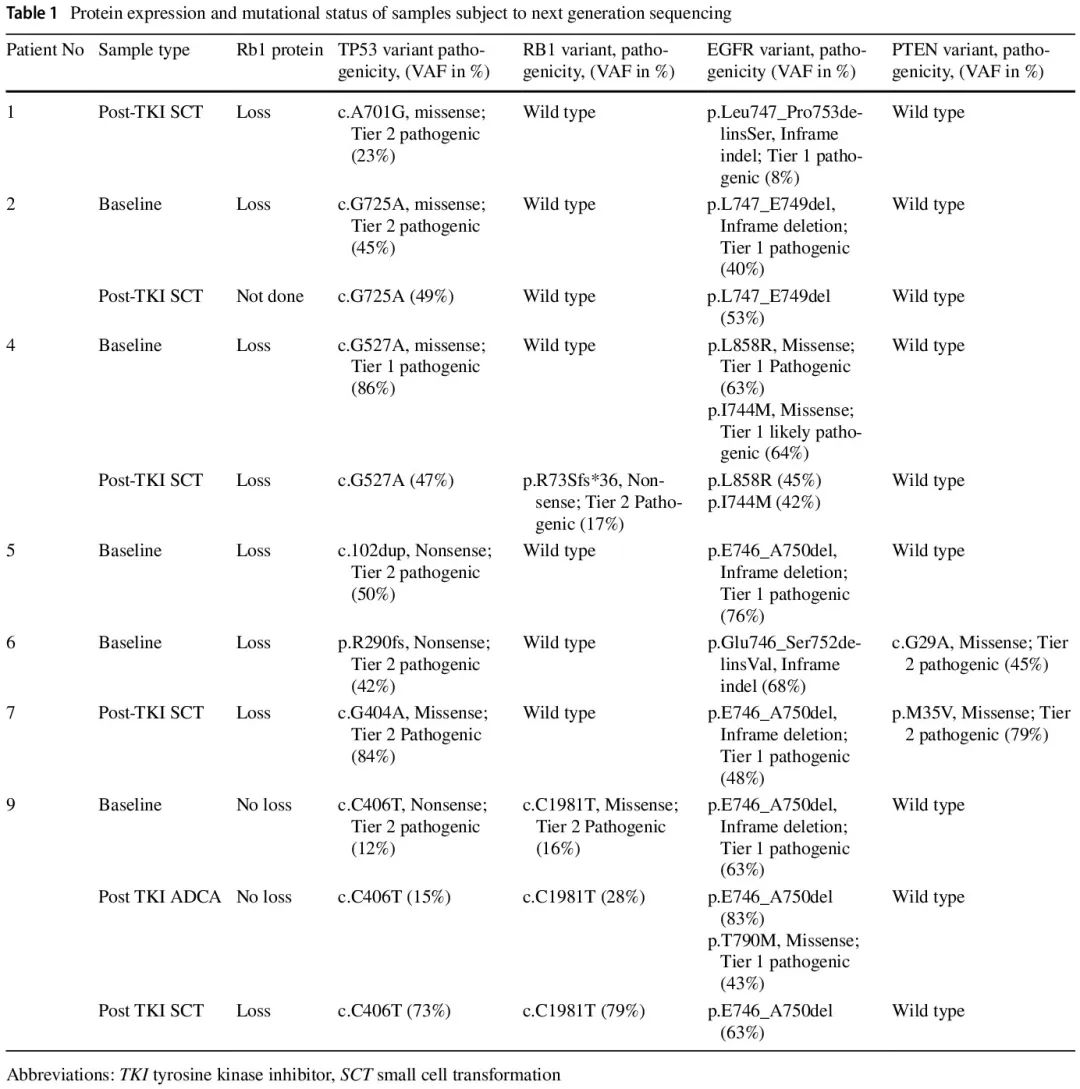
表1
对照队列(未发生小细胞转化的患者)
在未发生小细胞转化的队列中,除1例患者的基线和TKI治疗后肿瘤样本均显示Rb1缺失外,所有检测的组织样本(n = 17)均显示Rb1蛋白表达保留。两次活检均显示腺癌组织学,且肿瘤细胞对神经内分泌标志物呈阴性。NGS检测未在任何检测样本中发现RB1突变,包括Rb1蛋白表达缺失的样本。
Rb1缺陷与小细胞转化的相关性
在本研究中,基线Rb1缺陷在发生小细胞转化的病例中显著富集,见于7/7例接受检测的小细胞转化病例和1/9例未发生小细胞转化的病例(p = 0.0014)。在8例Rb1缺陷的病例中,7例为免疫组化显示Rb1蛋白缺失,1例为Rb1保留/p16高/Cyclin-D1低且存在RB1突变。根据21例具有配对的Rb1免疫组化和RB1突变检测结果的组织样本(小细胞转化队列10例,非小细胞转化队列11例),Rb1蛋白表达状态与RB1突变状态的总体一致性为57%(12/21)。基于免疫组化的基线Rb1缺失对未来小细胞转化的灵敏度为87.5%(7/8),特异性为88%(8/9),阳性预测值为87.5%(7/8),阴性预测值为88%(8/9)。
讨 论
小细胞转化于2006年首次被发现,在出现TKI耐药后进行的活检中,其发生率在不同研究中分别为3%(4/155)、10%(21/206)、14%(5/37)和18%(7/39) ,与本研究中的10%(9/84)相近。小细胞转化的诊断通常基于小活检样本,其组织学表现可为单纯小细胞癌或混合性小细胞癌 。转化的小细胞癌具有与典型原发性小细胞肺癌相似的免疫组化特征,对突触素、胰岛素瘤相关蛋白1及其他神经内分泌标志物呈阳性,大多数病例中甲状腺转录因子-1弥漫阳性。如先前研究观察到的,在发生小细胞转化的患者中,EGFR外显子19缺失作为起始突变较常见,本研究队列中仅有1例患者存在EGFR外显子21 p.L858R突变。不同TKI药物的小细胞转化发生率无显著差异。在本研究及其他研究中,几乎所有代的TKI(包括第三代的奥希替尼和rociletinib)治疗后都观察到小细胞转化。
在大多数发生小细胞转化的患者中,通常对EGFR-TKI有初始反应,本研究队列也是如此。本研究队列中,从开始使用TKI到疾病进展的中位时间为10个月,这与先前研究相当。Roca等人对25项研究中37例小细胞转化患者进行的荟萃分析显示,中位进展时间为19个月(1-61个月),而在更近的队列研究中,中位进展时间分别为13个月和15个月。考虑到小细胞转化的中位时间比临床试验中所有接受TKI治疗的EGFR突变肺腺癌患者的中位无进展生存期(约8-11个月)更长,可以推断,TKI暴露时间越长的患者,发生小细胞转化的可能性越高。这对于针对EGFR p.T790M突变的第三代TKI可能尤为正确,因为这类药物通常能带来更长的治疗反应持续时间。相反,也有研究称,部分患者在原发性TKI耐药(<6个月)时被诊断为小细胞转化,尽管他们接受TKI治疗的时间非常有限,但病情进展迅速。可以推测,“早期转化”和“晚期转化”的小细胞转化分子机制可能存在根本差异,前者可能代表采样有限的EGFR突变混合型小细胞肺癌。在这类肿瘤中,TKI治疗后腺癌成分可能消退,留下占主导的小细胞癌,再次活检时就被解释为小细胞转化。
小细胞转化是在EGFR-TKI压力下发生的这一普遍观点,得到了一些证据的支持,比如转化后的小细胞癌在停用TKI一段时间后可恢复为腺癌,以及在接受ALK-TKI治疗的间变性淋巴瘤激酶(ALK)重排腺癌中也出现了类似的小细胞转化。然而,存在未接受过TKI治疗的EGFR突变小细胞癌、未接受过TKI治疗的ALK重排小细胞癌,以及在接受化疗的EGFR野生型肺腺癌、免疫治疗后的EGFR野生型鳞状细胞癌或手术后驱动基因状态未知的肺腺癌中发生的小细胞转化,这些都表明TKI暴露并非转化的唯一驱动力,TKI治疗可能只是一个加速因素,它揭示了某些肺癌固有的谱系可塑性。能够识别出这部分易发生小细胞转化的肺腺癌亚群,对临床实践和治疗具有重要意义。
作为一种耐药机制,小细胞转化的表型与其他基因耐药机制(如EGFR p.T790M突变 、PIK3CA突变、C-MET扩增 或EGFR p.C797S突变 )并不相互排斥。这些基因耐药机制可能与小细胞转化同时发生,也可能在小细胞转化之前或之后的其他时间点出现。本研究中的患者9先出现EGFR p.T790M突变,随后在第二次活检时被诊断为小细胞转化,此时EGFR p.T790M突变消失,这突出了在EGFR-TKI影响下,肺腺癌在表型和分子层面的动态可塑性。
在文献报道的大量转化型小细胞癌系列研究中,转化型小细胞癌的侵袭性表现各异。大多数患者接受传统的小细胞肺癌治疗方案(铂类化疗) ,部分患者联合EGFR-TKI治疗 。有个别报道称转化型小细胞癌对EGFR-TKI有良好反应,但这可能是由于转化后的小细胞癌中EGFR表达降低,但基因水平仍保留突变。大多数转化型小细胞癌对细胞毒性化疗有反应,但持久反应较为罕见,患者最终往往死于疾病,总生存期与典型原发性小细胞肺癌相似甚至更差。对于在化疗方案治疗期间病情进展的小细胞转化患者,重新引入基线TKI作为挽救治疗,部分患者有一定疗效。在本研究中,所有患者接受化疗后的预后都较差。免疫治疗在这些病例的治疗中作用有限。源自转化型小细胞癌的细胞系表现出多种波动表型(从腺癌转化为小细胞癌,反之亦然),对化疗药物的敏感性和耐药性也在动态变化,因此针对转化型小细胞癌的最佳治疗方案可能需要为每位患者量身定制。
在大多数典型原发性小细胞肺癌中,p53和Rb1必然失活。虽然约50%的肺腺癌中也会出现TP53突变,但RB1突变(<1%) 或Rb1缺失(<5%)在肺腺癌中较为罕见,同时发生EGFR、TP53和RB1突变的情况仅占所有肺腺癌的1%(43/4112)。有趣的是,至少有四项先前的研究观察到,在TKI压力下转化为小细胞癌的EGFR突变肺腺癌中,基线TP53和RB1改变的频率较高。在一组75对基线- TKI治疗后匹配的肿瘤样本中,Lee等人报告称,在转化为小细胞癌的17份基线样本中,88%(15/17)存在Rb1缺失,而在未转化组的58份样本中,这一比例仅为8%(5/58)。他们还指出,基线时Rb1和p53失活的肺腺癌发生小细胞转化的风险比其他情况高43倍。另一项根据RB1突变状态选择病例的研究发现,三重突变(EGFR/TP53/RB1)的肺腺癌发生小细胞转化的频率,是没有这些突变的肺腺癌的6倍。此外,无论是否发生小细胞转化,三重突变的肺腺癌无进展生存期(9.5个月)和总生存期(29.1个月)都比EGFR/TP53双突变和EGFR单突变的肺腺癌更短。与这些报道一致,我们发现所有转化为小细胞癌的肺腺癌在基线时,TP53突变和Rb1缺陷的频率都很高。即使在患者9中,其肿瘤在基线时表达Rb1蛋白,但呈现p16高和Cyclin-D1低的特征,提示Rb1功能失活。
我们发现Rb1蛋白表达水平与RB1突变状态的相关性较差,一致性仅为57%(12/21)。总体而言,Rb1缺失比RB1突变更为常见。本研究使用的NGS方法仅覆盖RB1基因的外显子区域,然而,RB1基因常因基因组重排(断点位于内含子区域)或表观遗传沉默机制而发生改变 ,这导致检测灵敏度较低。即使基因覆盖范围合适,在最近一项研究中,高达20%(169/208)的典型原发性小细胞肺癌在突变状态和蛋白表达水平之间存在不一致性,在16%(29/184)Rb1缺失的病例中,即使人工复查NGS reads也未发现突变。相反,同一研究发现,5%(10/208)的病例尽管存在RB1突变,但Rb1表达仍保留。在先前的研究中,转化型小细胞癌中也观察到类似的“Rb1表达/RB1突变”特征,频率为25%(3/12),本研究队列中的患者9也是如此。在典型原发性小细胞肺癌中,这类病例显示出高p16和低cyclin-D1蛋白水平,提示表达的突变型Rb1蛋白确实无功能,本研究中患者9的转化型小细胞癌也是如此。
在小鼠模型中,Rb1对神经内分泌分化起关键调控作用,在p53失活的细胞中,Rb1失活会驱动细胞沿神经内分泌谱系发生表型分化。然而,尽管Rb1缺失/RB1突变和TP53突变是小细胞转化的必要条件,但它们似乎不足以导致TKI耐药或小细胞转化。Neiderst等人在吉非替尼敏感的细胞系中证明,通过sh-RNA介导的Rb1缺失,既不影响吉非替尼的敏感性,在诱导TKI耐药时也不会导致小细胞癌的发生。Offin等人发现,只有25%的携带RB1突变的EGFR突变肺腺癌最终会转化为小细胞癌。在这种情况下,基线时Rb1缺失可能有助于识别小细胞转化风险增加的患者。尽管在本研究中,免疫组化检测显示基线Rb1缺失对未来小细胞转化的敏感性和阳性预测值均为87.5%,但对所有基线Rb1缺失的肺腺癌进行前瞻性随访,才能更准确地计算出基线Rb1缺失的EGFR突变肺腺癌发生小细胞转化的风险。
克隆进化研究表明,转化型小细胞癌的肿瘤克隆并非直接从最初的肺腺癌细胞进化而来,而是在早期就发生了分支。在转化前的系列测序肿瘤中,观察到激活诱导的胞苷脱氨酶高突变(AID)/APOBEC相关的突变特征,与基线腺癌(主要表现为C>T转换)相比,转化型小细胞癌中C>A转换增加。据推测,p53/Rb1失活会导致G2/M细胞周期检查点失调,使全基因组加倍的发生率(80%)高于传统非小细胞肺癌(34%)或典型原发性小细胞肺癌(51%) 。转化型小细胞癌在基线时的拷贝数变异负荷就高于未转化的病例,较高的拷贝数变异负荷还与更短的转化时间和更短的生存期相关。虽然转化型小细胞癌的RNA和mi-RNA谱与典型原发性小细胞肺癌更为相似,而与匹配的基线样本和其他保留腺癌组织学特征的TKI耐药肺腺癌差异较大,但它们保留了肺腺癌的DNA甲基化模式。在有限的基线-TKI治疗后匹配样本研究中,转化型小细胞癌获得的单基因突变包括NOTCH(神经源位点Notch同源蛋白) 、PTEN(磷酸酶和张力蛋白同源物) 、BRCA2(乳腺癌基因2) 、MYC原癌基因(MYC)扩增 、TERT(端粒酶逆转录酶)扩增 和PIK3CA(磷脂酰肌醇-4,5-二磷酸-3-激酶催化亚基α) ,但目前尚不清楚这些是旁观者突变还是具有因果关系。尽管本研究使用了包含上述大多数基因的代表性panel,但在本研究队列中,仅在两份样本中检测到额外的PTEN突变,一份在基线时(患者6),一份在TKI治疗后的样本中(患者7)。Suda等人先前表明,在耐药转化后出现PTEN p.M264I突变。最近一项基于小鼠模型的研究强调了PTEN缺失在促进由Rb1/p53失活引发的神经内分泌癌谱系可塑性中的作用,这可能也适用于TKI治疗后转化的小细胞癌。
本研究存在多种局限性。由于只有9例小细胞转化患者和9例对照病例,统计效力有限。需要更多队列或更大的多机构数据集,来确认基线Rb1缺失的预测价值,并更精确地估计小细胞转化的发生率。此外,使用的靶向NGS panel可能无法完全捕获RB1基因的内含子或结构变异,导致灵敏度较低,与蛋白表达数据的一致性较差。患者接受了不同代的TKI(有时还联合化疗),这使得难以确定某些TKI或联合治疗策略是否更容易导致小细胞转化。本文将突变和免疫组化模式与临床结果进行了关联,而体外或体内功能模型有助于确定基线Rb1或PTEN缺失在驱动谱系可塑性中的因果作用。这些机制数据能更好地为治疗策略和前瞻性生物标志物开发提供参考。
频繁的基线Rb1缺失和TP53突变是EGFR突变肺腺癌转化为小细胞癌的特征。由于Rb1和p53在基线时就已失活,可能存在其他尚未明确的机制,在TKI压力下促使其表型转变为小细胞癌,其中PTEN缺失是一个值得进一步分析的潜在因素。“小细胞转化”可能代表了肺腺癌细胞的动态谱系可塑性,且与其他耐药机制并不相互排斥。基线Rb1缺失有可能作为小细胞转化的组织学预测指标,但这需要在更大的队列中进行前瞻性验证。
参考文献:
Nambirajan A, Rathor A, Baskarane H, Gs A, Khurana S, Sushmitha S, Sharma A, Malik PS, Jain D. Baseline retinoblastoma transcriptional corepressor 1 (Rb1) functional inactivation is a pre-requisite but not sufficient for small-cell histological transformation in epidermal growth factor receptor (EGFR) mutant lung adenocarcinomas post-tyrosine kinase inhibitor therapy. Virchows Arch. 2025 Feb 21. doi: 10.1007/s00428-025-04054-0. Epub ahead of print. PMID: 39982521.



