Gut:胃部微生物群诱导恶性肿瘤前期病变
时间:2021-08-22 08:02:39 热度:37.1℃ 作者:网络
胃癌(GC)是导致全世界癌症相关死亡率的一大病因。尽管遗传因素或行为风险可能导致GC,但同时,它是由微生物致癌物--幽门螺旋杆菌--引起的最具代表性的癌症实例,幽门螺旋杆菌是第一个被公认的细菌致癌物。幽门螺杆菌感染会引发慢性浅表性胃炎(CSG),根据Correa广泛接受的级联理论,依次出现顶细胞丧失的萎缩、肠化生(IM)和发育不良,最终导致GC。高酸度的胃环境限制了微生物的生长,从而降低了进入消化道的病原体的感染风险。随着胃癌发生级联的进展,由于顶细胞丧失导致的胃酸分泌减少,使得慢性萎缩性胃炎发生后各种细菌的定植和过度生长。
幽门螺杆菌在GC发展中的作用,包括其毒力、遗传多样性和宿主的炎症反应,已经被广泛研究。有趣的是,幽门螺杆菌诱导的GC的易感性已经被发现是不同的,只有少数幽门螺杆菌感染者最终会发展为癌症。因此,非幽门螺杆菌的胃部微生物也可能与幽门螺杆菌一起参与致癌:事实上,在胃癌患者中,已检测到高含量的肠道共生菌,而幽门螺杆菌的含量较低。胃微生物群的动态也取决于胃蛋白酶原I/II的比例,抑酸药物的使用,如质子泵抑制剂,以及疾病状态。胃微生物群的结构在整个Correa的级联中可以有很大的变化,表明生物群失调与GC的进展有关。

为了更好地了解胃癌发生的生物学特性,小鼠模型可以提供一个良好的研究系统,以评估在不同疾病阶段从人类采集的胃微生物群落的功能特性。转基因胰岛素-胃泌素(INS-GAS)小鼠可以自发地发展为胃腺癌,此外,小鼠感染小鼠适应性的螺旋杆菌会加速疾病进展,这是最被广泛接受的小鼠GC模型。 然而,在这些模型中,促进循环胃泌素升高的宿主因素可引起慢性胃炎和消化道肿瘤。
尽管除幽门螺旋杆菌外的微生物也可能有助于胃癌的发生,但目前,用于研究人类胃部微生物群在这一过程中的作用的野生型无菌(GF)小鼠模型还没有出现。最近,研究人员评估了移植了来自不同胃病患者的胃微生物群的GF小鼠胃的组织病理学特征,以及它们与微生物群的关系。
在这项研究中,研究人员分析了12名胃发育不良或胃癌患者的胃冠、胃窦组织和胃液中的微生物群概况。此后,将慢性浅表性胃炎、肠化生或GC患者(分别为n=15和n=12)的胃冠和胃窦组织及胃液接种到42只GF C57BL/6小鼠身上。研究人员通过扩增子测序对胃部微生物群进行分析。接种后1个月,研究人员对小鼠胃部的组织病理学特征进行免疫组织化学分析,还对另外15只独立的GF小鼠进行了1年的分析。
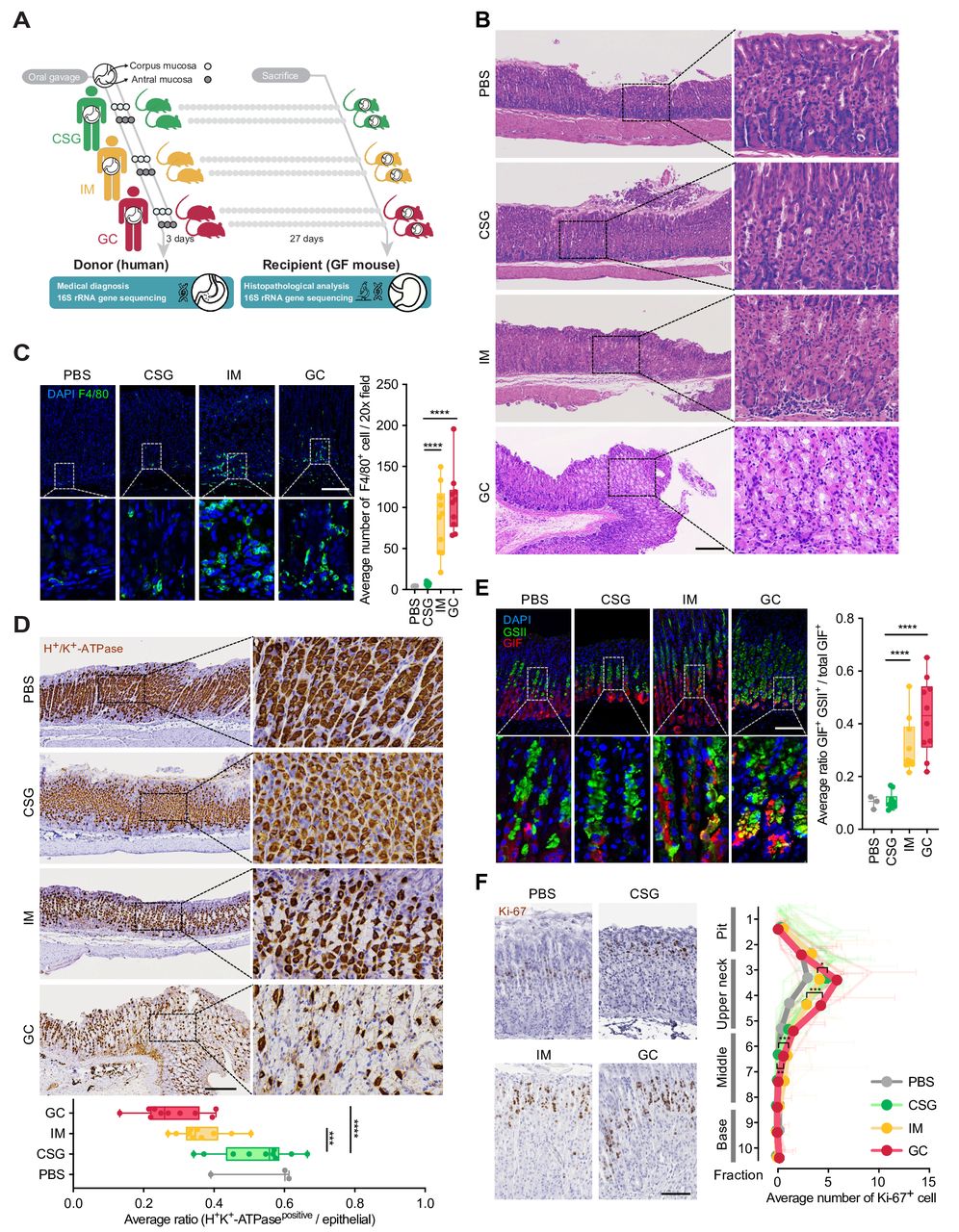
用人类内窥镜活检组织移植的无菌(GF)小鼠胃的组织病理学分析
结果显示,发育不良或GC患者的胃冠和胃窦的微生物群落结构相似。肠化生或GC患者的胃微生物群选择性地定植于小鼠胃部,并诱发恶性肿瘤前的病变:顶细胞的丧失和炎症灶的增加,F4/80和Ki-67的表达,以及CD44v9/GSII凝集素的表达。接种后1年时,研究人员注意到了明显的小鼠发育不良变化。
因此,该研究表明,恶性肿瘤前期的主要组织病理学特征在移植了来自肠化生或GC患者的胃微生物群的GF小鼠中是可重复的。GF小鼠对于研究人类胃部微生物组的功能是有用的。
原始出处:
Soon-Kyeong Kwon et al. Human gastric microbiota transplantation recapitulates premalignant lesions in germ-free mice. Gut (2021).



