智飞生物发布重组新冠疫苗Ⅲ期临床关键数据:总保护效率82%、Delta保护率78%
时间:2021-08-28 12:01:30 热度:37.1℃ 作者:网络

智飞生物公告
8月27日晚间,智飞生物发布公告称,与中科院微生物所合作研发的重组新型冠状病毒疫苗获得Ⅲ期临床试验关键性数据。Ⅲ期临床试验关键数据结果证明,重组新型冠状病毒疫苗(CHO细胞)在符合本临床试验方案的人群中具有很好的安全性和防病效果。
公告称,该疫苗自2020年12月12日开始,陆续在我国湖南省、乌兹别克斯坦、印度尼西亚、巴基斯坦和厄瓜多尔开展国际多中心Ⅲ期临床试验,计划入组18周岁以上普通人群共计29000人,按照0、1、2月的免疫程序共接种3剂疫苗。
截止到本次数据分析日,实际共入组28500人,其中疫苗组14251例、安慰剂组14249例。共监测到全程接种后的主要终点病例数221例,对于任何严重程度的COVID-19的保护效力为81.76%,达到WHO要求的新冠疫苗有效性标准。其中对于COVID-19重症及以上病例、死亡病例的保护效力均为100%。
目前已完成大部分主要终点病例的基因分型,初步分析结果显示:对Alpha变异株的保护效力为92.93%;对Delta变异株的保护效力为77.54%。
本研究安全性数据结果显示:总体不良事件/反应的发生率,疫苗组与安慰剂组无显著差异,安全性良好。已完成的Ⅲ期临床试验关键数据结果证明,重组新型冠状病毒疫苗(CHO细胞)在符合本临床试验方案的人群中具有很好的安全性和防病效果。
对比全球主要获批上市和紧急使用新冠疫苗的III期临床数据,智飞生物重组新冠疫苗的综合保护率居前,且是唯一对野生株和主要变异株完成完整三期临床试验的新冠疫苗。
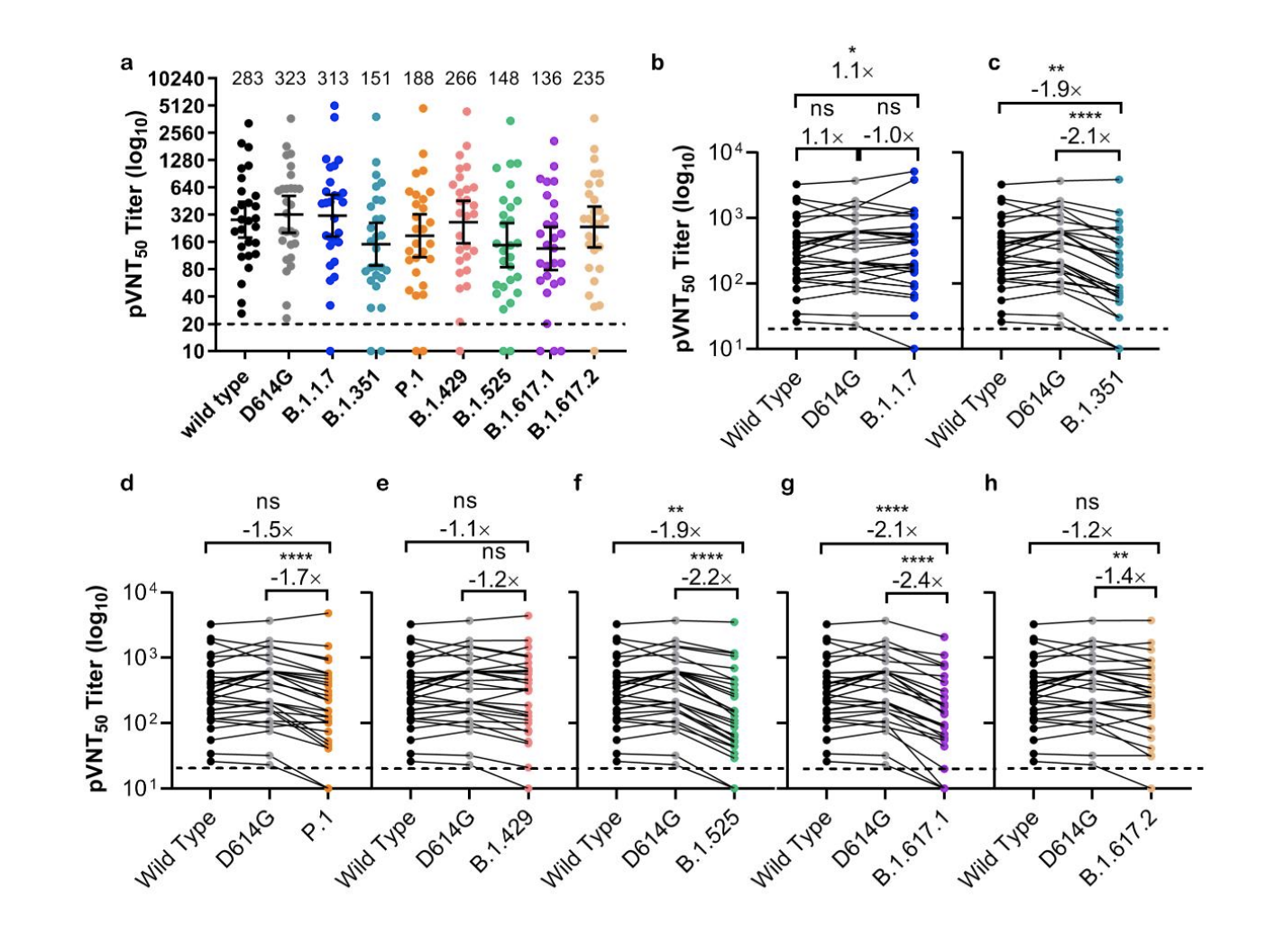
ZF2001中和三种SARS-CoV-2变异假病毒血清样本抗体滴度水平。
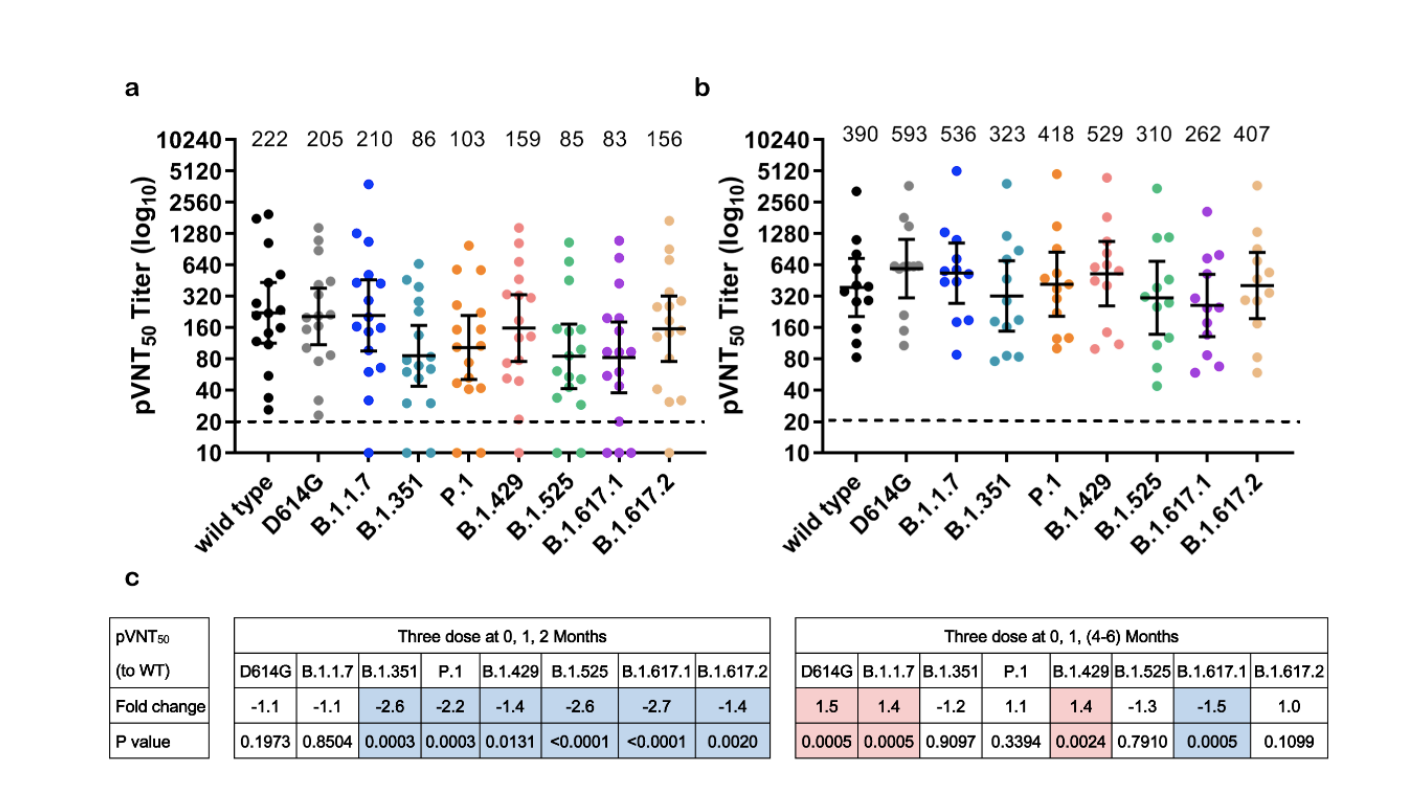
接受三剂ZF2001受测者血清样本抗体水平
7月15日,智飞生物与中国科学院微生物研究所在预发表平台bioRxiv上发表实验结果称,以模拟Delta变体颗粒进行测试,与早先出现的病毒颗粒相比,接种过智飞三剂疫苗者的血清样本显示其中和抗体降低了1.2倍。科研人员指出,仍需要来自临床试验或实际使用的数据来确定疫苗对病毒变体的防护力。该研究采用了28名受测者样本。试验结果也发现,施打第二剂和第三剂疫苗的间隔时间较长者,对新冠病毒变体的活性更大。
智飞的ZF2001疫苗已在中国和乌兹别克斯坦获得紧急授权使用,目前已生产超过1亿剂。


