Eur Respir J:新冠病毒和流感病毒感染的特异性宿主反应与基因特征
时间:2021-10-28 16:01:45 热度:37.1℃ 作者:网络
重症新冠肺炎通常并发血管疾病和凝血功能障碍。包括血管屏障破坏、水肿、内皮炎和血栓形成。血栓和微血管并发症在死亡患者中经常被记录,表明血管病变是重症患者的主要驱动因素。虽然这些机制促进疾病进展,但尚不清楚哪些机制是导致死亡的主要因素。
发表在Eur Respir J杂志的一项研究验证了临床研究中提出的新冠肺炎生物标志物,探索其发病机制,以更好地定义宿主对新型冠状病毒感染的反应。

研究人员从10例死于呼吸衰竭的新冠肺炎患者和5例H1N1流感患者的尸检肺组织中提取组织芯片(TMA)。对照组材料取自4名未感染患者。病例组样品固定在10%福尔马林溶液中至少24小时,直到封闭和切片进行显微镜分析。用苏木精和尹红对肺福尔马林固定石蜡包埋(FFPE)样本进行染色,观察肺组织病理学变化,并构建TMA。研究人员使用Nanostring GeoMXTM平台对FFPE组织进行靶向转录组学研究,以深入了解新冠肺炎、H1N1流感和未感染对照患者肺转录组情况。
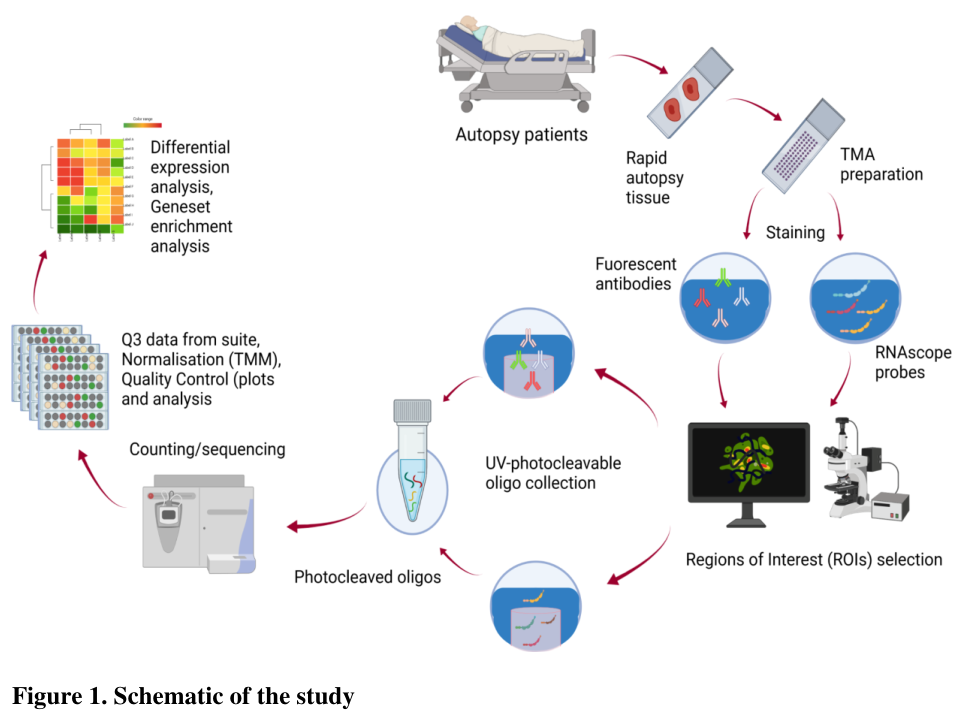
宿主转录组学显示,与未感染对照组相比,新冠肺炎患者肺部炎症、I型干扰素产生、凝血和血管生成相关基因显著上调。高病毒载量新冠病毒感染核心与其他核心相比,只有17个基因表达上调和7个基因差异下调。新冠病毒特异性基因S和ORF1ab是高病毒载量组中最强烈上调的基因(分别为1.916和1.861 log2倍变化)。
新型冠状病毒在肺部的不均匀分布,高病毒载量区域与I型干扰素应答增加有关。一旦样本中存在的优势细胞类型、患者内相关性和患者变异得到控制,重症流感患者和新冠肺炎患者的肺部差异表达的基因数量非常有限。值得注意的是,与流感患者相比,新冠肺炎患者肺部的干扰素相关基因IFI27(被认为是区分细菌和病毒性肺部感染的血液生物标记物)显著上调。

数据表明,空间转录组学是识别组织内新基因特征的有效工具,为新冠肺炎的发病机制提供新见解,有助于患者分诊和治疗。
原文出处:
Kulasinghe A, Tan CW, dos Santos Miggiolaro AFR, et al. Profiling of lung SARS-CoV-2 and influenza virus infection dissects virus-specific host responses and gene signatures. Eur Respir J 2021; in press (https://doi.org/10.1183/13993003.01881-2021).



