梅斯盘点:2021年度肺癌领域十大进展
时间:2021-12-31 10:11:53 热度:37.1℃ 作者:网络
合集:2021年度十大进展
肺癌在2021年度,虽然整体仍然沿续过往一些主要思路,但是也有很多突破,包括一些少见靶点的治疗方面突破比较显眼。同时,KRAS,以及免疫增强剂等新型的治疗药物,也取得初步效果。梅斯医学为您盘点2021年度肺癌领域的进展。
1、KRAS抑制剂在肺癌中初获成功
KRAS突变是NSCLC常见突变类型,在肺腺癌中发生率更高,约为25%~30%,最常见的突变位点是G12C(39%),其次为G12V(21%)、G12D(17%)。近年来,直接靶向KRAS蛋白的小分子TKI相继被开发并进入临床研究。
Sotorasib(AMG 510)是KRAS G12C突变蛋白抑制剂,与突变KRAS蛋白的12号半胱氨酸(G12C)进行不可逆的结合抑制下游通路。2021年的ASCO年会公布了AMG 510治疗KRAS G12C突变NSCLC的II期CodeBreaK100研究的最新数据[14],Sotorasib组的ORR达到37.1%,中位PFS为6.8个月,DCR为80.6%,中位OS为12.5个月。
2021年的WCLC年会报道了CodeBreaK100研究的基线脑转移的亚组数据[15],基线脑转移患者的中位PFS为5.3个月,中位OS为8.3个月;在16名可评估的脑转移患者中,颅内DCR为88%(14/16)。此外,WCLC 2021年会还报道了CodeBreaK100研究的探索性分析初步结果[16],Sotorasib在STK11突变同时伴有野生型KEAP1的组中疗效改善,而KEAP1突变组似乎获益较少,提示KRAS G12C突变NSCLC对Sotorasib的反应可能取决于共突变状态。
KRAS抑制剂JDQ443在临床前研究中初步显示出有潜力的抗肿瘤活性。目前,一项全球开放性多中心KRAS G12C突变晚期实体瘤患者中JDQ443剂量爬坡的Ib/II期研究正在进行中。同时,该研究还设置了多个队列,以探索联合治疗方式克服耐药。
2、辅助化疗中添加免疫治疗的获益研究
IMpower010研究:是一项随机、开放标签的全球多中心 III 期临床研究,探索在辅助化疗中添加阿替利珠单抗的获益。该研究纳入1280名患已完全切除的 IB-IIIA 期 NSCLC 和 ECOG PS 0-1的患者,接受-顺铂的化疗(加上培美曲塞、多西他赛、 吉西他滨或长春瑞滨),21天/周期,共4周期。然后1005名患者按1:1随机分配至Atezolizumab 1200mg Q3W组(16个周期或直到疾病复发或不可接受的毒性)或最佳支持治疗组(BSC)。对复发部位和复发后的后续治疗进行了探索性分析。
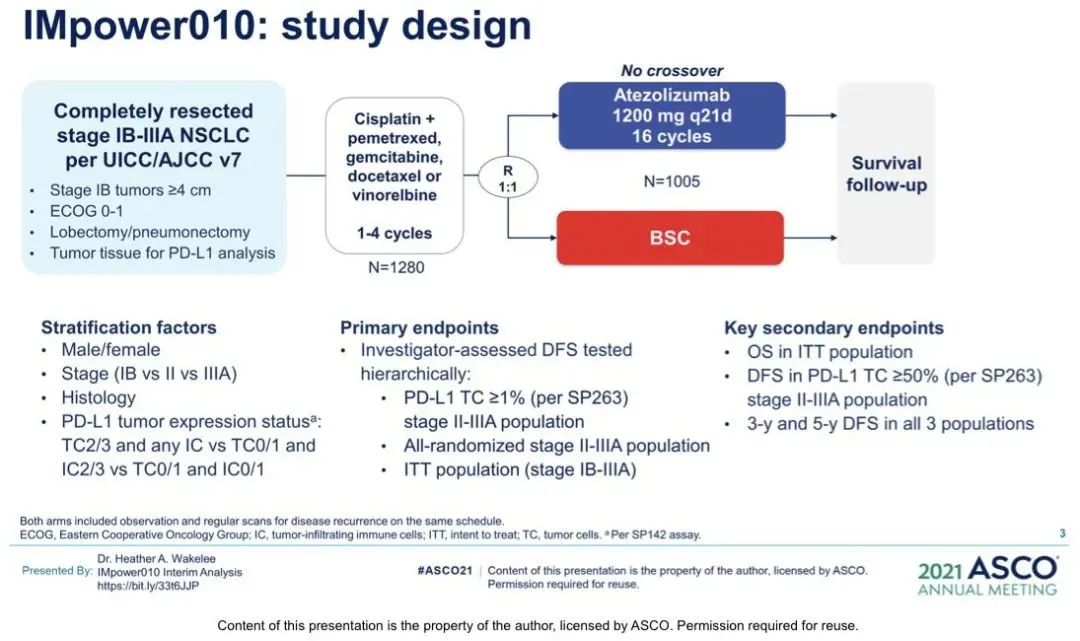
研究设计
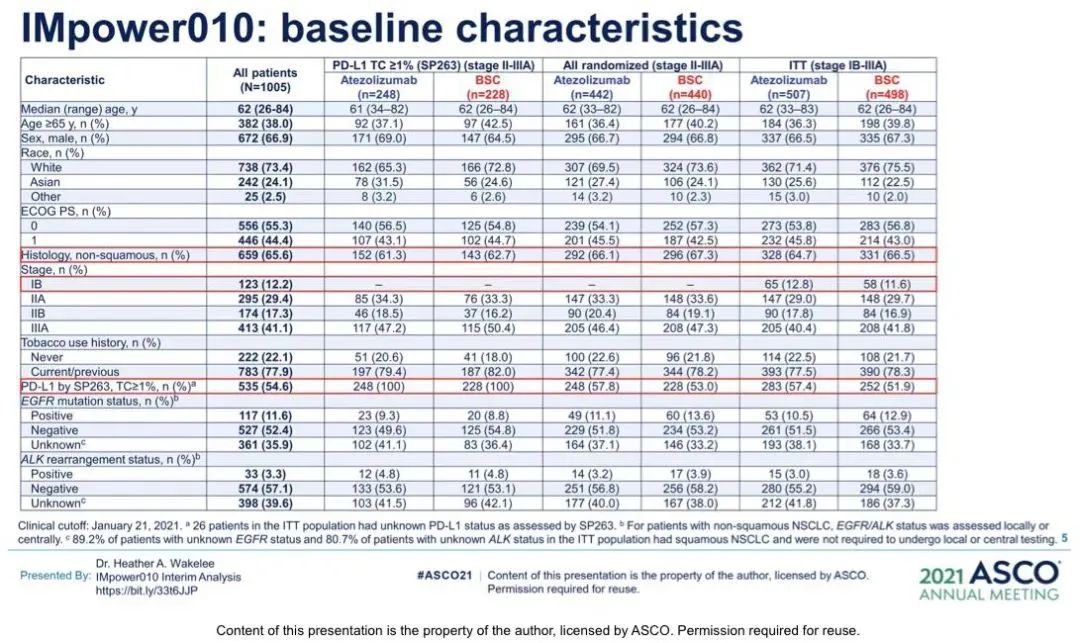
基线特征
研究结果:在 PD-L1 TC≥1% II-IIIA 期(HR [95% CI] 0.66 [0.50, 0.88])和所有随机II-IIIA期(HR 0.79 [0.64 , 0.96]) 患者的DFS出现显著性边界交叉。在所有随机分配的 II-IIIA 期患者中,随着PD-L1表达的增加,观察到DFS的改善【TC <1%,0.97 (0.72, 1.31);TC 1-49%,0.87(0.60, 1.26);TC 50%,0.43(0.27, 0.68)】。在PD-L1 TC ≥1%的 II-IIIA 期患者中,Atezolizumab组有73名(29%)复发,而BSC组有102名(45%)复发。本研究提示DFS中期分析中,BSC组的复发率高于Atezolizumab组,但复发患者之间的复发模式没有明显差异。BSC组复发后CIT的使用率更高。
3、肿瘤疫苗的探索,结果初现
Atalante-1研究:一项随机III期临床研究,旨在评估OSE2101【Tedopi,一种抗癌疫苗(修饰表位仅限于来自 5 种肿瘤相关抗原的 HLA-A2+)】对比标准治疗(多西他赛或培美曲塞)在免疫检查点抑制剂治疗失败后的NSCLC患者中的有效性和安全性。
研究结果显示,研究纳入219名EGFR和ALK阴性的NSCLC ,ECOG PS 0-1患者,随机2:1接受OSE2101皮下Q3W治疗6个周期,随后Q8W维持1年,Q12W直到进展,与标准治疗(多西他赛或培美曲塞 Q3W)比较。主要研究终点为OS,次要终点为DCR、生活质量QoL。
OSE2101组 vs 标准治疗组,OS分别为11.1、7.5个月 [HR 0.59(0.38-0.91)p = 0.02]。6个月的DCR为25% vs 24%(NS),mPFS为2.7个月vs 3.4个月(NS),ORR为8% vs 18%(p=0.07)。
OSE2101组 vs 标准治疗组,进展后生存期为7.7个月 vs 4.6个月 [HR 0.46 p=0.004],ECOG PS恶化时间为8.6个月 vs 3.3个月 [HR0.45 p=0.0005]。OSE2101的QoL全球健康状况保持不变(p<0.05)。 严重不良事件分别为38%与68%(p<0.001)。与标准治疗相比,OSE2101在晚期HLA-A2+ NSCLC患者中具有良好的获益/风险。在免疫检查点抑制剂继发性抵抗的患者中,OS的HR从0.86改善为0.59,OSE2101的中位OS显著增加了3.6 个月。
4、免疫增强剂在肺癌治疗中的应用
DUBLIN-3研究:是一项国际多中心、III 期、随机对照临床研究,旨在评估普那布林(一种新型免疫增强小分子,可增强树突细胞成熟和T细胞增殖)+多西他赛对比单药多西他赛在EGFR野生型NSCLC二/三线治疗中的安全性和有效性。研究在全球共纳入559例受试者,按1:1随机分组,两组受试者均在每个化疗周期(21天)的第1天接受75 mg/㎡多西他赛给药,联合治疗组在第1天多西他赛给药后1小时和第8天给予30 mg/㎡普那布林。研究的主要终点为OS,次要终点包括:ORR、PFS、4级中性粒细胞减少症的发生率、24个月 OS 率、36 个月OS率、48个月OS率等。(#LBA48)研究结果:相较于单用多西他赛组,普那布林联合多西他赛组的平均OS为15.08个月vs 12.77个月,中位OS为10.5个月vs 9.4个月, 24个月OS率(22.1% vs 12.5%)、36个月OS率(11.7% vs 5.3%)以及48个月OS率(10.6% vs 0%),显示出该联合方案具有持久的抗癌获益。
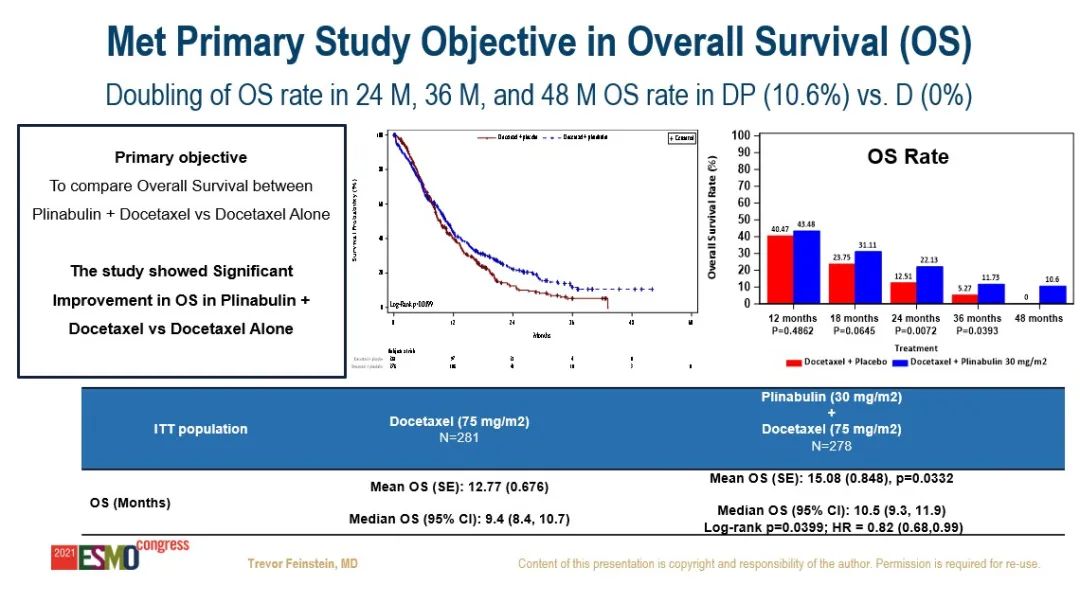
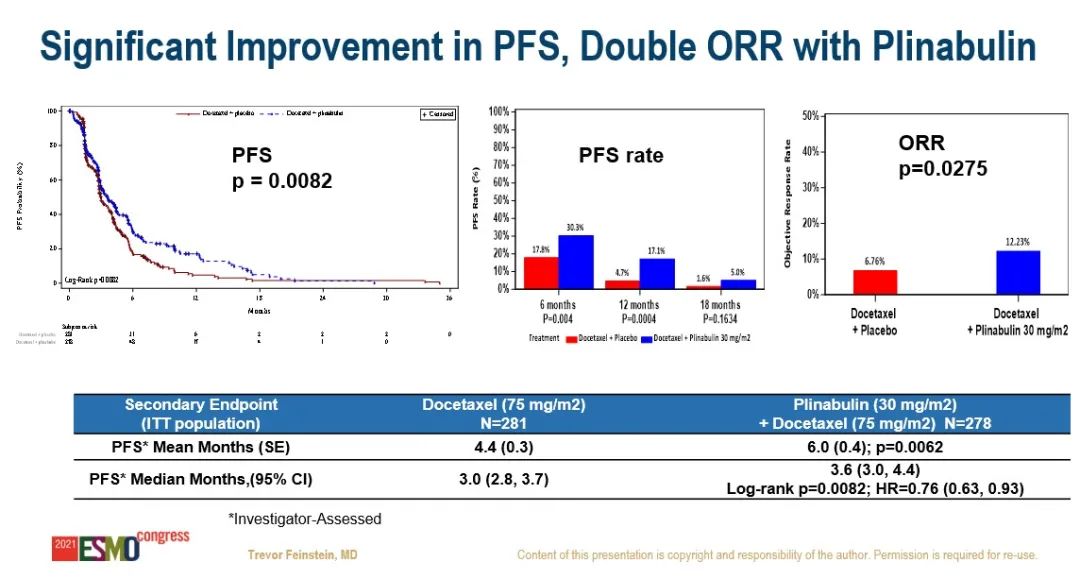
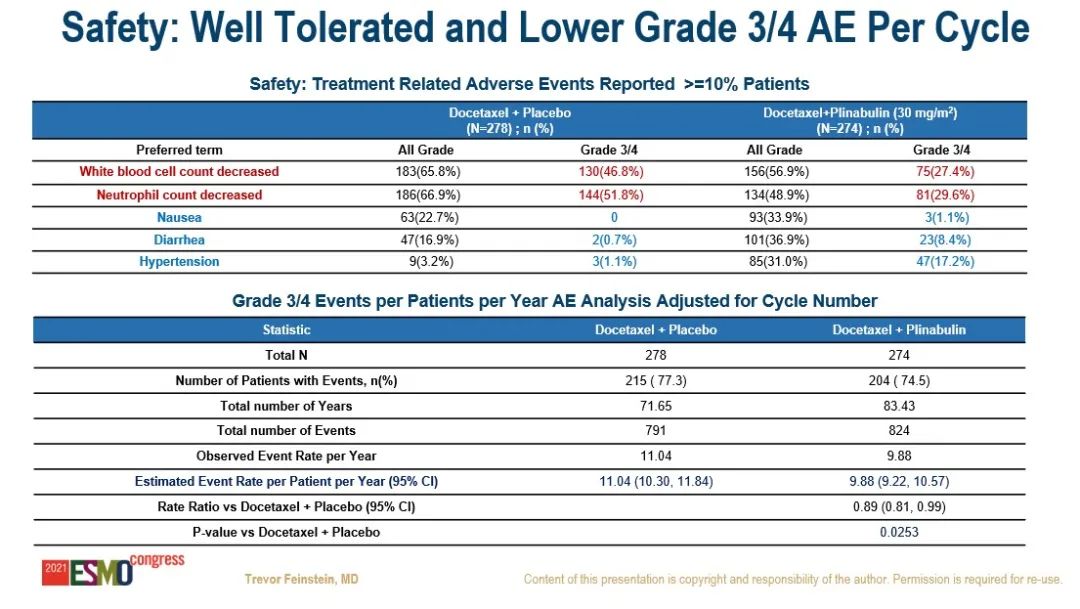
平均PFS为6.0个月vs 4.4个月,中位PFS为3.6个月vs 3.0个月,ORR为12.23% vs 6.76%,4级中性粒细胞减少症的发生率显著下降(第一疗程第8天:27.8% vs 5.26%;全部疗程第8天:33.58% vs 5.13%)。安全性方面,联合治疗组的耐受性良好,相较于对照组,患者生活质量更好。
5、达拉非尼联合曲美替尼组成的双靶方案用于BRAF V600E在肺腺癌治疗,写入指南
2021年WCLC年会和ESMO年会上公布的最新中国人群流行病学数据显示,BRAF基因突变发生率约为1.78%~3.15%[5,6],其中BRAF V600E在肺腺癌中最常见。目前,达拉非尼联合曲美替尼组成的双靶方案(D+T方案)已经成为指南(包括NCCN指南、ESMO指南和CSCO指南)的优先推荐。
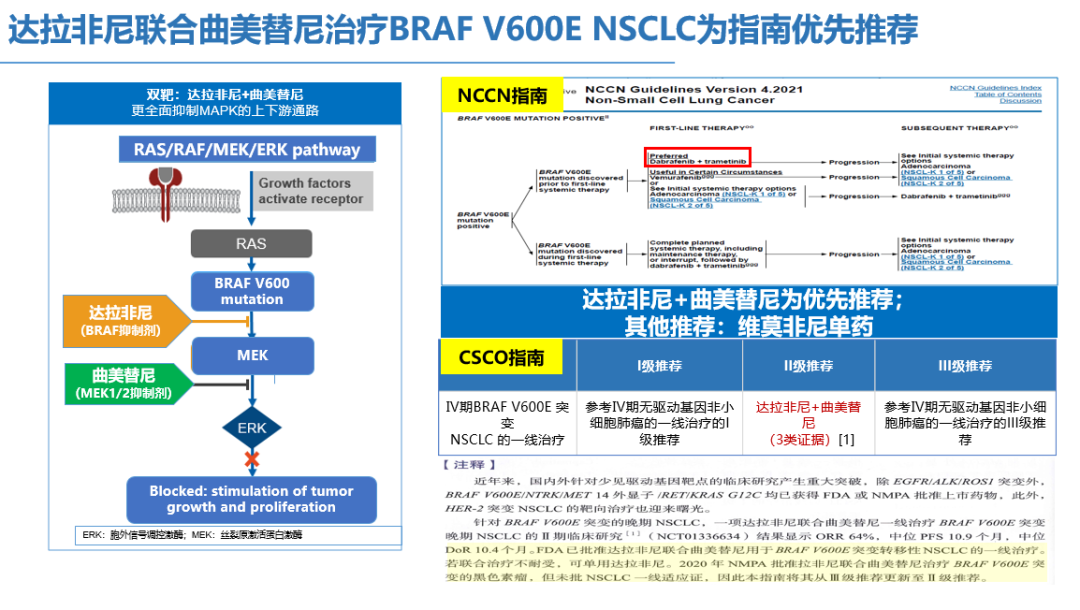
图2 BRAF V600突变肺癌治疗指南推荐
指南的推荐基于一项名为BRF113928研究的II期临床试验,最近更新的数据显示初治和经治的晚期BRAF V600E突变NSCLC患者,采用达拉非尼联合曲美替尼治疗的ORR分别为63.9%和68.4%,中位PFS分别为10.8个月和10.2个月,中位OS分别为17.3个月和18.2个月。
ESMO 2021年会报道了一项纳入63051例患者的真实世界研究[8],与BRF113928研究中总体人群24.6个月的中位OS相比,达拉非尼联合曲美替尼在真实世界中展现出更长的生存获益(29.3个月)。
6、MET抑制剂捷报频传,Capmatinib、Tepotinib、和Savolitinib疗效不断公开
MET ex14跳突患者传统化疗和免疫治疗的效果欠佳,近年来MET抑制剂捷报频传,Capmatinib、Tepotinib、和Savolitinib相继获批上市。Capmatinib一线治疗MET ex14跳突的ORR达68%,是目前治疗MET ex14跳跃突变最高效的靶向药物,并具有优秀的颅内控制。同时,一线治疗ORR高于二线治疗的40.6%,因此推荐尽早使用。此外,Tepotinib在老年患者中疗效和安全性得到证实。Amivantamab在MET ex14跳跃突变中也进行了探索并显示出良好疗效,MET ex14跳跃突变或再添新药物。
GEOMETRY mono-1研究的MET ex14跳跃突变队列更新数据,接受Capmatinib一线治疗患者(n=28,cohort 5b)的ORR高达67.9%,中位DOR为11.14个月,中位PFS达12.4个月,中位OS达20.8个月。接受Capmatinib二线治疗患者(n=69,cohort4)的ORR为40.6%,中位DOR为9.7个月,中位PFS为5.4个月,中位OS达13.6个月。
VISION研究的亚组分析结果,在按年龄划分的亚组(<75岁和≥75岁)中,Tepotinib均显示出了相似的疗效和安全性。VISION研究入组了大量MET ex14跳跃突变的老年NSCLC患者,<75岁人群(n=157)的ORR为52.2%,疾病控制率(DCR)为74.5%;≥75岁人群(n=118)的ORR为44.9%,DCR为75.4%。
CHRYSALIS研究的初步结果,Amivantamab在MET ex14跳跃突变NSCLC患者中显示出抗肿瘤活性,64%(9/14)的可评估患者出现部分缓解,中位治疗时间6.5个月。
7、Selpercatinib和普拉替尼用于RET融合患者的疗效数据让人印象深刻
NSCLC中RET重排的发生率约有1%~2%,常见于年轻、不吸烟的肺腺癌患者。国际上众多已经上市的RET-TKI包括凡德他尼、卡博替尼、Selpercatinib(LOXO-292)和普拉替尼(BLU-667)。其中普拉替尼(BLU-667)已于今年在中国获批上市。
WCLC 2021年会报道的LIBRETTO-321研究带来了Selpercatinib的中国人群数据。这是一项在中国进行的II期临床研究,在47例RET融合阳性患者中,初治患者的ORR为90%,经治患者的ORR为58.3%。这与先前报道的LIBRETTO-001研究结果一致。
针对普拉替尼的ARROW研究是一项全球性I/II期临床研究,WCLC 2021年会公布了ARROW研究的中国队列数据,既往接受过化疗的患者ORR为66.7%,DCR为93.9%;此前未经治疗的患者ORR为80%,DCR为86.7%。在中国人群中观察到的疗效结果与ARROW研究中此前报道的全球人群疗效结果一致。
8、多个HER2抑制剂在NSCLC中获得疗效突破
在NSCLC中,HER2基因突变表现为基因扩增和突变,20外显子插入突变(HER2 exon20)最为常见,3%的NSCLC患者存在HER2基因突变。目前NCCN指南仅推荐抗体偶联药物治疗HER2阳性NSCLC患者,包括T-DM1和DS-8201。
DESTINY-Lung01是一项评估DS-8201用于HER2过表达和HER2突变晚期NSCLC患者的多中心II期临床研究,ESMO 2021年会公布了HER2突变队列的数据,ORR达54.9%,DCR达92.3%,中位PFS为8.2个月,中位OS为17.8个月,在不同HER2突变亚型患者中均表现出活性。
2021年ASCO年会报道了吡咯替尼联合阿帕替尼治疗33例经治HER2突变NSCLC的II期临床研究数据,总体的中位PFS为6.8个月,中位OS未达到;基线脑转移患者的ORR为46.2%(6/13),无脑转移患者的ORR为45.0%(9/20),二线治疗患者ORR为47.1%(8/17),三线及以上患者的ORR为43.8%(7/16)。
ASCO报道的另一项II期临床研究显示,曲妥珠单抗、帕妥珠单抗和多西他赛三联疗法在晚期HER2突变NSCLC患者中,ORR为28.9%,缓解持续时间(DOR)为11.0个月,中位PFS为6.8个月,中位OS为17.6个月。
ESMO报道了Poziotinib治疗48例未经治疗的HER2 exon20突变NSCLC的初步数据,ORR为43.8%,DCR为75%,中位PFS为5.6个月。
9、帕博利珠单抗用于早期NSCLC新辅助治疗的最终安全性分析、主要研究终点和更新的疗效结果
研究结果显示,帕博利珠单抗用于早期NSCLC的新辅助治疗,MPR率为27%,pCR率为12%,3~4级TRAE率为8%。RP2D/S推荐以三周为间隔注射两剂帕博利珠单抗新辅助治疗,两周后进行手术。从治疗到手术的较长间隔与较高的MPR率相关。
10、小细胞肺癌缓慢进展,D + EP作为扩展期SCLC的标准治疗(CASPIAN研究)
一项评估依托泊苷 + 顺铂/卡铂(EP) ± 度伐利尤单抗(D) ± Tremelimumab(T)一线治疗ES-SCLC的III期研究,与单纯EP相比,D + EP可见显著OS获益(数据截止日期[DCO]: 2019-3-11;HR 0.73 [95% CI 0.59=0.91; p=0.0047])。中位随访25.1个月(DCO 2020-1-27)的后续分析显示,D + EP vs EP的OS获益稳定(HR 0.75 [95% CI 0.62-0.91;nominal p=0.0032]);与单纯EP相比,D + T + EP有OS数值改善(HR 0.82 [95% CI 0.68-1.00;p=0.0451]),但未达到统计学差异(p≤0.0418)。本次更新中位随访>3年的OS数据,是截至目前EP+PD(L)1的III期研究报告的最长时间结果。(#LBA61) 研究方法:既往未接受治疗的ES-SCLC患者按照1:1:1随机分组:D 1500 mg + EP q3w;D 1500 mg + T 75 mg + EP q3w;EP q3w。IO组患者接受4周期EP + D ± T,随后D 1500 mg q4w维持治疗。EP组患者接受最多6周期EP。主要终点为D + EP vs EP和D + T + EP vs EP的OS。在长期随访期间评估严重AEs(SAEs)。 研究结果:D + EP组、D + T + EP组和EP组的患者数分别为:268、268和269。截至2021-3-27, 中位随访39.4个月,成熟度86%。与EP相比,D + EP继续显示OS获益:HR 0.71 (95% CI 0.60-0.86;nominal p=0.0003)。D + EP vs EP:中位OS 12.9个月 vs 10.5个月;24个月OS率22.9% vs 13.9%;36个月OS率17.6% vs 5.8%。与EP相比,D + T + EP继续显示OS数值改善:HR 0.81(95% CI 0.67-0.97; nominal p=0.02);中位OS为10.4个月,36个月OS率为15.3%。在截止日,46例患者继续接受D治疗(D + EP组27 例,D + T + EP组19例)。D + EP、D + T + EP和EP的安全性分别为:SAEs(所有原因)32.5%、 47.4%、36.5%;导致死亡AEs(所有原因)5.3%、10.9%、6.0%。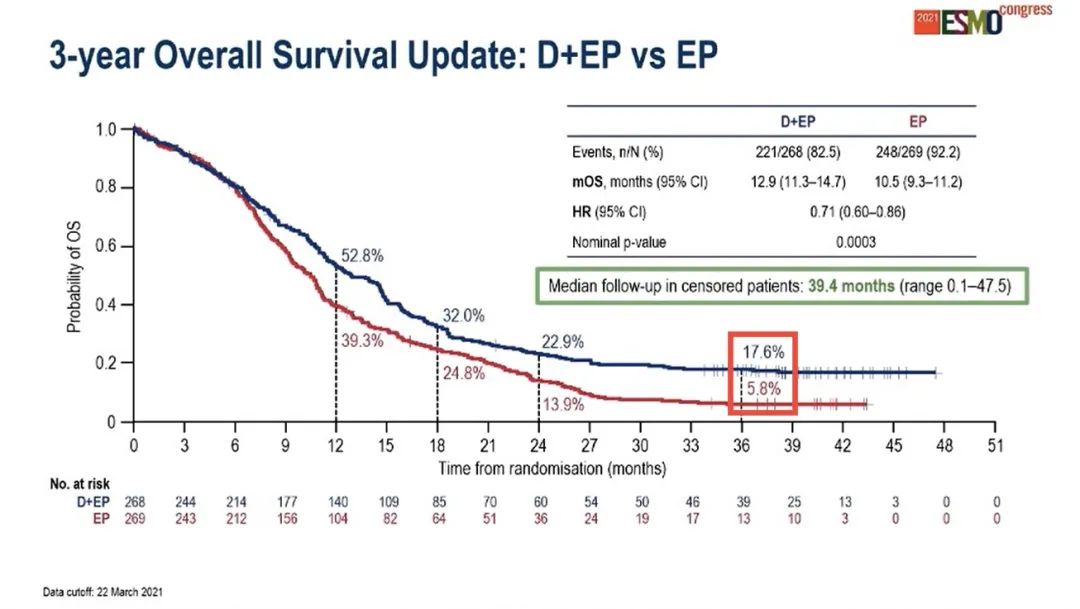
CASPIAN 研究3年OS数据
与既往分析一致,中位随访>3年后,D + EP表现出比EP更持久的OS获益和良好的安全性。接受D + EP治疗的患者在第3年时的生存率是单纯EP组的3倍,进一步确立了D + EP作为ES-SCLC一线治疗的标准治疗方案。

