病例分享 | 青年女性反复腹痛伴腹水,最终竟为罕见病?
时间:2024-08-26 06:00:32 热度:37.1℃ 作者:网络
腹痛、腹胀是消化科的常见症状,它们看似简单,实则背后可能隐藏着错综复杂的病因。对于许多患者来说,这些症状可能只是短暂的不适,但对于某些患者而言,他们却长期被这些症状困扰着。今天,我们为大家分享一位发作性腹痛、腹水的青年女性,由于未找到明确病因,她4年间不得不反复住院治疗,幸运的是,其所患疾病终于在山东大学齐鲁医院消化内科得以确诊。接下来,让我们一起跟随她的诊疗足迹,探寻罕见病HAE的奥秘。
病例回顾
不明原因反复腹痛,终在消化科寻得线索
患者青年女性,35岁,主诉“腹痛、腹胀4年,加重5天”。
患者最早于2020年10月出现腹痛、腹胀。腹痛性质剧烈,腹痛从中上腹部开始,最后表现为全腹痛。偶伴恶心、呕吐,不伴发热、便秘等。遂于当地医院妇科住院治疗,行常规化验示血象、CRP(C反应蛋白)升高;子宫附件彩超、胃肠镜、胸部CT等未发现特殊异常,盆腹MRI显示腹盆腔大量积液。给予相应对症治疗后患者好转出院。
一个月后患者再次出现上述症状,就诊于当地医院感染科,行泌尿系超声未发现异常,腹部彩超提示大量腹水,于是行彩超下腹腔积液穿刺置管引流,再次好转出院。几年间,患者腹痛症状反复,均于当地医院住院治疗,对症治疗后好转出院,这样的“剧情”不知道反复上演了多少次,对她的生活造成极大的影响。
2024年3月13日,患者再次出现剧烈腹痛,就诊于当地医院行腹部彩超提示腹腔积液,部分肠管壁增厚;盆腔积液。为求进一步诊疗,3月15日就诊于我院急诊科,血液化验示血象、CRP升高,D-二聚体 8.34ug/ml(0~0.5ug/ml), FDP 24.47ug/ml(<5ug/ml),因此,行肠系膜动静脉血管成像排除了肠系膜血栓。腹部CT平扫+增强提示腹膜稍厚,盆腔少量积液(图1)。急诊给予对症处理后转入我院消化内科,行相关化验。三大常规、肝肾功、甲功、风湿免疫相关指标、肿瘤指标均正常,病原体检查均未检出。行经口+经肛小肠镜亦未找到“幕后真凶”。
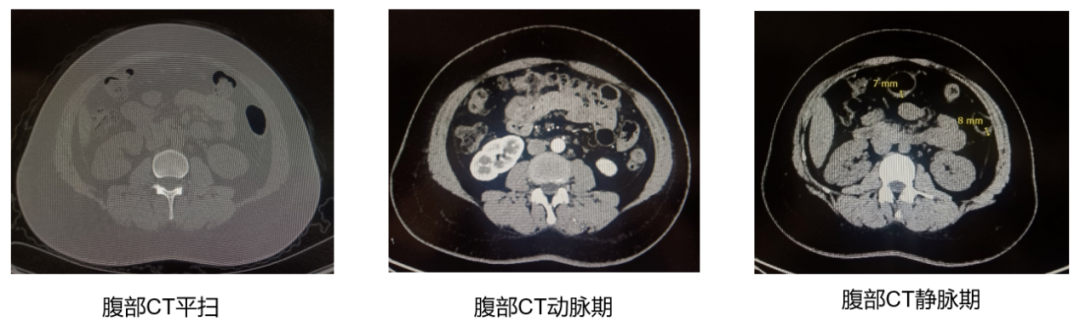
图1 腹部CT平扫+增强检查结果
为了查明患者反复腹痛、腹水的背后的原因,不得不使出大招——全外显子基因检测。经过20多天的漫长等待,终于等到了检测结果。结果发现患者SERPING1基因有1个杂合突变,且患者父亲也存在该杂合突变(图2),提示遗传性血管性水肿1型。这条线索为我们后续的诊疗提供了非常大的帮助。
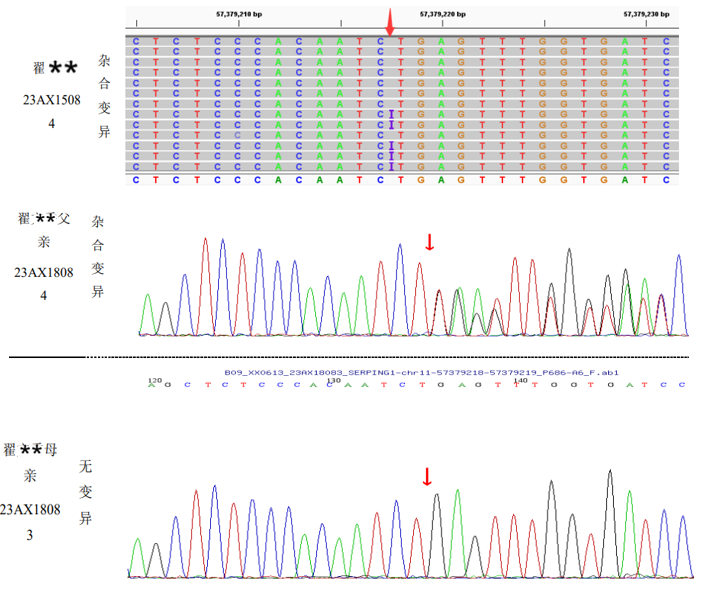
图2 患者及其父母全外显子基因检测结果
进一步明确诊断,回溯病因
遗传性血管性水肿(hereditary angioedema,HAE)是一种罕见的常染色体显性遗传病,主要特征是反复发生的、自限性的皮肤或黏膜水肿,水肿部位以胃肠道和呼吸道最多。胃肠道水肿则会导致剧烈腹痛、伴随恶心、呕吐或腹泻,甚至出现腹腔积液。HAE主要是由于编码C1 酯酶抑制物(C1-INH)的基因SERPING1突变引起。该基因突变导致C1-INH的浓度和(或)功能降低,进而导致缓激肽生成异常和血管通透性增加(图3)[1]。另一方面,C1-INH缺乏会导致C1分子不受控制地自身活化,启动补体经典激活途径,裂解并消耗大量C4,导致患者体内C4的水平低于正常值[2]。在HAE患者中,1型患者的补体C4、C1-INH浓度和功能均低下,2型患者中,补体C4和C1-INH功能低下,但C1-INH浓度正常或稍增高。
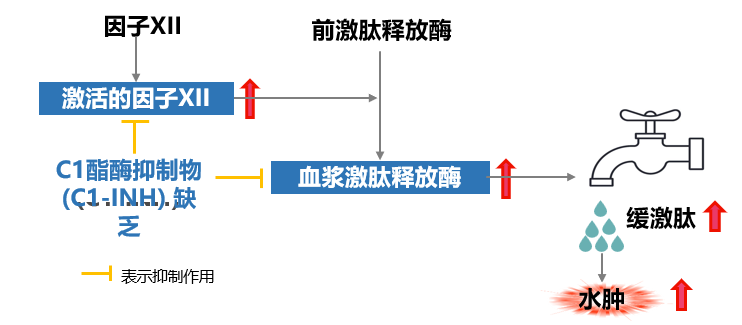
图3 HAE发病机制
因此,进一步检测C4、C1抑制剂浓度和功能。结果示:C4:0.08 g/L(0.1-0.4 g/L),C1 INH浓度 0.04g/L(0.21-0.39 g/L),C1 INH功能 3.6%(≥68%)。根据HAE的分型标准,本病例属于HAE1型,和此前所做的基因检测结果一致。这真是一个令人兴奋的结果,我们终于揭露了“凶手”的真实身份。为了明确患者该致病基因的突变来源,后续对其父母行基因检测。结果提示患者父亲也有上述基因位点的突变,而其母亲则无该位点的突变。
由于HAE有典型的皮肤、黏膜反复发作性水肿的表现,于是追问患者病史。患者表示自己与父母均未出现过皮肤水肿史。但是父亲有间断腹痛史,未行系统诊治。另外,患者回忆自己每次腹痛发作几乎都是处于月经结束后10余天。据以往病例报道,HAE发病的可能诱因包括轻微外伤、感染、情绪、医源性操作、雌激素、ACEI类药物。联想到女性内源性雌激素也是在末次月经结束后10余天达到分泌高峰,我们推测本病例患者的发病诱因可能是患者内源性雌激素的升高,这也可能是患者父亲同样存在基因变异但腹痛症状较轻的原因。
思考与总结
HAE典型特征为皮肤、黏膜反复发作性水肿,但本病例患者无典型皮肤、黏膜水肿表现,加上此前患者的一般化验及辅助检查无特殊指向性,更是加大了诊断难度。该患者在确诊之前多被诊断为女性盆腔炎、腹腔感染、腹腔积液、腹膜炎等。因此,我们再次回顾患者诊疗过程中的一些蛛丝马迹,以便再次面对类似特征的患者时可以想到HAE。临床表现方面,患者腹痛、腹水症状反复发作,经对症治疗后可缓解。实验室检查方面,我们注意到每次症状发作时,患者血象、CRP及D-二聚体升高(图4),病情好转后这些指标又回落至正常水平。影像学检查方面,疾病发作期可有腹水、肠壁水肿等,这些指标的变化、影像学特征与既往报道的病例特点一致。
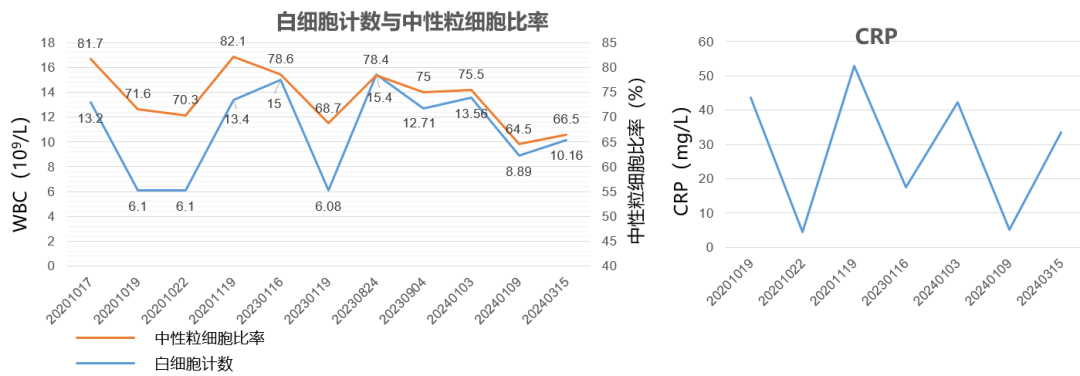
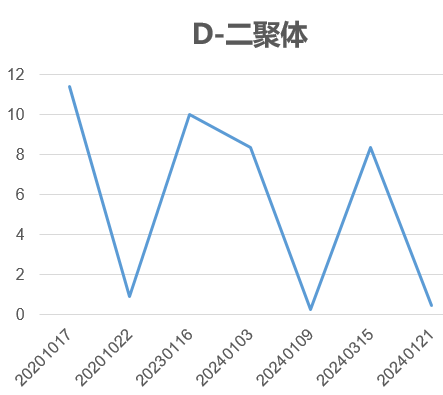
图4 患者WBC、中性粒细胞比率、CRP、D-二聚体指标变化
考虑到72%-97%HAE患者会表现出反复发作的腹痛,应积极进行补体C4初筛
研究显示,21%的HAE患者仅表现为胃肠道症状,其中腹痛在HAE患者中发生率高达93%,高达80%的HAE患者腹痛反复发作[3-4]。然而,由于HAE较为罕见,我国HAE诊断率不足5%,患者从发病到明确诊断,时间跨度长达13年,仅以胃肠道症状为主要或唯一表现的患者甚至更久,给患者带来沉重的疾病负担[5]。
因此,当临床遇到反复发作的腹痛且B超或CT可见肠壁水肿/腹水时,应考虑到HAE的可能。若是初步怀疑HAE,可行C4水平的检测进行初步筛查,简单经济有效,若C4水平低下,可进一步行C1-INH浓度及其功能测定,以明确诊断。随着医学进展,消化科医师对HAE的认识不断提高。令人振奋的是,最近由多位消化科专家共同参与制定的全球首个《遗传性血管性水肿消化科诊疗路径》已经发布,消化科有了属于自己的HAE诊疗路径(图5)。
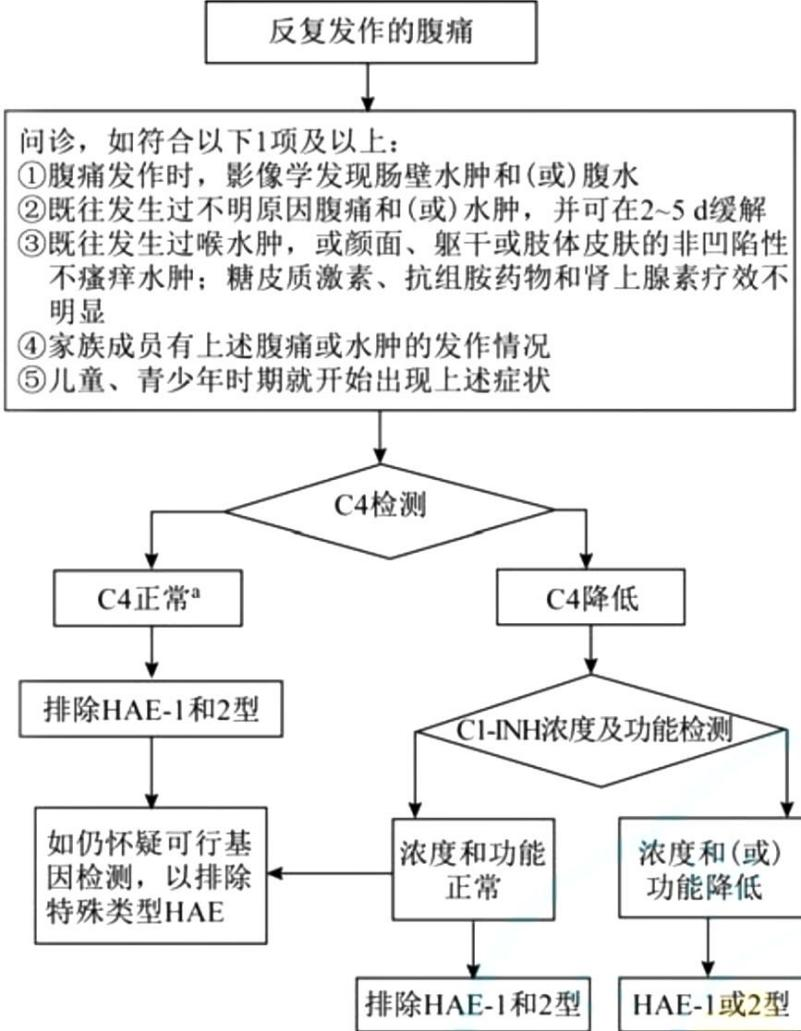
图5 消化科HAE患者诊断流程图
HAE的治疗主要包括急性发作期治疗、短期和长期预防性治疗。急性期治疗目的在于缓解症状,国内一线治疗用药是缓激肽受体拮抗剂艾替班特,血浆治疗为二线方案,禁食等为对症治疗[6]。对于所有明确诊断的HAE患者,建议使用药物进行长期预防治疗,如拉那利尤单抗,以减少HAE对日常生活的影响,防止致命性水肿的发生[7]。此外,家系筛查和避免诱发因素也是预防发作的重要环节。
总之,HAE不仅严重影响了患者的生活质量,甚至可能会累积呼吸道,致喉头水肿而窒息,对HAE的正确识别与治疗刻不容缓。希望通过本病例的分享,可以给消化科医师或者有类似疾病发作史的患者提供一些参考。
参考文献:
[1] 遗传性血管性水肿消化科诊疗协作组. 遗传性血管性水肿消化科诊疗路径. 中华消化杂志,2024,44(05):289-295.
[2]曹阳,刘爽,支玉香.遗传性血管性水肿发病机制研究进展[J].中国医学科学院学报,2020,42(05):686-690.
[3] Cao Y, Liu S, Zhi Y. Recurrent and acute abdominal pain as the main clinical manifestation in patients with hereditary angioedema. Allergy Asthma Proc. 2021 Mar 1;42(2):131-135.
[4] 王畅畅,李巍,董翔,等.以反复腹痛为主要表现的遗传性血管性水肿1例并文献复习[J].数理医药学杂志,2024,37(04):313-317.
[5] 支玉香,安利新,赖荷,等.遗传性血管性水肿的诊断和治疗专家共识[J].中华临床免疫和变态反应杂志,2019,13(01):1-4.
[6] 王瑜,田杵文,姚玲雅,等. 胃肠道发作为主要表现的遗传性血管性水肿[J]. 中华消化杂志,2024,44(04):277-279.
[7] Maurer M, Magerl M, Betschel S, et al. The international WAO/EAACI guideline for the management of hereditary angioedema-The 2021 revision and update[J]. Allergy. 2022 Jul;77(7):1961-1990.


