Gut:夏丽敏教授团队揭示肝脏免疫微环境失衡驱动肝癌恶性进展的全新机制
时间:2025-03-03 12:17:00 热度:37.1℃ 作者:网络
肝细胞癌(HCC)进展与转移的关键驱动因素在于其独特的免疫抑制性肿瘤微环境。该微环境以各类免疫细胞的功能失调为核心特征,其中免疫抑制性细胞通过破坏免疫稳态显著促进肿瘤演进。解析免疫抑制性肿瘤微环境的分子调控机制,特别是各类抑制性免疫细胞异常活化的关键通路,已成为优化肝癌免疫治疗策略的重要突破口。
2025年2月27日,华中科技大学附属同济医院夏丽敏教授课题组在国际消化病学领域顶级期刊《Gut》(IF: 23.1)在线发表题为“E-twenty-six-specific sequence variant 5 (ETV5) facilitates hepatocellular carcinoma progression and metastasis through enhancing polymorphonuclear myeloid-derived suppressor cell (PMN-MDSC)-mediated immunosuppression”的研究论著。率先鉴定发现全新髓源抑制性细胞亚群S100A9+MDSCs,揭示肝癌细胞与S100A9+MDSCs动态互作促进肝癌进展转移的信号调控网络。
该研究表明肝癌细胞中的ETV5通过促进肝癌细胞分泌S100A9,大量募集MDSC到肿瘤微环境,并诱导其分化为S100A9+MDSC并增强其免疫抑制活性。肿瘤内的S100A9+MDSC可以分泌抑制性细胞因子,同时细胞表面高表达PD-L1,抑制细胞毒性CD8+T细胞的浸润和活性。抗PD-L1单抗联合应用抗S100A9的单抗或S100A9受体的抑制剂,可产生协同抗肿瘤效应,在肝癌中表现出显著的疗效。

肝细胞癌是全球癌症相关死亡的第三大病因,其高复发转移特性严重制约患者预后。近年来,以纳武利尤单抗(抗PD-1)和阿替利珠单抗(抗PD-L1)为代表的免疫检查点阻断剂治疗革新了晚期肝细胞癌治疗格局。然而,大部分肝细胞癌患者对免疫治疗存在原发性耐药,无法获得显著生存获益。研究表明,以髓系来源抑制性细胞(MDSCs)为核心的免疫抑制微环境是导致治疗响应低下的关键机制。
MDSCs作为起源于髓系祖细胞的异质性免疫抑制细胞群,在肿瘤进展中呈现显著扩增与活化。根据表型特征可分为两大亚群:单核型MDSCs(M-MDSCs)和多形核MDSCs(PMN-MDSCs),其中PMN-MDSCs在肝细胞癌免疫微环境中占据主导地位。MDSCs通过多种机制驱动HCC进展,这类细胞通过上调免疫检查点表达、分泌抑制性细胞因子等机制,显著削弱细胞毒性T细胞的抗肿瘤功能。靶向MDSC细胞是治疗肝细胞癌的一种有前途的方法,但MDSCs与肿瘤细胞间的动态互作网络及其调控机制仍需系统解析。
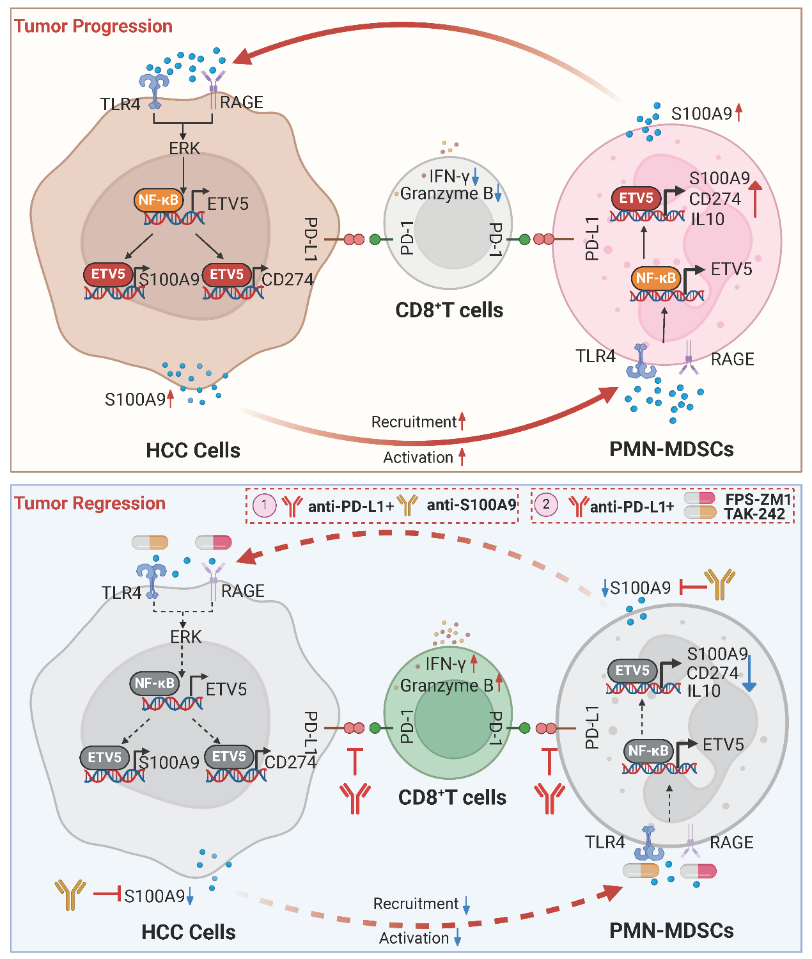
在本研究中,研究人员综合利用RNA-seq、ChIP-Seq和CUT&Tag等多种技术,结合多种小鼠肝癌模型,首次揭示肝癌细胞与MDSCs间的双向调控机制:
1)肝癌细胞通过转录因子ETV5直接激活S100A9的转录和分泌;
2)肿瘤源性S100A9通过配体-受体作用诱导S100A9+MDSCs在肿瘤微环境中的异常募集和活化;
3)S100A9+MDSCs内的ETV5转录激活PD-L1和S100A9的表达;
4)活化的S100A9+MDSCs通过分泌S100A9激活肝癌细胞ERK/NF-κB信号通路,进而正反馈上调ETV5表达,形成"ETV5-S100A9-ERK/NF-κB"自我维持环路。
基于上述机制,研究团队开发了具有自主知识产权的靶向S100A9的单克隆抗体。利用人源化小鼠模型证明S100A9中和阻断抗体联合PD-L1单抗可产生协同效应。联合治疗有效逆转了S100A9+MDSCs介导的免疫抑制微环境,并促进CD8+T细胞浸润与活化,显著抑制肝癌生长和转移。
本研究首次揭示肝癌细胞与S100A9+MDSCs之间的正反馈环路动态重塑肝癌免疫抑制微环境的分子机制,为肝癌免疫治疗提供了新型生物标志物,其靶向干预策略为开发基于微环境调控的联合免疫治疗方案提供了重要理论依据,具有显著的转化医学价值。
张泽睿博士为该论著的第一作者。华中科技大学附属同济医院消化内科夏丽敏教授为唯一通讯作者。该研究受到国家自然科学基金区域创新发展联合基金重点项目、面上项目、湖北省自然科学基金创新群体项目、华中科技大学基础研究发展支持计划项目的资助。感谢陈孝平院士、樊代明院士、吴开春教授、聂勇战教授、徐骁教授、张必翔教授、王帅教授、田德安教授、刘梅教授、丁则阳教授、张斌豪教授对该研究的大力支持和帮助。


