Eur Respir J:单细胞测序揭示BMPR2突变通过ID基因调节右心室功能
时间:2021-12-06 16:01:37 热度:37.1℃ 作者:网络

肺动脉高压(PAH)是一种进行性疾病,其病理特征包括肺微血管增厚和变窄,导致肺血管阻力升高和右心室肥厚,常导致右心室衰竭。在过去的 20 年里,在遗传性PAH患者中发现了 BMP 信号通路上的突变。 例如,已经在先天性心脏病相关 PAH (CHD-PAH) 患者中发现了 BMPR2 突变。 迄今为止,相关研究集中在肺血管重塑以了解具有 BMPR2 突变的 PAH/CHD-PAH 的病因。 PAH 患者的最终心力衰竭是否与原代心肌细胞(CM)的异常有关尚未阐明。
虽然之前的一项研究提供了证据表明心脏缺陷,包括室间隔缺损(VSD),可能是由小鼠胚胎 BMPR2 突变引起的,但由于与这种突变相关的寿命短,没有报道小鼠是否患有 PAH。 此外,最近的一项研究表明,具有 Bmpr2 单等位基因突变的大鼠在 6 个月后自发发展为 PAH,并且与 WT 大鼠相比,它们的右心室 CM 表现出降低的 Ca2+ 反应性。 非自发性 PAH 大鼠的心输出量甚至降低,进一步研究表明 Bmpr2 突变大鼠的右心室 CM 缺乏野生型大鼠 CM 的适应性。 在本报告之前,证据仅适用于 CHD-PAH 受试者的心脏缺陷,以支持我们的假设,即突变的 BMPR2 影响 PAH 患者的 CM。
DNA 结合蛋白 (ID) 的抑制剂是螺旋-环-螺旋 (HLH) 转录因子,据报道是心脏发生过程中 BMP 受体下游的重要靶标。 在我们之前的综述中,我们基于 Id 敲除 (KO) 小鼠和 BMPR2 mox-cre KO 小鼠的相似表型推测 BMPR2 通过下游效应基因 Id 在发育过程中有助于心脏形成。 最近的一项研究表明,Id 基因对心脏发育至关重要,因为小鼠中 Id 的四种亚型 (1-4) 的四重 KO 导致心脏发育缺失。 BMP 受体通过磷酸化的 Smad1/5 传递信号以诱导大多数细胞类型中的 IDs 表达,而 PAH/CHD-PAH 中报道的 BMPR2 和 BMP I 型受体的突变可能会影响 IDs,从而影响 CM 基因转录。
在先天性心脏病相关肺动脉高压 (CHD-PAH) 患者中发现了骨形态发生蛋白 II 型受体 (BMPR2) 的突变。在本研究中,我们的数据阐明缺陷 BMPR2 信号是否通过下游效应器、DNA 结合蛋白 (ID) 抑制剂在心脏发育过程中起作用,从而促进 CHD 患者 PAH 的进展。
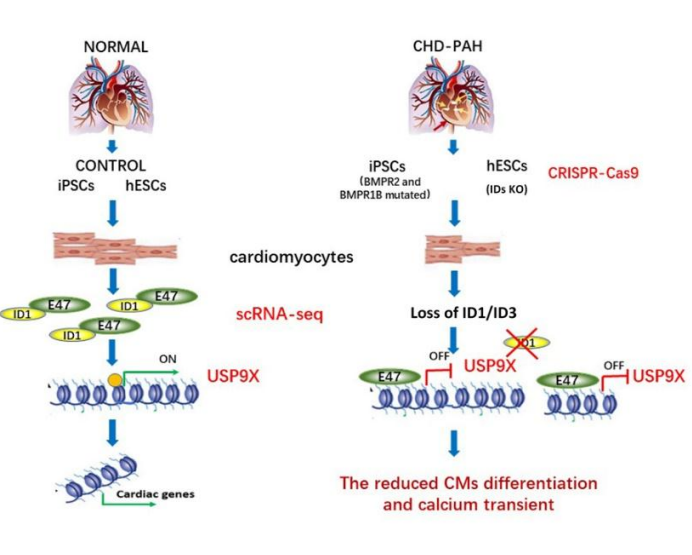
为了确认 ID 是心脏中胚层祖细胞 (CMP) 中 BMPR2 信号传导的下游效应器并有助于 PAH,我们生成了心肌细胞 (CM) 特异性Id 1/3敲除小鼠 (Ids cDKO),并且约48%的小鼠可形成轻度 PAH,并改变了血流动力学指标和肺血管重构。此外,我们生成了ID1和ID3双基因敲除 (IDs KO) 人类胚胎干细胞,重现了 CHD-PAH iPSC 的 BMPR2 信号传导缺陷。共聚焦显微镜实验证明,从具有 BMPR 突变的 CHD-PAH 患者衍生的诱导多能干细胞 (iPSC) 分化出的 CM 表现出功能失调的心脏分化和减少的 Ca 2+瞬变。在 CHD-PAH iPSC 和Bmpr2 +/-大鼠右心室中,Smad1/5 磷酸化和 ID1 和 ID3 表达降低。此外,超声显示 33% 的 Ids cDKO 小鼠在其室间隔和肺反流中有可检测的缺陷。从小鼠右心室分离的 CM 也显示出降低的 Ca 2+瞬变和缩短的肌节。单细胞RNA测序数据分析显示,与野生型 (WT) 细胞相比,IDs KO 细胞中 CMP 的分化受损和 USP9X 表达下调。我们发现 BMPR2 通过 IDs 和 USP9X 发出信号来调节心脏分化,ID1 和 ID3 表达的丧失导致BMPR2突变的CHD-PAH 患者的 CM 功能障碍。
参考文献:
Du M, Jiang H, Liu H, Zhao X, Zhou Y, Zhou F, Piao C, Xu G, Ma F, Wang J, Perros F, Morrell NW, Gu H, Yang J. Single-cell RNA sequencing reveals that BMPR2 mutation regulates right ventricular function via ID genes. Eur Respir J. 2021 Dec 2:2100327. doi: 10.1183/13993003.00327-2021. Epub ahead of print. PMID: 34857612.


