Nature子刊 | 华中科技大学陈科/胡俊逸/陈朝晖等合作发现膀胱癌的潜在治疗新靶点
时间:2022-12-29 11:59:49 热度:37.1℃ 作者:网络
单细胞测序技术显著提高了对膀胱癌(BC)遗传图谱和分子特征的理解。
2022年11月8日,华中科技大学陈科、胡俊逸、陈朝晖和天津医科大学陶振共同通讯在Nature Communications 发表题为“Single cell sequencing reveals that CD39 inhibition mediates changes to the tumor microenvironment”的研究论文,该研究通过单细胞转录组分析将CD39确定为BC的潜在治疗靶点。在皮下肿瘤模型和原位膀胱癌模型中,多氧钨酸钠抑制CD39(CD39i)能够限制BC的生长并提高荷瘤小鼠的总生存期。
通过单细胞RNA测序,发现CD39i增加了肿瘤内NK细胞,常规1型树突状细胞(cDC1)和CD8+ T细胞并降低了Treg丰度。此外,CD39i和顺铂之间观察到显着的协同作用,但CD39i+抗PD-L1(或抗PD1)策略在BC模型中没有显示出任何协同作用。总之,该研究结果证实CD39是BC免疫治疗的潜在靶标。

膀胱癌(BC)是全球最普遍的癌症之一,大约75%的新诊断BC是非肌肉侵入性(NMIBC)。尽管治疗和早期诊断已大幅改善,但BC相关死亡率仍然很高。因此,显然需要进一步改进BC患者的诊断和治疗技术。对于NMIBC,局部肿瘤切除后膀胱内卡介苗(BCG)免疫疗法在过去30年中得到了有效应用,51%的患者患有复发性疾病,19%的患者进展为肌肉浸润性疾病。,
相比之下,肌层浸润性和晚期膀胱癌的系统管理包括切除整个器官(膀胱切除术)和主要基于铂类化疗的尿路分流。然而,并非所有患者都对基于顺铂(CIS)的新辅助化疗有反应,只有50%的患者可以从常规化疗中受益。人们对免疫检查点阻断(ICB)治疗越来越感兴趣,因为抗PD1(aPD1)和抗PD-L1(aPD-L1)治疗已逐渐成为局部晚期或转移性尿路上皮癌患者标准的一部分,这些患者在基于CIS的化疗后复发或被认为不符合CIS条件,但客观缓解率仅为20%。
最近,研究者生成了BC患者8个肿瘤样本和3个副肿瘤样本的单细胞图谱,揭示了不同分子亚型之间的不同成分和微环境特征,这可能导致对化疗或其他靶向治疗的不同反应,强调了开发个性化治疗的必要性。CD39,也称为外核苷三磷酸二磷酸水解酶-1,是一种由ENTPD1基因编码的跨膜蛋白。它可以在5'-核苷酸酶(CD73)的协同作用下,通过级联反应将ATP和ADP转化为免疫抑制腺苷(ADO)。
该研究发现CD39在BC组织中显著过表达,并与免疫抑制有关。CD39水平较高的患者从aPD-L1治疗中获得益处的潜力较小。通过皮下模型,证明了多氧钨酸钠(POM-1,一种新型ENTPDase抑制剂)对CD39(CD39i)的抑制作用可以抑制BC生长并改善体内预后,这与癌组织中CD8+ T细胞和常规1型树突状细胞(cDC1)的浸润水平增加有关。此外,还发现CD39i与CIS具有协同作用,CIS是一种广泛用于BC临床治疗的化疗药物,而不是与免疫治疗剂(aPD1或aPD-L1)联合使用。总的来说,这些结果表明CD39i作为BC的治疗靶点的可能性,CD39i和CIS的组合可能是首选的治疗方法。
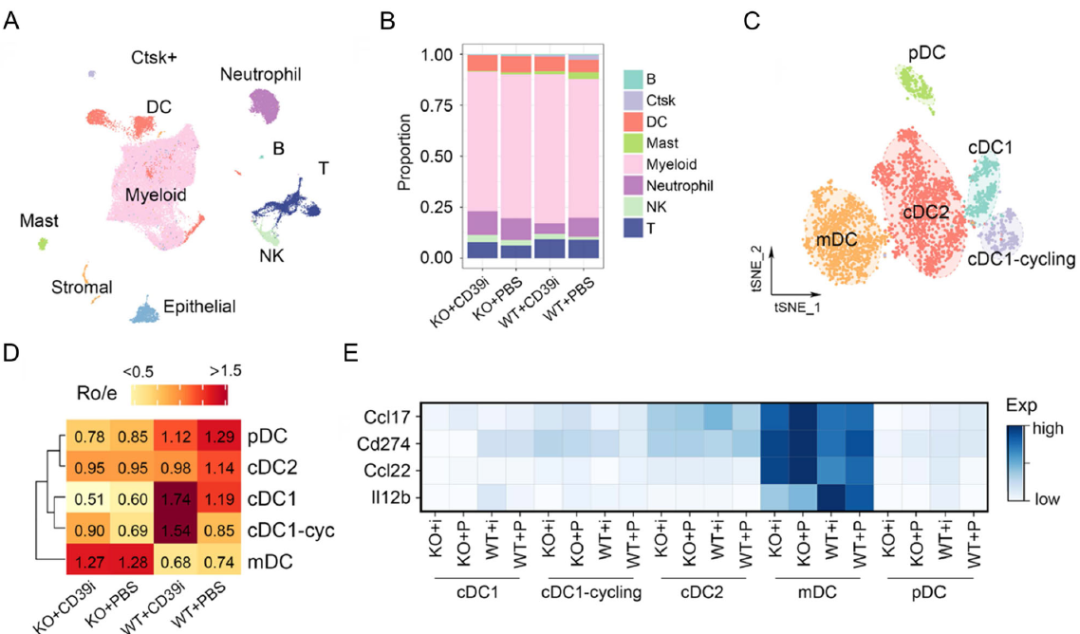
Batf3−/− cDC1缺失对肿瘤微环境及CD39i疗效的影响(图源自Nature Communications )
总之,使用单细胞测序,研究提供了CD39i介导的肿瘤微环境中变化的全景视图,并增强了对CD39i作用的理解。CD39i通过增加肿瘤浸润NK细胞,cDC1和循环CD8+ T细胞的比例来发挥抗肿瘤作用。同时,研究工作提供了基于CD39i的联合方案,为临床转化奠定了坚实的基础。
参考消息:
https://doi.org/10.1038/s41467-022-34495-z


