给肾动脉狭窄患者做支架置入,到底有没有用?【深度探讨】
时间:2024-05-21 18:00:07 热度:37.1℃ 作者:网络
肾动脉狭窄的定义和病因
有临床意义的肾动脉狭窄(renal artery stenosis,RAS)指肾动脉狭窄程度>肾动脉直径的50%,其不仅是继发性高血压(hypertension,HT)的首要原因,还能引起缺血性肾病,诱发急性冠脉综合征及爆发性肺水肿。若不予及时合理的治疗,病情可进行性加重,危及患者生命。
动脉粥样硬化是肾动脉狭窄的首要病因,动脉粥样硬化性肾动脉狭窄(atherosclerotic renal artery stenosis, ARAS)占比90%以上。基于目前庞大的老年、HT、动脉粥样硬化和慢性肾脏疾病人群基数推测ARAS有着巨大的患病人群总数,再结合考虑其所带来的危害,我们认为ARAS的治疗是一项非常值得研究的临床问题。
ARAS病理生理
在进一步阐述ARAS的治疗前,笔者认为详细地理解RAS造成的病理生理学变化极为重要。RAS导致的直接效应是患肾的灌注减低,肾小球滤过率减低,并由此引起以下病理生理改变及相应的临床表现:
-
第一,可出现肾素-血管紧张素系统的激活(单侧肾动脉狭窄)。循环肾素、血管紧张素及醛固酮水平增高,从而引起外周血管阻力增加,心脏、神经系统、血管及肾脏等靶器官损害。临床表现为顽固性HT、心肌肥厚、卒中等不良心血管事件;
-
第二,血管容量负荷过重,常见于双侧肾动脉狭窄或单功能肾,可伴肾素-血管紧张素系统抑制。临床表现为顽固性HT、心衰反复发作;
-
第三,肾组织缺血、缺氧,激活炎症反应及纤维化进展,临床表现为肾功能损伤。
ARAS治疗
3.1 药物治疗
药物治疗包括病因及降压治疗两个方面。
-
动脉粥样硬化的病因治疗主要针对危险因素,包括戒烟、降脂、控制血压,抗血小板和降糖治疗等,重点是降脂治疗。
-
降压治疗常用的降压药物均无绝对禁忌。需要强调的有两点:
一是肾动脉狭窄并非使用ACEI/ARB类降压药物的禁忌证。这点常被不在少数的临床大夫误解,反而因其对RAS引起的病理生理学的变化针对性作用,ACEI/ARB类降压药物被指南推荐用于大部分ARAS患者,但是在单功能肾或双侧肾动脉重度狭窄的患者需慎用。因为血管紧张素对出球动脉的扩张作用大于入球动脉,对这类患者使用ACEI/ARB类降压药可能因肾小球滤过压进一步降低引起肾功能恶化;
二是利尿剂,因其对肾素-血管紧张素系统的进一步激活不作首选药物,仅在使用其他药物血压不达标或不耐受后推荐加用。其他相关药物治疗参考动脉粥样硬化性疾病及高血压管理相关指南不再赘述,本文着重阐明ARAS的介入治疗。
3.2 介入治疗
根据RAS的病理生理变化我们可知,解除肾动脉梗阻,恢复肾动脉血流对RAS患者至关重要,即再血管化治疗应该为RAS的根本治疗措施。
早在1974年,Hunt等就证实,与单纯药物治疗相比,通过外科旁路移植手术的方式可使RAS患者血压得到良好的控制,肾功能改善,心肌梗死、卒中发病率及死亡率降低。与外科手术相比,介入治疗可以在更小的创伤及更低的系统并发症发生率基础上实现同等的再血管化治疗效果。
目前一般推荐经皮介入治疗作为肾动脉血管重建的首选方法,血管外科直视手术仅适用于某些特殊情况:① 病变不适合行介入治疗;② 病变肾动脉附近腹主动脉需要外科重建;③ 介入治疗失败的补救措施;③ 对比剂严重过敏;④ 服用抗血小板药物有禁忌等。
介入治疗包括单纯经皮肾动脉腔内球囊扩张成型术(percutaneous transluminal renal angioplasty, PTRA)和经皮肾动脉腔内球囊扩张成型及支架置入术(percutaneous renal angioplasty and stenting, PTRAS)。PTRA可适用于非动脉粥样硬化所致的RAS,包括纤维肌性发育不良(fibromuscular dysplasia, FMD)和大动脉炎。然而由于ARAS狭窄即斑块位置常位于肾动脉开口,且斑块较大,PTRA常常手术成功率较低(PTRA术后残余狭窄>30%)且伴较高的再狭窄率;因此,PTRAS目前是ARAS的首选再血管化治疗方案。
目前,国内外针对肾动脉狭窄介入治疗指征的指南与专家共识仍基于临床经验,尚缺乏统一、高水平循证医学证据支持。在ARAS的介入治疗仍存在着争议,为数不多的随机对照研究(randomized control trial,RCT)并未发现肾动脉介入治疗与单纯优化的药物治疗相比存在显著优势。究其原因包括:研究对象的选择偏移,非硬性的研究终点,过高的意向性分析率,过高的并发症发生率及单中心年纳入研究对象数量过少等。这些局限性共同导致了这些RCT研究证据强度一般,研究结论未被广泛认可。其中,最主要的争议点在对研究对象的不恰当选择上即纳入的研究人群不太可能受益于PTRAS。也正是因为这些广泛争议的存在,国内外与ARAS管理相关的指南更新速度也较慢。为了方便大家参考,笔者用下表(表1)总结了ARAS接受介入治疗的指南和共识推荐。
表1 国内外指南与专家共识关于动脉粥样硬化性肾动脉狭窄的介入治疗推荐
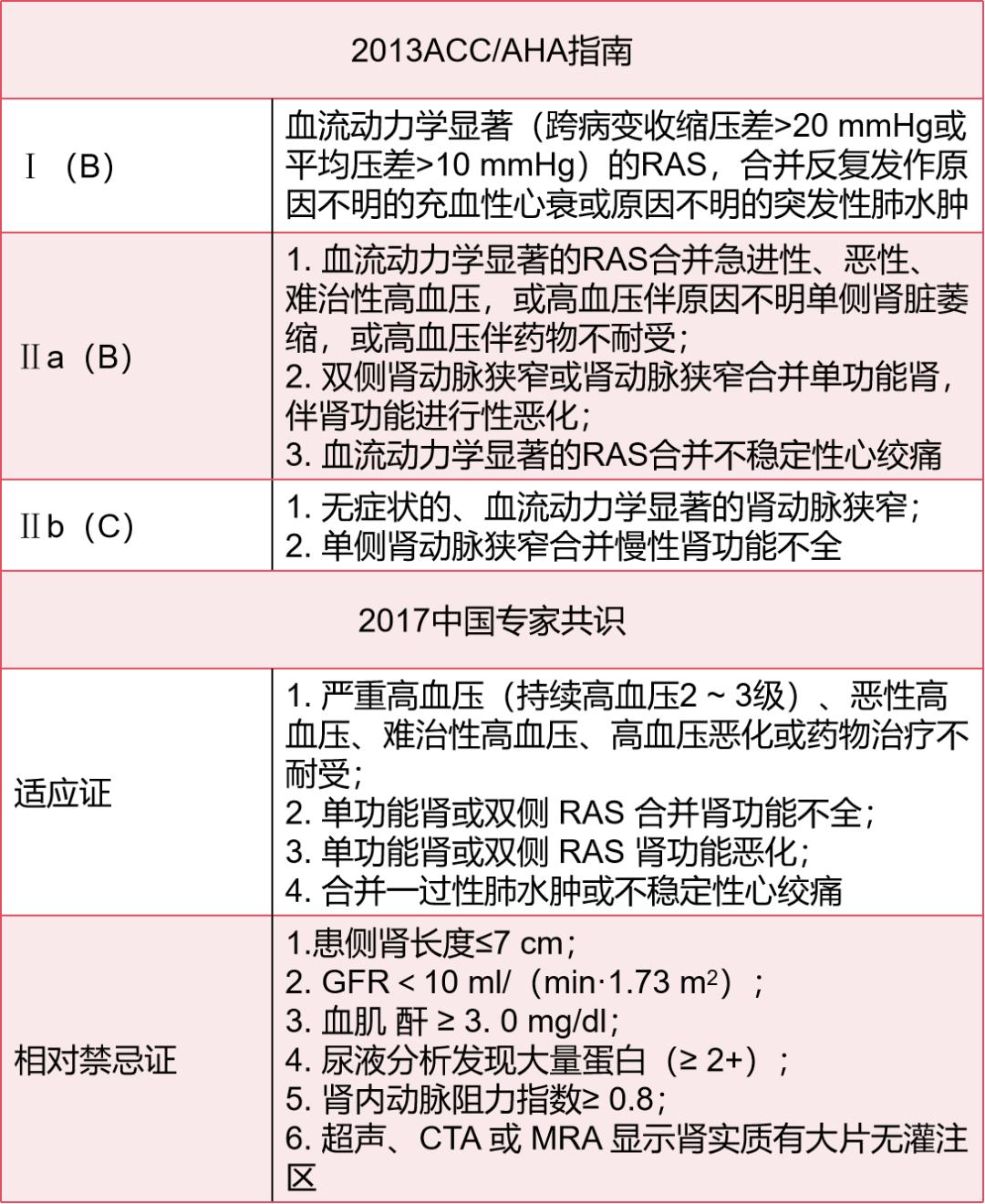
总结
提到ARAS的介入治疗,很多医生和学者会讲“大型临床试验的结果表明肾动脉支架置入不能改善ARAS患者的预后”,形成了“多数人的声音即共识”的现状:ARAS的患者不应该接受支架置入治疗。但笔者认为我们需要更加辩证地去分析这个问题。
-
首先,我们不能单纯摘取某个或某几个临床研究文章的结论来当做指南进行参考,因为临床研究的人群是限定的。比如CORAL研究除外了肾动脉狭窄程度>80%的患者,最终纳入患者的狭窄程度为67.3%±11.4%。但是对于造影判定中等狭窄程度(50%~70%)的病变并未测量有创压力去明确因狭窄带来的灌注减低;ASTRAL研究中PTRAS组中仅有60%的患者狭窄程度>70%,设计时研究者更是排除了临床医师确定可从PTRAS中获益的ARAS。也就是说这些研究的结论其实对狭窄程度极重的患者是不适用的,一味迷信RCT的结论必然造成治疗不足的情况。
-
其次,ARAS又是一个具有高度异质性的群体,肾动脉的狭窄和常见临床表现高血压、肾功能不全方面存在不同的因果逻辑关系。高血压、肾功能不全是动脉粥样硬化的危险因素,自然也是ARAS的危险因素,患者有高血压、肾功能不全合并ARAS并不意味着是继发于ARAS;还有可能是长期原发性高血压造成肾小球中小动脉玻璃样变硬化,进而引起肾功能不全,高血压和肾功能不全共同引起动脉粥样硬化进展,ARAS和肾功能受损为高血压靶器官损害表现。如果为后一种临床逻辑,那么若以血压水平和肾功能改善为终点事件,PTRAS对ARAS获益就会受限。
综上所述,明确ARAS人群行PTRAS的适应证对ARAS患者的预后及PTRAS的合理应用至关重要。在介入治疗技术进步(桡动脉通路、无接触技术、导管内导管技术)的同时,我们需要系统性结合临床特点、生物标记物、无创性影像学特征及介入治疗相关的指标进行多模态的分析,去探寻ARAS患者获益于PTRAS的因素,为临床提供更有价值的治疗指导。我们中心目前也参与了一项北京大学第一医院李建平教授牵头的“在肾动脉狭窄高血压患者中利用血流储备分数指导肾动脉介入治疗策略的可行性研究”,期待其能为PTRAS的应用提供更有价值的指导证据。



