Cancer Cell:复旦大学樊嘉等团队合作首次绘制肝癌转移的时空多组学演化图谱
时间:2023-12-17 14:41:10 热度:37.1℃ 作者:网络
目前缺乏对转移性肝细胞癌(HCC)的全面分子分析。
2023年12月14日,复旦大学樊嘉、孙云帆、上海科技大学张力烨及上海顿慧医疗彭海翔共同通讯在Cancer Cell 在线发表题为“Integrated multi-omics profiling to dissect the spatiotemporal evolution of metastatic hepatocellular carcinoma”的研究论文,该研究对182例HCC患者的257个原发区和176个转移区进行了多组学分析,发现原发肿瘤富含缺氧特征,有利于多克隆传播。原发性和转移性HCC之间的基因组差异很大,早期传播很普遍。在转移中观察到的显著的肿瘤内新抗原异质性与T细胞反应性下降有关,这是由于新抗原呈递被破坏造成的。
该研究确定克隆在转移方面比那些有Wnt突变的亚克隆表现出更强的选择优势,并且其特征是微环境中富含激活的成纤维细胞,有利于前转移表型。最后,没有Wnt突变的转移灶表现出更高的免疫抑制B细胞富集,这些B细胞通过HLA-E:CD94-NKG2A检查点轴介导CD8+ T细胞的终端衰竭。总的来说,该结果提供了一个复杂的转移进化过程的多维剖析。

肝癌是全球癌症死亡的第三大原因,其中肝细胞癌(HCC)占大多数高达60%的局部可切除的患者在诊断后5年仍然存活,而远处转移的患者只有4%由于转移在很大程度上仍然无法治愈,了解这一过程对于改善晚期HCC患者的预后非常重要。
一些大规模的测序工作对驱动HCC发病机制的关键遗传和转录过程产生了有价值的见解。然而,大多数分析都是针对原发性HCC进行的,很少有测序转移。尽管转移瘤与原发瘤具有共同的关键驱动基因改变或转录程序,但它们在播散和治疗过程中往往会发展出新的性状。随着高度异质性的原发病变和可能更均匀的转移的演变,迫切需要通过测序匹配的原发和转移肿瘤获得转移性疾病的全面遗传和分子景观,以阐明生物学基础并确定更有效的HCC转移治疗策略。
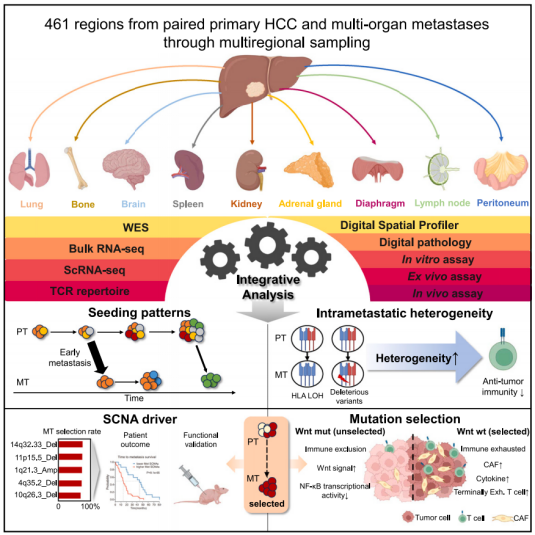
机理模式图(图源自Cancer Cell )
该研究对182例HCC患者的257个原发区和176个转移区进行了多组学分析,发现原发肿瘤富含缺氧特征,有利于多克隆传播。原发性和转移性HCC之间的基因组差异很大,早期传播很普遍。在转移中观察到的显著的肿瘤内新抗原异质性与T细胞反应性下降有关,这是由于新抗原呈递被破坏造成的。
该研究确定克隆在转移方面比那些有Wnt突变的亚克隆表现出更强的选择优势,并且其特征是微环境中富含激活的成纤维细胞,有利于前转移表型。最后,没有Wnt突变的转移灶表现出更高的免疫抑制B细胞富集,这些B细胞通过HLA-E:CD94-NKG2A检查点轴介导CD8+ T细胞的终端衰竭。总之,该研究基于多组学平台,首次系统刻画了肝癌转移的时空演进全景图谱,揭示了肝癌转移的复杂进化轨迹和克隆选择机制,为研发肝癌转移预测的新标志物和治疗新靶点提供了宝贵的数据和理论基础。
复旦大学附属中山医院樊嘉院士、上海科技大学张力烨研究员、复旦大学附属中山医院孙云帆副研究员及上海顿慧医疗彭海翔博士为本文共同通讯作者,孙云帆副研究员、吴频博士、张泽凡博士、王泽健博士、周恺乾博士、宋敏芳博士、纪元教授、臧凤琳教授为本文共同第一作者。该课题得到了国家自然科学基金、上海市创新集群等项目资助,顿慧医疗和上海科技大学超算中心为多组学数据产出和生物信息分析提供了大力支持。
原文链接:
https://www.cell.com/cancer-cell/fulltext/S1535-6108(23)00401-4


